名校
1 . 丙烯是重要的化工原料,广泛用于合成聚丙烯、丙烯醛等工业领域。回答下列问题:
(1)丙烷无氧脱氢法制备丙烯的反应为 。科学上规定:在298.15K时,由最稳定的单质生成1mol化合物时的焓变,叫作该物质的标准摩尔生成焓(
。科学上规定:在298.15K时,由最稳定的单质生成1mol化合物时的焓变,叫作该物质的标准摩尔生成焓( );最稳定的单质的标准摩尔生成焓为零。
);最稳定的单质的标准摩尔生成焓为零。
已知:部分物质的标准摩尔生成焓数据如表:
则上述反应的
______  。
。
(2)T1℃时,将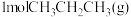 充入某刚性密闭容器中,在催化作用下发生无氧脱氢反应。用压强传感器测出容器内体系压强随时间的变化关系如表所示:
充入某刚性密闭容器中,在催化作用下发生无氧脱氢反应。用压强传感器测出容器内体系压强随时间的变化关系如表所示:
①已知: 。
。 内,用H2的分压变化表示上述脱氢反应的平均速率为
内,用H2的分压变化表示上述脱氢反应的平均速率为______  。
。
②T1℃时,反应的平衡常数
______  。
。 随反应温度升高而
随反应温度升高而______ (填“增大”“减小”或“不变”)。
(3)丙烷在有氧气参与的条件下也可以发生脱氢反应: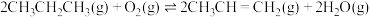 。下列说法正确的是______(填序号)。
。下列说法正确的是______(填序号)。
(4)甲醇催化也可以制取丙烯,其反应为
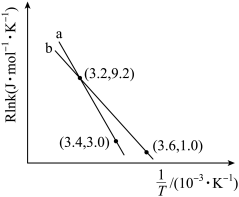
①该反应的阿伦尼乌斯经验公式的实验数据如图中直线a所示,已知阿伦尼乌斯经验公式为 (
( 为活化能,k为速率常数,R和C为常数)。则该反应的活化能
为活化能,k为速率常数,R和C为常数)。则该反应的活化能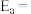
______  。
。______ (填序号)。
a.升高温度 b.增大压强 c.增大
(1)丙烷无氧脱氢法制备丙烯的反应为
 。科学上规定:在298.15K时,由最稳定的单质生成1mol化合物时的焓变,叫作该物质的标准摩尔生成焓(
。科学上规定:在298.15K时,由最稳定的单质生成1mol化合物时的焓变,叫作该物质的标准摩尔生成焓( );最稳定的单质的标准摩尔生成焓为零。
);最稳定的单质的标准摩尔生成焓为零。已知:部分物质的标准摩尔生成焓数据如表:
物质 | CH3CH2CH3(g | )CH3CH=CH2(g) |
| -104 | 19.8 |

 。
。(2)T1℃时,将
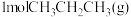 充入某刚性密闭容器中,在催化作用下发生无氧脱氢反应。用压强传感器测出容器内体系压强随时间的变化关系如表所示:
充入某刚性密闭容器中,在催化作用下发生无氧脱氢反应。用压强传感器测出容器内体系压强随时间的变化关系如表所示:时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
压强/kPa | 100 | 136 | 163 | 178 | 180 | 180 | 180 |
 。
。 内,用H2的分压变化表示上述脱氢反应的平均速率为
内,用H2的分压变化表示上述脱氢反应的平均速率为 。
。②T1℃时,反应的平衡常数

 。
。 随反应温度升高而
随反应温度升高而(3)丙烷在有氧气参与的条件下也可以发生脱氢反应:
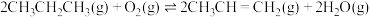 。下列说法正确的是______(填序号)。
。下列说法正确的是______(填序号)。| A.相对于丙烷直接催化脱氢法,有氧气催化脱氢,反应更容易进行 |
| B.相同条件下,氢气、丙烯、丙烷三种气体中,还原性最强的是氢气 |
| C.恒温恒容条件下,当混合气体的密度不再随时间改变时,说明反应达到限度 |
| D.通入更多的氧气,有利于提高丙烷转化率,提高丙烯的产率 |
(4)甲醇催化也可以制取丙烯,其反应为

①该反应的阿伦尼乌斯经验公式的实验数据如图中直线a所示,已知阿伦尼乌斯经验公式为
 (
( 为活化能,k为速率常数,R和C为常数)。则该反应的活化能
为活化能,k为速率常数,R和C为常数)。则该反应的活化能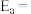
 。
。
a.升高温度 b.增大压强 c.增大

您最近半年使用:0次
名校
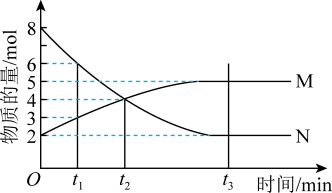
2 . Ⅰ.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图: 时刻,正逆反应速率大小
时刻,正逆反应速率大小
___________  。(填“>”“=”或“<”)
。(填“>”“=”或“<”)
(2)若 min,计算反应开始至
min,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率___________ 。
(3) 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为___________ 。
(4)写出反应的化学方程式___________ 。
(5)如果升高温度,则
___________ (填“增大”“减小”或“不变”)。
Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(6)①本实验待测数据可以是___________ ,实验Ⅰ和实验Ⅱ可以探究___________ ,对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是___________ 。
(7)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中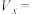
___________ 。
 时刻,正逆反应速率大小
时刻,正逆反应速率大小
 。(填“>”“=”或“<”)
。(填“>”“=”或“<”)(2)若
 min,计算反应开始至
min,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率(3)
 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为(4)写出反应的化学方程式
(5)如果升高温度,则

Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
| 序号 | 纯锌粉/g | 2.0 硫酸溶液/mL 硫酸溶液/mL | 温度/℃ | 硫酸铜固体/g | 加入蒸馏水/mL |
| Ⅰ | 2.0 | 50.0 | 25 | 0 | 0 |
| Ⅱ | 2.0 | 40.0 | 25 | 0 | 10.0 |
| Ⅲ | 2.0 | 50.0 | 25 | 0.2 | 0 |
| Ⅳ | 2.0 | 50.0 | 25 | 4.0 | 0 |
(6)①本实验待测数据可以是
②实验Ⅲ和实验Ⅳ的目的是
(7)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | ||||
 溶液 溶液 | 水 | KI溶液 |  溶液 溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 |  | 4.0 | 4.0 | 2.0 |
您最近半年使用:0次
名校
3 . 对水样中影响M分解速率的因素进行研究。在相同温度下,M的物质的量浓度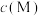 随时间(t)的变化如图所示。下列说法正确的是
随时间(t)的变化如图所示。下列说法正确的是
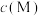 随时间(t)的变化如图所示。下列说法正确的是
随时间(t)的变化如图所示。下列说法正确的是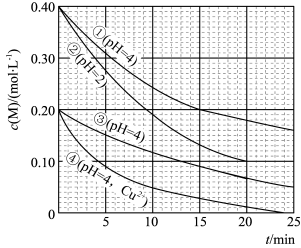
| A.水样pH越大,M的分解速率越大 |
B.水样中添加 ,能减小M的分解速率 ,能减小M的分解速率 |
| C.由①③得,反应物浓度越大,M的分解速率越小 |
D.在0~20min内,②中M的分解速率为0.015 |
您最近半年使用:0次
解题方法
4 . 甲烷和乙炔(CH≡CH)在有机合成中有着广泛的用途。
(1)已知:①
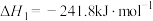
②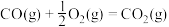

③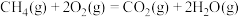
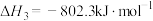
写出甲烷与水蒸气在高温下制备合成气(CO、 )的热化学方程式:
)的热化学方程式:___________ 。
(2)用甲烷在高温下气相裂解制取乙炔和氢气,其反应原理为
 。几种气体平衡时分压(Pa)的对数与温度(K)的关系如图所示。
。几种气体平衡时分压(Pa)的对数与温度(K)的关系如图所示。
___________ (用气体平衡分压代替浓度计算)。
② ℃时,向体积为2L的恒容密闭容器中充入
℃时,向体积为2L的恒容密闭容器中充入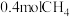 进行上述反应。当反应达到平衡时,测得
进行上述反应。当反应达到平衡时,测得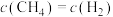 ,则
,则 的转化率为
的转化率为___________ 。若改变温度至 ℃,10s后反应再次达到平衡,测得
℃,10s后反应再次达到平衡,测得 ,则该变化过程中
,则该变化过程中
___________ (填“>”或“<”) 。
。
(3)一定温度下,向体积为2L的恒容密闭容器中充入 (乙炔)和2molHCl发生反应:
(乙炔)和2molHCl发生反应: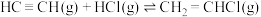
 。测得反应物(
。测得反应物( 或HCl)浓度随时间的变化关系如图所示。
或HCl)浓度随时间的变化关系如图所示。
___________ (填“>”“<”或“=”) 。
。
②15min时仅改变了一个外界条件,改变的条件可能是___________ 。
③0~10min内氯乙烯的平均反应速率
___________  。向密闭容器中充入一定量乙炔和氯化氢,发生上述反应,测得乙炔的平衡转化率与温度、S的关系如图所示。其中
。向密闭容器中充入一定量乙炔和氯化氢,发生上述反应,测得乙炔的平衡转化率与温度、S的关系如图所示。其中 ,则S代表的物理量是
,则S代表的物理量是___________ 。
(1)已知:①

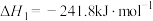
②
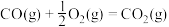

③
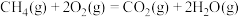
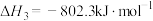
写出甲烷与水蒸气在高温下制备合成气(CO、
 )的热化学方程式:
)的热化学方程式:(2)用甲烷在高温下气相裂解制取乙炔和氢气,其反应原理为

 。几种气体平衡时分压(Pa)的对数与温度(K)的关系如图所示。
。几种气体平衡时分压(Pa)的对数与温度(K)的关系如图所示。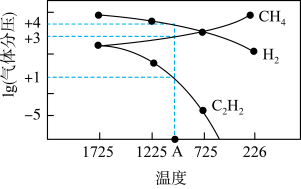

②
 ℃时,向体积为2L的恒容密闭容器中充入
℃时,向体积为2L的恒容密闭容器中充入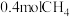 进行上述反应。当反应达到平衡时,测得
进行上述反应。当反应达到平衡时,测得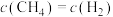 ,则
,则 的转化率为
的转化率为 ℃,10s后反应再次达到平衡,测得
℃,10s后反应再次达到平衡,测得 ,则该变化过程中
,则该变化过程中
 。
。(3)一定温度下,向体积为2L的恒容密闭容器中充入
 (乙炔)和2molHCl发生反应:
(乙炔)和2molHCl发生反应: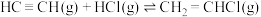
 。测得反应物(
。测得反应物( 或HCl)浓度随时间的变化关系如图所示。
或HCl)浓度随时间的变化关系如图所示。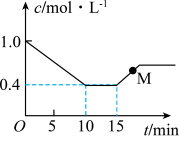

 。
。②15min时仅改变了一个外界条件,改变的条件可能是
③0~10min内氯乙烯的平均反应速率

 。向密闭容器中充入一定量乙炔和氯化氢,发生上述反应,测得乙炔的平衡转化率与温度、S的关系如图所示。其中
。向密闭容器中充入一定量乙炔和氯化氢,发生上述反应,测得乙炔的平衡转化率与温度、S的关系如图所示。其中 ,则S代表的物理量是
,则S代表的物理量是
您最近半年使用:0次
解题方法
5 . 按要求回答下列问题:
(1)下列变化中属于吸热反应的是_______ 。
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化 ④氯酸钾分解制氧气 ⑤甲烷在氧气中的燃烧反应
(2)反应C(s)+H2O(g) CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是_______ 。
①增加C的量
②将容器的体积缩小一半
③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积变大
(3)在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:

①从3min到9min,v(CO2)=_______ (结果保留两位有效数字);a点时v(正)_______ v(逆)(填>、<或=)。
②若已知生成标准状况下2.24LCH3OH(g)时放出热量为4.9kJ,而上述反应的实际放热量总小于49kJ,其原因是_______ 。
(4)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示。
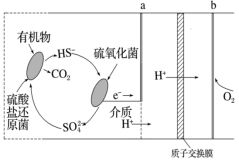
①该微生物燃料电池,负极为_______ (填“a”或“b”)。
②该电池正极电极反应式为_______ 。
③当电路中有0.5mol电子发生转移,则有_______ mol的H+通过质子交换膜。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化 ④氯酸钾分解制氧气 ⑤甲烷在氧气中的燃烧反应
(2)反应C(s)+H2O(g)
 CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是①增加C的量
②将容器的体积缩小一半
③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积变大
(3)在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
①从3min到9min,v(CO2)=
②若已知生成标准状况下2.24LCH3OH(g)时放出热量为4.9kJ,而上述反应的实际放热量总小于49kJ,其原因是
(4)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示。

①该微生物燃料电池,负极为
②该电池正极电极反应式为
③当电路中有0.5mol电子发生转移,则有
您最近半年使用:0次
6 . 中国科学家设计构建了结构封装双钯活性位点—纳米“蓄水”膜反应器,实现了 一步无副反应高效稳定制乙醇。回答下列问题:
一步无副反应高效稳定制乙醇。回答下列问题:
(1)已知乙醇、氢气的标准燃烧热 分别为
分别为 、
、 ,则反应
,则反应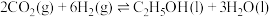 的
的
___________  ,该反应在
,该反应在___________ (填“高温下”“低温下”或“任何温度下均”)有利于自发进行。
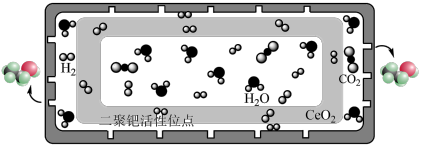
(2)结构封装双钯活性位点—纳米“蓄水”膜反应器结构(如图所示)类似于一个胶囊,胶囊内部封装了二氧化铈载体分散的双钯催化剂,胶囊的壳层具有高选择性、疏水性,可及时分离出产物乙醇。该反应器可使 高效稳定地转化为乙醇,请分析可能原因:
高效稳定地转化为乙醇,请分析可能原因:___________ 。
(3)在一恒压密闭容器中充入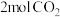 、
、 ,发生主反应I
,发生主反应I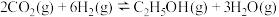 、副反应II
、副反应II 。已知初始压强为
。已知初始压强为 ,反应
,反应 时,测得
时,测得 下,总共生成
下,总共生成 水。甲醇与乙醇的选择性[如
水。甲醇与乙醇的选择性[如 的选择性
的选择性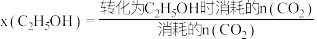 ]随温度和反应时间的变化关系如图。
]随温度和反应时间的变化关系如图。
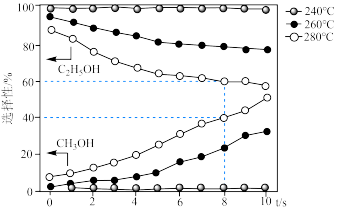
①在 下,当温度为
下,当温度为 时,乙醇的选择性能保持在近
时,乙醇的选择性能保持在近 的水平,但温度为
的水平,但温度为 和
和 时选择性大幅下降,其原因可能为
时选择性大幅下降,其原因可能为___________ 。
② 下,
下, 内
内 的转化率为
的转化率为___________ %,氢气分压的平均变化率为___________  。
。
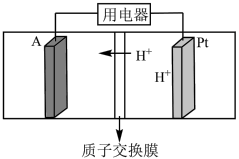
(4)酸性 燃料电池的装置图如图所示,A极输入的物质为
燃料电池的装置图如图所示,A极输入的物质为___________ (填化学式), 极的电极反应式为
极的电极反应式为___________ 。
 一步无副反应高效稳定制乙醇。回答下列问题:
一步无副反应高效稳定制乙醇。回答下列问题:(1)已知乙醇、氢气的标准燃烧热
 分别为
分别为 、
、 ,则反应
,则反应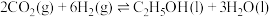 的
的
 ,该反应在
,该反应在(2)结构封装双钯活性位点—纳米“蓄水”膜反应器结构(如图所示)类似于一个胶囊,胶囊内部封装了二氧化铈载体分散的双钯催化剂,胶囊的壳层具有高选择性、疏水性,可及时分离出产物乙醇。该反应器可使
 高效稳定地转化为乙醇,请分析可能原因:
高效稳定地转化为乙醇,请分析可能原因:
(3)在一恒压密闭容器中充入
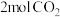 、
、 ,发生主反应I
,发生主反应I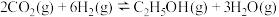 、副反应II
、副反应II 。已知初始压强为
。已知初始压强为 ,反应
,反应 时,测得
时,测得 下,总共生成
下,总共生成 水。甲醇与乙醇的选择性[如
水。甲醇与乙醇的选择性[如 的选择性
的选择性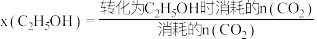 ]随温度和反应时间的变化关系如图。
]随温度和反应时间的变化关系如图。
①在
 下,当温度为
下,当温度为 时,乙醇的选择性能保持在近
时,乙醇的选择性能保持在近 的水平,但温度为
的水平,但温度为 和
和 时选择性大幅下降,其原因可能为
时选择性大幅下降,其原因可能为②
 下,
下, 内
内 的转化率为
的转化率为 。
。(4)酸性
 燃料电池的装置图如图所示,A极输入的物质为
燃料电池的装置图如图所示,A极输入的物质为 极的电极反应式为
极的电极反应式为
您最近半年使用:0次
2024-03-31更新
|
109次组卷
|
2卷引用:2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学
解题方法
7 . 已知4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确关系是
| A.4v(NH3)=5v(O2) | B.5v(O2)=6v(H2O) |
| C.2v(NH3)=3v(H2O) | D.4v(O2)=5v(NO) |
您最近半年使用:0次
2024-03-22更新
|
498次组卷
|
2卷引用:陕西省西安市蓝田县乡镇高中联考2023-2024学年高二上学期11月期中化学试题
解题方法
8 . 羰基硫( ,沸点:
,沸点: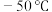 )又称氧硫化碳,其结构与
)又称氧硫化碳,其结构与 类似.回答下列问题:
类似.回答下列问题:
(1)实验室中通常用粉状硫氰化钾、水和浓硫酸反应制备 ,同时生成两种硫酸氢盐。写出该反应的化学方程式:
,同时生成两种硫酸氢盐。写出该反应的化学方程式:__________________________________ .
(2)以 为原料制备其他含硫物质的流程如下(部分产物已略去):
为原料制备其他含硫物质的流程如下(部分产物已略去):
 溶液
溶液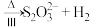
①反应Ⅰ中另一种产物是_____________ 。
②写出反应Ⅲ的离子方程式:_____________________________________________ 。
(3) 和
和 反应是制备
反应是制备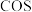 的另一种方法。恒温下,向体积为
的另一种方法。恒温下,向体积为 密闭容器中分别充入
密闭容器中分别充入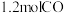 和
和 ,发生反应:
,发生反应: 后达到平衡状态,测得混合体系中含
后达到平衡状态,测得混合体系中含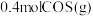 。
。
①平衡时, 的浓度为
的浓度为_____________  ;
; 内用
内用 表示的化学反应速率
表示的化学反应速率_____________  。
。
②下列描述中能说明上述反应已达平衡状态的是_____________ (填字母)。
a.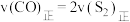
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器内气体压强保持不变
 ,沸点:
,沸点: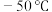 )又称氧硫化碳,其结构与
)又称氧硫化碳,其结构与 类似.回答下列问题:
类似.回答下列问题:(1)实验室中通常用粉状硫氰化钾、水和浓硫酸反应制备
 ,同时生成两种硫酸氢盐。写出该反应的化学方程式:
,同时生成两种硫酸氢盐。写出该反应的化学方程式:(2)以
 为原料制备其他含硫物质的流程如下(部分产物已略去):
为原料制备其他含硫物质的流程如下(部分产物已略去): 溶液
溶液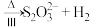
①反应Ⅰ中另一种产物是
②写出反应Ⅲ的离子方程式:
(3)
 和
和 反应是制备
反应是制备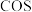 的另一种方法。恒温下,向体积为
的另一种方法。恒温下,向体积为 密闭容器中分别充入
密闭容器中分别充入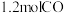 和
和 ,发生反应:
,发生反应: 后达到平衡状态,测得混合体系中含
后达到平衡状态,测得混合体系中含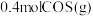 。
。①平衡时,
 的浓度为
的浓度为 ;
; 内用
内用 表示的化学反应速率
表示的化学反应速率 。
。②下列描述中能说明上述反应已达平衡状态的是
a.
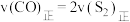
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器内气体压强保持不变
您最近半年使用:0次
解题方法
9 . 2022年北京冬奥会开幕式于2022年2月4日在国家体育场鸟巢隆重举行,其中奥运圣火的燃料为氢燃料,具有热值高、耐寒、环保无污染等优点。工业上可以通过催化重整二氧化碳和水蒸气制氢,主要有如下三个反应:
Ⅰ. ;
;
Ⅱ. ;
;
Ⅲ. 。
。
回答下列问题:
(1)反应
_____________ 。
(2)将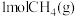 与
与 充入初始体积为
充入初始体积为 的恒压反应容器中,平衡时,各含碳物质的物质的量分数与温度之间的变化关系如图所示。
的恒压反应容器中,平衡时,各含碳物质的物质的量分数与温度之间的变化关系如图所示。

①曲线a代表的物质为_____________ (填化学式,下同);曲线c代表的物质为_____________ 。
② 至
至 ,曲线b代表物质的物质的量分数先随温度升高而增大的主要原因是
,曲线b代表物质的物质的量分数先随温度升高而增大的主要原因是___________________________________________________ 。
③ 时,反应进行
时,反应进行 后,甲烷的物质的量浓度为
后,甲烷的物质的量浓度为 内
内 表示的化学反应速率为
表示的化学反应速率为_____________  ;平衡时,容器中气体总物质的量为
;平衡时,容器中气体总物质的量为 ,容器体积为
,容器体积为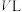 ,则反应Ⅰ的平衡常数
,则反应Ⅰ的平衡常数
_____________ (通过反应Ⅰ、Ⅱ计算即可,反应Ⅲ不影响计算结果,用含有n、V的代数式表示,不需要化简)。
Ⅰ.
 ;
;Ⅱ.
 ;
;Ⅲ.
 。
。回答下列问题:
(1)反应

(2)将
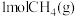 与
与 充入初始体积为
充入初始体积为 的恒压反应容器中,平衡时,各含碳物质的物质的量分数与温度之间的变化关系如图所示。
的恒压反应容器中,平衡时,各含碳物质的物质的量分数与温度之间的变化关系如图所示。
①曲线a代表的物质为
②
 至
至 ,曲线b代表物质的物质的量分数先随温度升高而增大的主要原因是
,曲线b代表物质的物质的量分数先随温度升高而增大的主要原因是③
 时,反应进行
时,反应进行 后,甲烷的物质的量浓度为
后,甲烷的物质的量浓度为 内
内 表示的化学反应速率为
表示的化学反应速率为 ;平衡时,容器中气体总物质的量为
;平衡时,容器中气体总物质的量为 ,容器体积为
,容器体积为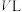 ,则反应Ⅰ的平衡常数
,则反应Ⅰ的平衡常数
您最近半年使用:0次
名校
10 . 在恒温的2L密闭容器中进行反应,气体X、Y,Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡。
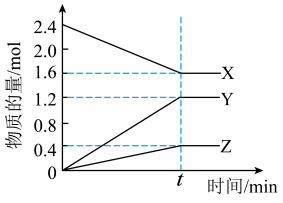
(1)上述反应_______ (填“是”或“不是”)可逆反应。
(2)该反应的化学方程式是_______ 。
(3)反应起始至t=2min时刻,Y的平均反应速率是_______ 。
(4)tmin后,体系内的压强与反应前的压强之比为:_______ 。

(1)上述反应
(2)该反应的化学方程式是
(3)反应起始至t=2min时刻,Y的平均反应速率是
(4)tmin后,体系内的压强与反应前的压强之比为:
您最近半年使用:0次