解题方法
1 . 人类利用二氧化碳合成淀粉对社会的发展起着重要作用,合成过程首先是利用二氧化碳制备甲醇,合成甲醇的反应为:CO2+3H2 CH3OH+H2O ∆H1。回答下列问题:
CH3OH+H2O ∆H1。回答下列问题:
(1)已知:①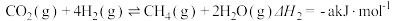
②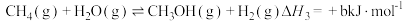
③ 均为大于零的数,且
均为大于零的数,且

___________  (用含
(用含 、
、 的式子表示)。甲醇熔融碳酸盐燃料电池的正极(含
的式子表示)。甲醇熔融碳酸盐燃料电池的正极(含 )电极反应式为
)电极反应式为___________ 。
(2)研究合成甲醇的催化剂时,在其他条件不变仅改变催化剂种类的情况下,对反应器出口产品进行成分分析,结果如图所示。在以上催化剂中,该反应的最佳催化剂为___________ (填化学式)。 的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。
的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。___________ 。
②结合上图及学过的知识推测,有水参与的历程,反应速率加快的原因是___________ 。
(4)在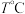 时,将
时,将 和
和 充入容积为
充入容积为 的恒容容器中,只发生
的恒容容器中,只发生 ,测得体系中剩余
,测得体系中剩余 的物质的量随时间变化如图中状态Ⅰ所示。
的物质的量随时间变化如图中状态Ⅰ所示。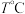 时,
时,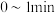 内甲醇的反应速率
内甲醇的反应速率
___________ 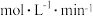 。
。
②该反应的平衡常数表达式为___________ 。
③保持投料量不变,仅改变某一个条件后,测得 随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是
随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是___________ 。
 CH3OH+H2O ∆H1。回答下列问题:
CH3OH+H2O ∆H1。回答下列问题:(1)已知:①
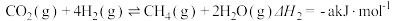
②
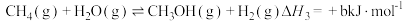
③
 均为大于零的数,且
均为大于零的数,且

 (用含
(用含 、
、 的式子表示)。甲醇熔融碳酸盐燃料电池的正极(含
的式子表示)。甲醇熔融碳酸盐燃料电池的正极(含 )电极反应式为
)电极反应式为(2)研究合成甲醇的催化剂时,在其他条件不变仅改变催化剂种类的情况下,对反应器出口产品进行成分分析,结果如图所示。在以上催化剂中,该反应的最佳催化剂为
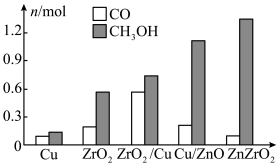
 的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。
的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。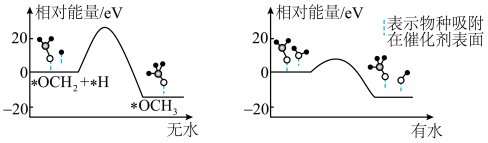
②结合上图及学过的知识推测,有水参与的历程,反应速率加快的原因是
(4)在
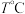 时,将
时,将 和
和 充入容积为
充入容积为 的恒容容器中,只发生
的恒容容器中,只发生 ,测得体系中剩余
,测得体系中剩余 的物质的量随时间变化如图中状态Ⅰ所示。
的物质的量随时间变化如图中状态Ⅰ所示。
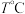 时,
时,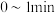 内甲醇的反应速率
内甲醇的反应速率
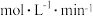 。
。②该反应的平衡常数表达式为
③保持投料量不变,仅改变某一个条件后,测得
 随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是
随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是
您最近半年使用:0次
解题方法
2 . 某温度时,在容积为2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答:___________ 。
(2)写出该反应的化学方程式___________ 。
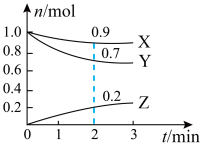
(2)写出该反应的化学方程式
您最近半年使用:0次
3 . 在温度不变、恒容的容器中进行反应:A(g) B(g)+C(g),若反应物的浓度由 0.1 mol/L 降低到 0.06mol/L 时,需20s;那么由 0.06 mol/L 降低到 0.036mol/L,所需反应时间应为
B(g)+C(g),若反应物的浓度由 0.1 mol/L 降低到 0.06mol/L 时,需20s;那么由 0.06 mol/L 降低到 0.036mol/L,所需反应时间应为
 B(g)+C(g),若反应物的浓度由 0.1 mol/L 降低到 0.06mol/L 时,需20s;那么由 0.06 mol/L 降低到 0.036mol/L,所需反应时间应为
B(g)+C(g),若反应物的浓度由 0.1 mol/L 降低到 0.06mol/L 时,需20s;那么由 0.06 mol/L 降低到 0.036mol/L,所需反应时间应为| A.等于l0s | B.等于12s | C.大于12s | D.小于12s |
您最近半年使用:0次
4 . 反应2SO2+O2 2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为
2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为
 2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为
2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为| A.0.1s | B.2.5s | C.5s | D.10s |
您最近半年使用:0次
5 . 在下列过程中,需要加快化学反应速率的是
| A.塑料老化 | B.炼钢 | C.钢铁生锈 | D.食物腐败 |
您最近半年使用:0次
6 . 氢能的开发和利用是推动我国能源结构转型,保障国家能源安全,实现“碳达峰”、“碳中和”目标的重要途径。目前,我国已成为世界第一大产氢国,主要有三类工业制氢路线:
(1)化工燃料重整制氢
已知:
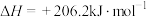

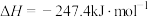
则 与
与 反应生成
反应生成 和
和 的反应热是
的反应热是___________  。
。
(2)工业副产氢
已知:工业上用水煤气法制氢气,有关化学方程式是:
反应一:

反应二:

①反应一在 时达到化学平衡状态,则此温度下该反应的平衡常数表达式
时达到化学平衡状态,则此温度下该反应的平衡常数表达式
___________ 。
②在 时将
时将 和
和 各
各 通入体积为
通入体积为 的密闭容器中反应发生反应二,
的密闭容器中反应发生反应二, 时达到平衡状态,该反应的平衡常数是9,则
时达到平衡状态,该反应的平衡常数是9,则 的转化率是
的转化率是___________ ,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率 是
是___________  。
。
(3)清洁能源电解制氢
已知:利用电解饱和食盐水可制得氢气,下图为电解装置示意图: 电极是极
电极是极___________ (填“阴”或“阳”), 电极的电极反应式
电极的电极反应式___________ 。
②假设室温条件下电解 饱和食盐水一段时间,当两极产生的气体共
饱和食盐水一段时间,当两极产生的气体共 (标准状况下)时,溶液的
(标准状况下)时,溶液的 为
为___________ (溶液体积没有变化)。
(1)化工燃料重整制氢
已知:

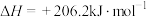

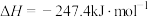
则
 与
与 反应生成
反应生成 和
和 的反应热是
的反应热是 。
。(2)工业副产氢
已知:工业上用水煤气法制氢气,有关化学方程式是:
反应一:


反应二:


①反应一在
 时达到化学平衡状态,则此温度下该反应的平衡常数表达式
时达到化学平衡状态,则此温度下该反应的平衡常数表达式
②在
 时将
时将 和
和 各
各 通入体积为
通入体积为 的密闭容器中反应发生反应二,
的密闭容器中反应发生反应二, 时达到平衡状态,该反应的平衡常数是9,则
时达到平衡状态,该反应的平衡常数是9,则 的转化率是
的转化率是 的浓度变化表示的反应速率
的浓度变化表示的反应速率 是
是 。
。(3)清洁能源电解制氢
已知:利用电解饱和食盐水可制得氢气,下图为电解装置示意图:

 电极是极
电极是极 电极的电极反应式
电极的电极反应式②假设室温条件下电解
 饱和食盐水一段时间,当两极产生的气体共
饱和食盐水一段时间,当两极产生的气体共 (标准状况下)时,溶液的
(标准状况下)时,溶液的 为
为
您最近半年使用:0次
7 . 体积均为1L的两个恒容密闭容器I、Ⅱ中,均充入2mol 和2mol
和2mol ,发生反应:
,发生反应:
 ,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是
,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是
 和2mol
和2mol ,发生反应:
,发生反应:
 ,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是
,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是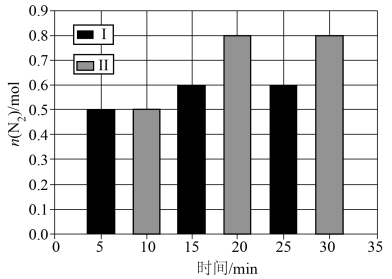
| A.容器I改变的条件可能是使用了催化剂 |
| B.相对容器Ⅱ,容器I改变的条件可能是加压或者升温 |
| C.容器Ⅱ中NO的平衡转化率为80% |
D.容器Ⅱ中0~10min内, |
您最近半年使用:0次
解题方法
8 . 某温度下,在一个 的密闭容器中,加入
的密闭容器中,加入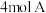 和
和 发生反应:
发生反应: ,反应
,反应 后达到平衡,测得生成
后达到平衡,测得生成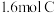 ,则下列说法正确的是
,则下列说法正确的是
 的密闭容器中,加入
的密闭容器中,加入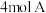 和
和 发生反应:
发生反应: ,反应
,反应 后达到平衡,测得生成
后达到平衡,测得生成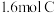 ,则下列说法正确的是
,则下列说法正确的是A.前 ,D的平均反应速率为 ,D的平均反应速率为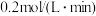 |
B.达到平衡时,B的平衡转化率是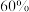 |
| C.升高该体系的温度,化学平衡常数不变 |
| D.增加C,逆向反应速率增大 |
您最近半年使用:0次
名校
解题方法
9 . 铁的化合物在工业中有重要价值。回答下列问题:
(1)复合氧化物铁酸锰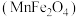 可用于热化学循环分解制氢气,原理如下:
可用于热化学循环分解制氢气,原理如下:
①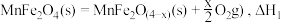
②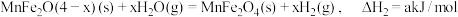
③
则 的燃烧热
的燃烧热
___________ 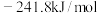 (填>、=或<),
(填>、=或<),
___________ (用含a的代数式表示)
(2)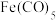 是一种重要的催化剂,制取反应为
是一种重要的催化剂,制取反应为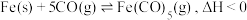 。在
。在 恒容密闭容器中加入足量铁粉和
恒容密闭容器中加入足量铁粉和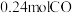 。
。
①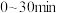 内在T温度下进行反应,测得
内在T温度下进行反应,测得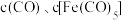 随时间的变化关系,以及
随时间的变化关系,以及 和
和 开始随条件的变化关系如图甲所示。
开始随条件的变化关系如图甲所示。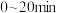 内用
内用 表示的平均反应速率为
表示的平均反应速率为___________  ;则此温度下的
;则此温度下的
___________ (写出计算式即可)。
②曲线I代表___________ [填 或
或 ]浓度的变化,
]浓度的变化, 时改变的条件是
时改变的条件是___________ 。 后曲线Ⅱ下降的原因是
后曲线Ⅱ下降的原因是___________ 。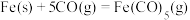 达到平衡状态的是
达到平衡状态的是___________ 。
A.密度保持不变 B. 体积分数保持不变
体积分数保持不变
C.平均摩尔质量保持不变 D.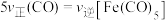
(1)复合氧化物铁酸锰
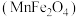 可用于热化学循环分解制氢气,原理如下:
可用于热化学循环分解制氢气,原理如下:①
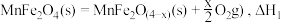
②
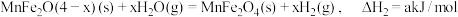
③

则
 的燃烧热
的燃烧热
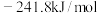 (填>、=或<),
(填>、=或<),
(2)
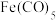 是一种重要的催化剂,制取反应为
是一种重要的催化剂,制取反应为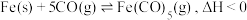 。在
。在 恒容密闭容器中加入足量铁粉和
恒容密闭容器中加入足量铁粉和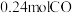 。
。①
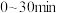 内在T温度下进行反应,测得
内在T温度下进行反应,测得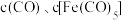 随时间的变化关系,以及
随时间的变化关系,以及 和
和 开始随条件的变化关系如图甲所示。
开始随条件的变化关系如图甲所示。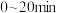 内用
内用 表示的平均反应速率为
表示的平均反应速率为 ;则此温度下的
;则此温度下的
②曲线I代表
 或
或 ]浓度的变化,
]浓度的变化, 时改变的条件是
时改变的条件是 后曲线Ⅱ下降的原因是
后曲线Ⅱ下降的原因是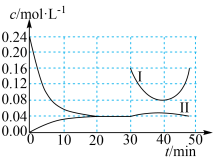
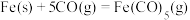 达到平衡状态的是
达到平衡状态的是A.密度保持不变 B.
 体积分数保持不变
体积分数保持不变C.平均摩尔质量保持不变 D.
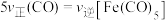
您最近半年使用:0次
名校
解题方法
10 . I、一定温度时,在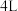 密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:
密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:________________ , 时刻M的转化率为
时刻M的转化率为________________ 。
(2)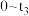 时间内用M表示的化学反应速率为
时间内用M表示的化学反应速率为________  /(
/(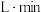 ).
).
(3)下列能表示上述反应达到化学平衡状态的是________(填编号)。
Ⅱ、一定条件下,在容积为 的密闭容器中发生反应:
的密闭容器中发生反应: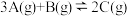 。开始时加入
。开始时加入 、
、 、
、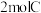 ,在
,在 末测得C的物质的量是
末测得C的物质的量是 。
。
(4)用B的浓度变化表示反应的平均速率:________________ 。
(5)在 末,A的浓度为
末,A的浓度为________________ 。
(6)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①充入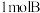 ,化学反应速率
,化学反应速率________________ ;
②将容器的容积变为 ,化学反应速率
,化学反应速率________________ ;
③升高温度,化学反应速率________________ 。
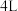 密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:
密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示: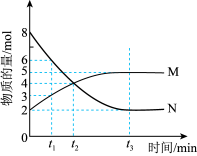
 时刻M的转化率为
时刻M的转化率为(2)
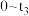 时间内用M表示的化学反应速率为
时间内用M表示的化学反应速率为 /(
/(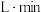 ).
).(3)下列能表示上述反应达到化学平衡状态的是________(填编号)。
A. | B.M与N的物质的量之比保持不变 |
| C.容器中压强保持不变 | D.混合气体密度保持不变 |
Ⅱ、一定条件下,在容积为
 的密闭容器中发生反应:
的密闭容器中发生反应: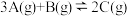 。开始时加入
。开始时加入 、
、 、
、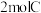 ,在
,在 末测得C的物质的量是
末测得C的物质的量是 。
。(4)用B的浓度变化表示反应的平均速率:
(5)在
 末,A的浓度为
末,A的浓度为(6)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①充入
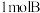 ,化学反应速率
,化学反应速率②将容器的容积变为
 ,化学反应速率
,化学反应速率③升高温度,化学反应速率
您最近半年使用:0次



