解题方法
1 . 乙醇因其含氢量高、毒性低、价格低廉且来源广泛,成为理想的液态储氢载体之一。乙醇―水催化重整可获得 ,其主要反应为:
,其主要反应为:
Ⅰ.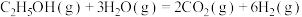

Ⅱ.

回答下列问题:
(1)已知:298K时,相关物质的相对能量如下表:
则a=___________ 。
(2)在恒温恒容条件下,投入1mol 和3mol
和3mol 发生反应
发生反应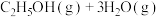
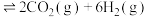 ,下列情况表明该反应达到平衡状态的是___________(填标号)。
,下列情况表明该反应达到平衡状态的是___________(填标号)。
(3)科学家研究了Grubbs催化剂作用于乙醇水溶液重整产氢的反应,测得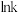 (k为速率常数)与反应温度倒数(
(k为速率常数)与反应温度倒数( )的相关关系及线性拟合如图1所示。请分析该反应的k随反应温度T的变化关系:
)的相关关系及线性拟合如图1所示。请分析该反应的k随反应温度T的变化关系:___________ 。 下,
下,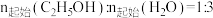 时,若仅考虑以上反应Ⅰ和Ⅱ,平衡时
时,若仅考虑以上反应Ⅰ和Ⅱ,平衡时 和CO的选择性及
和CO的选择性及 的产率随温度的变化如图2所示。
的产率随温度的变化如图2所示。 的选择性
的选择性
①图中表示 产率随温度变化的曲线是
产率随温度变化的曲线是___________ (填字母),判断依据是___________ 。
②一定温度下,加入 可以提高平衡时
可以提高平衡时 的产率,其原因是
的产率,其原因是___________ 。
(5)向一容积为2L的恒容密闭容器中通入2mol 和6mol
和6mol ,一定温度下发生反应
,一定温度下发生反应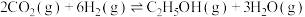 。若起始时气体的总压为p Pa,20min时达到平衡状态,测得
。若起始时气体的总压为p Pa,20min时达到平衡状态,测得 的物质的量分数为12.5%。
的物质的量分数为12.5%。
①平衡时气体的总压为___________ Pa(用含p的分数表示,需化简)。
②0~20min内,用 浓度的变化表示的平均反应速率
浓度的变化表示的平均反应速率
___________ ;该温度下,上述反应的平衡常数
___________ 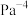 (用含p的分数表示,需化简;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用含p的分数表示,需化简;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 ,其主要反应为:
,其主要反应为:Ⅰ.
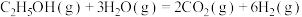

Ⅱ.


回答下列问题:
(1)已知:298K时,相关物质的相对能量如下表:
| 物质 |  |  |  |  |  |
相对能量/( ) ) | ―242 | ―393 | 0 | ―110 | a |
(2)在恒温恒容条件下,投入1mol
 和3mol
和3mol 发生反应
发生反应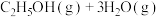
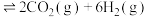 ,下列情况表明该反应达到平衡状态的是___________(填标号)。
,下列情况表明该反应达到平衡状态的是___________(填标号)。| A.混合气体的密度保持不变 | B.混合气体的总压强保持不变 |
| C.混合气体的平均摩尔质量保持不变 | D.产物的浓度之比保持不变 |
(3)科学家研究了Grubbs催化剂作用于乙醇水溶液重整产氢的反应,测得
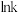 (k为速率常数)与反应温度倒数(
(k为速率常数)与反应温度倒数( )的相关关系及线性拟合如图1所示。请分析该反应的k随反应温度T的变化关系:
)的相关关系及线性拟合如图1所示。请分析该反应的k随反应温度T的变化关系: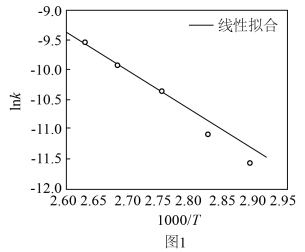
 下,
下,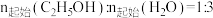 时,若仅考虑以上反应Ⅰ和Ⅱ,平衡时
时,若仅考虑以上反应Ⅰ和Ⅱ,平衡时 和CO的选择性及
和CO的选择性及 的产率随温度的变化如图2所示。
的产率随温度的变化如图2所示。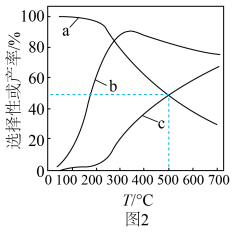
 的选择性
的选择性
①图中表示
 产率随温度变化的曲线是
产率随温度变化的曲线是②一定温度下,加入
 可以提高平衡时
可以提高平衡时 的产率,其原因是
的产率,其原因是(5)向一容积为2L的恒容密闭容器中通入2mol
 和6mol
和6mol ,一定温度下发生反应
,一定温度下发生反应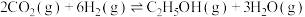 。若起始时气体的总压为p Pa,20min时达到平衡状态,测得
。若起始时气体的总压为p Pa,20min时达到平衡状态,测得 的物质的量分数为12.5%。
的物质的量分数为12.5%。①平衡时气体的总压为
②0~20min内,用
 浓度的变化表示的平均反应速率
浓度的变化表示的平均反应速率

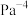 (用含p的分数表示,需化简;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用含p的分数表示,需化简;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
您最近半年使用:0次
2 . CO是一种重要化工原料,也是一种燃料.工业上,合成 的原理为
的原理为 (正反应是放热反应).向1L恒容密闭容器中充人
(正反应是放热反应).向1L恒容密闭容器中充人 和
和 ,发生上述反应.测得CO浓度随时间,温度变化如图所示.
,发生上述反应.测得CO浓度随时间,温度变化如图所示.
(1)温度
_______  (填“>” “<”或 “=”),判断依据是
(填“>” “<”或 “=”),判断依据是___________ .
(2)下列叙述能说明该反应达到平衡状态的是________(填字母).
(3)a点:正反应速率逆反应速率__________ (填“>” “<”或 “=”,下同),逆反应速率:a_____ b.
(4) 温度下,2~6min内
温度下,2~6min内 的平均反应速率为
的平均反应速率为__________  .
.
(5) 温度下,CO平衡转化率为
温度下,CO平衡转化率为______________ .
(6)CO空气碱性燃料电池放电效率高,写出负极的电极反应式:_____________ .
 的原理为
的原理为 (正反应是放热反应).向1L恒容密闭容器中充人
(正反应是放热反应).向1L恒容密闭容器中充人 和
和 ,发生上述反应.测得CO浓度随时间,温度变化如图所示.
,发生上述反应.测得CO浓度随时间,温度变化如图所示.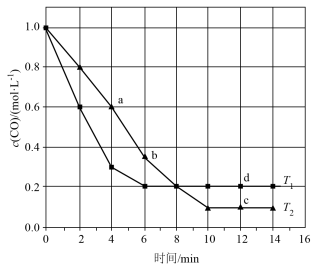
(1)温度

 (填“>” “<”或 “=”),判断依据是
(填“>” “<”或 “=”),判断依据是(2)下列叙述能说明该反应达到平衡状态的是________(填字母).
| A.混合气体密度不随时间变化 |
| B.气体总压强不随时间变化 |
C. 体积分数不随时间变化 体积分数不随时间变化 |
D.CO消耗速率等于 生成速率 生成速率 |
(3)a点:正反应速率逆反应速率
(4)
 温度下,2~6min内
温度下,2~6min内 的平均反应速率为
的平均反应速率为 .
.(5)
 温度下,CO平衡转化率为
温度下,CO平衡转化率为(6)CO空气碱性燃料电池放电效率高,写出负极的电极反应式:
您最近半年使用:0次
3 . T℃时,在2L的密闭容器中, (均为气体)的物质的量随时间的变化曲线如图所示,下列说法错误的是
(均为气体)的物质的量随时间的变化曲线如图所示,下列说法错误的是
 (均为气体)的物质的量随时间的变化曲线如图所示,下列说法错误的是
(均为气体)的物质的量随时间的变化曲线如图所示,下列说法错误的是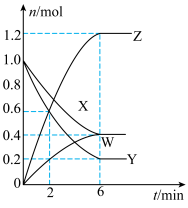
A.反应的化学方程式为 |
| B.适当升高温度,正反应速率和逆反应速率均增大 |
| C.初始时的压强与平衡时的压强比为10:11 |
D.若该反应在绝热容器中进行,也在 时达到平衡 时达到平衡 |
您最近半年使用:0次
解题方法
4 . 将1mol  充入10L恒容密闭容器中,在一定温度下发生反应:①
充入10L恒容密闭容器中,在一定温度下发生反应:①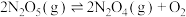

 ;②
;②
 。10min末,该反应达到平衡,此时
。10min末,该反应达到平衡,此时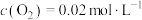 ,
, ,下列说法错误的是
,下列说法错误的是
 充入10L恒容密闭容器中,在一定温度下发生反应:①
充入10L恒容密闭容器中,在一定温度下发生反应:①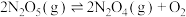

 ;②
;②
 。10min末,该反应达到平衡,此时
。10min末,该反应达到平衡,此时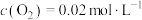 ,
, ,下列说法错误的是
,下列说法错误的是A.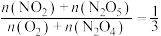 |
B.0~10min, |
C.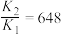 |
D.反应达到平衡后,保持其他条件不变,仅充入少量氦气,则 的反应速率保持不变 的反应速率保持不变 |
您最近半年使用:0次
5 . 研究 、
、 在一定条件下与
在一定条件下与 催化合成
催化合成 等有机化工产品,对落实“双碳目标”具有重要的意义。在一定条件下
等有机化工产品,对落实“双碳目标”具有重要的意义。在一定条件下 、
、 与
与 可发生如下反应:
可发生如下反应:
反应I: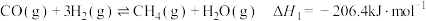
反应II: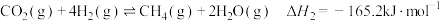
反应III: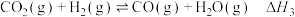
回答下列问题:
(1)反应II自发的条件是_______ (填“高温自发”、“低温自发”或“任何温度下都自发”),反应III正、逆反应的活化能分别为 、
、 ,则
,则
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(2)某温度下,向一刚性容器中加入等物质的量 和
和 ,发生反应III,测得
,发生反应III,测得 和
和 物质的量浓度随时间的变化如图所示。
物质的量浓度随时间的变化如图所示。
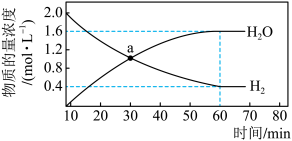
①下列说法正确的是_______ 。
a.a点时
b.60min内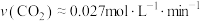
c.相同条件下,减小CO浓度, 增大
增大
d.平衡后,向容器中继续加入 和
和 ,重新达到平衡,
,重新达到平衡, 转化率不变
转化率不变
②已知 ,其中
,其中 、
、 分别为正、逆反应速率常数。a点时,
分别为正、逆反应速率常数。a点时,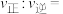
_______ 。
③70min时,升高温度, 转化率
转化率_______ (填“增大”、“减小”或“不变”),原因是_______ 。
(3)在密闭反应器中通入 和
和 ,分别在1MPa和5MPa下进行反应II和反应III。其
,分别在1MPa和5MPa下进行反应II和反应III。其 和
和 在含碳物质中的平衡组成(如
在含碳物质中的平衡组成(如 的平衡组成为
的平衡组成为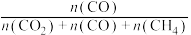 )受温度的影响如图所示:
)受温度的影响如图所示:
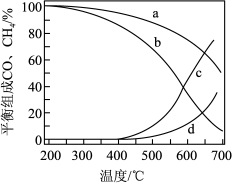
①5MPa时,表示 和
和 平衡组成的曲线分别是
平衡组成的曲线分别是_______ 、_______ (填“a”、“b”、“c”或“d”)。
②当 和
和 平衡组成均为30%时,
平衡组成均为30%时, 的平衡转化率为
的平衡转化率为_______ ,该温度下反应III的平衡常数 为
为_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 、
、 在一定条件下与
在一定条件下与 催化合成
催化合成 等有机化工产品,对落实“双碳目标”具有重要的意义。在一定条件下
等有机化工产品,对落实“双碳目标”具有重要的意义。在一定条件下 、
、 与
与 可发生如下反应:
可发生如下反应:反应I:
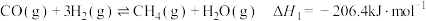
反应II:
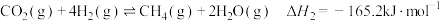
反应III:
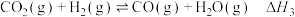
回答下列问题:
(1)反应II自发的条件是
 、
、 ,则
,则
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(2)某温度下,向一刚性容器中加入等物质的量
 和
和 ,发生反应III,测得
,发生反应III,测得 和
和 物质的量浓度随时间的变化如图所示。
物质的量浓度随时间的变化如图所示。
①下列说法正确的是
a.a点时

b.60min内
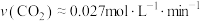
c.相同条件下,减小CO浓度,
 增大
增大d.平衡后,向容器中继续加入
 和
和 ,重新达到平衡,
,重新达到平衡, 转化率不变
转化率不变②已知
 ,其中
,其中 、
、 分别为正、逆反应速率常数。a点时,
分别为正、逆反应速率常数。a点时,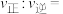
③70min时,升高温度,
 转化率
转化率(3)在密闭反应器中通入
 和
和 ,分别在1MPa和5MPa下进行反应II和反应III。其
,分别在1MPa和5MPa下进行反应II和反应III。其 和
和 在含碳物质中的平衡组成(如
在含碳物质中的平衡组成(如 的平衡组成为
的平衡组成为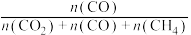 )受温度的影响如图所示:
)受温度的影响如图所示:
①5MPa时,表示
 和
和 平衡组成的曲线分别是
平衡组成的曲线分别是②当
 和
和 平衡组成均为30%时,
平衡组成均为30%时, 的平衡转化率为
的平衡转化率为 为
为
您最近半年使用:0次
6 . 乙烯可用于制备乙醇: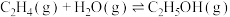 △H<0。向10L某恒容密闭容器中通入2mol
△H<0。向10L某恒容密闭容器中通入2mol (g)和a mol
(g)和a mol  (g),发生上述反应,测得
(g),发生上述反应,测得 (g)的平衡转化率与投料比X[
(g)的平衡转化率与投料比X[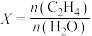 ]以及温度的关系如图所示。回答下列问题:
]以及温度的关系如图所示。回答下列问题:
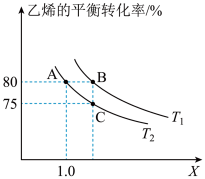
(1)反应从开始分别进行到A、B、C点时,放出的热量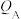 、
、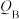 、
、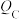 由大到小的顺序为
由大到小的顺序为___________ 。
(2)
___________ (填“>”“<”或“=”) 。已知该反应的反应速率表达式为
。已知该反应的反应速率表达式为 ,
,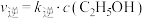 ,其中
,其中 、
、 为速率常数,只与温度有关。若其他条件不变,则温度从
为速率常数,只与温度有关。若其他条件不变,则温度从 变化到
变化到 的过程中,下列推断合理的是
的过程中,下列推断合理的是___________ (填字母)。
A. 减小的倍数大于
减小的倍数大于 B.
B. 减小的倍数小于
减小的倍数小于
C. 增大的倍数大于
增大的倍数大于 D.
D. 增大的倍数小于
增大的倍数小于
(3)若A点对应的体系中,反应从开始到达到平衡所用时间是2min,则0~2min内 (g)的平均反应速率
(g)的平均反应速率
___________  。
。 温度下,反应的平衡常数K=
温度下,反应的平衡常数K=___________ 。
(4)B点对应的体系中,a=___________ ;A、B、C点对应体系的气体总压强 、
、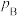 、
、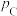 由大到小的顺序为
由大到小的顺序为___________ (气体均看作理想气体)。
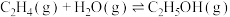 △H<0。向10L某恒容密闭容器中通入2mol
△H<0。向10L某恒容密闭容器中通入2mol (g)和a mol
(g)和a mol  (g),发生上述反应,测得
(g),发生上述反应,测得 (g)的平衡转化率与投料比X[
(g)的平衡转化率与投料比X[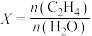 ]以及温度的关系如图所示。回答下列问题:
]以及温度的关系如图所示。回答下列问题:
(1)反应从开始分别进行到A、B、C点时,放出的热量
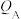 、
、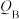 、
、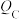 由大到小的顺序为
由大到小的顺序为(2)

 。已知该反应的反应速率表达式为
。已知该反应的反应速率表达式为 ,
,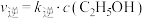 ,其中
,其中 、
、 为速率常数,只与温度有关。若其他条件不变,则温度从
为速率常数,只与温度有关。若其他条件不变,则温度从 变化到
变化到 的过程中,下列推断合理的是
的过程中,下列推断合理的是A.
 减小的倍数大于
减小的倍数大于 B.
B. 减小的倍数小于
减小的倍数小于
C.
 增大的倍数大于
增大的倍数大于 D.
D. 增大的倍数小于
增大的倍数小于
(3)若A点对应的体系中,反应从开始到达到平衡所用时间是2min,则0~2min内
 (g)的平均反应速率
(g)的平均反应速率
 。
。 温度下,反应的平衡常数K=
温度下,反应的平衡常数K=(4)B点对应的体系中,a=
 、
、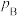 、
、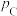 由大到小的顺序为
由大到小的顺序为
您最近半年使用:0次
7 . 下列实验装置或设计能完成相应实验的是
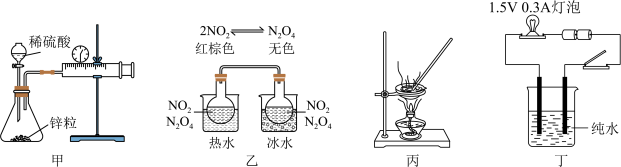

A.装置甲测定 表示的反应速率(单位: 表示的反应速率(单位: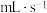 ) ) |
B.装置乙验证 正反应是放热反应 正反应是放热反应 |
C.装置丙在空气中蒸发 溶液得到 溶液得到 |
| D.装置丁验证纯水具有微弱的导电性 |
您最近半年使用:0次
名校
解题方法
8 . 已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
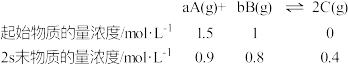
请回答下列问题。
(1)该可逆反应的化学方程式可表示为_______ 。
(2)用物质B来表示0~2s的平均反应速率为_______ 。
(3)从反应开始到2s末,A的转化率为_______ 。
(4)下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是_______ (填序号)。
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(5)若平衡后改变温度,使得容器中气体的平均摩尔质量变大,则反应向_______ (填“反应物”或“生成物”)的方向移动。
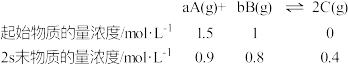
请回答下列问题。
(1)该可逆反应的化学方程式可表示为
(2)用物质B来表示0~2s的平均反应速率为
(3)从反应开始到2s末,A的转化率为
(4)下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(5)若平衡后改变温度,使得容器中气体的平均摩尔质量变大,则反应向
您最近半年使用:0次
解题方法
9 . 在容积为2L的密闭容器中发生反应: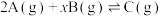 。图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示温度100℃和200℃平衡时C的体积分数随起始
。图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示温度100℃和200℃平衡时C的体积分数随起始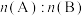 的变化关系,下列说法正确的是
的变化关系,下列说法正确的是

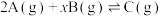 。图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示温度100℃和200℃平衡时C的体积分数随起始
。图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示温度100℃和200℃平衡时C的体积分数随起始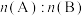 的变化关系,下列说法正确的是
的变化关系,下列说法正确的是
A.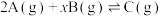 中, 中, |
B.200℃,反应从开始到平衡的平均速率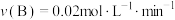 |
C.由图乙可知,反应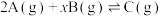 的 的 ,且 ,且 |
| D.当外界条件由200℃降温到100℃,原平衡一定被破坏,且正、逆反应速率均增大 |
您最近半年使用:0次
10 . 一定温度下, 溶液发生催化分解。不同时刻测得生成的
溶液发生催化分解。不同时刻测得生成的 的体积(已折算为标准状况下)如表。
的体积(已折算为标准状况下)如表。
下列叙述正确的是(溶液体积变化忽略不计)
 溶液发生催化分解。不同时刻测得生成的
溶液发生催化分解。不同时刻测得生成的 的体积(已折算为标准状况下)如表。
的体积(已折算为标准状况下)如表。| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
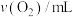 | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
A. 或 或 可以催化 可以催化 分解 分解 |
| B.第4min时的瞬时速率小于第6min时的瞬时速率 |
C.反应至6min时, 分解率为50% 分解率为50% |
D.0~6min的平均反应速率: |
您最近半年使用:0次



