1 . 工业上合成氮气: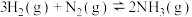 ,其原料之一的氢气可通过如下反应得到:
,其原料之一的氢气可通过如下反应得到: ,1mol甲烷和1mol水蒸气的总能量小于1mol一氧化碳和3mol氢气的总能量。
,1mol甲烷和1mol水蒸气的总能量小于1mol一氧化碳和3mol氢气的总能量。
(1)下列表示合成氨反应的速率中,反应最快的是 。
(2)在一个恒温恒容的密闭容器中进行合成氨反应,下列证据能判断反应已达平衡状态的是 。
(3)已知断开 键需吸热
键需吸热 ,断开
,断开 键需吸热
键需吸热 ,断开
,断开 键需吸热
键需吸热 。则氮气与氢气反应,每生成
。则氮气与氢气反应,每生成 需要 。
需要 。
(4)在一个密闭容器中进行的合成氨反应,达到平衡后改变一个条件,一段时间又达到平衡,此时测得氨气的浓度增大。下列可能的原因是 。
(5)在 体积不变的密闭容器中进行反应
体积不变的密闭容器中进行反应 ,测得
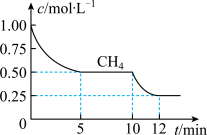
,测得 的物质的量浓度随反应时间的变化如图所示,反应进行到
的物质的量浓度随反应时间的变化如图所示,反应进行到 时,生成的
时,生成的 的物质的量为
的物质的量为_________ ,以 表示的平均反应速率为
表示的平均反应速率为__________ 。此时,若再加入 ,则化学平衡将向
,则化学平衡将向___________ 反应方向移动,过程中正反应速率的变化为_______________ 。
(6)如图所示,上述反应进行到10min时,改变外界条件导致如图所示的变化,则所改变的条件可能是_________________ 。
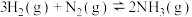 ,其原料之一的氢气可通过如下反应得到:
,其原料之一的氢气可通过如下反应得到: ,1mol甲烷和1mol水蒸气的总能量小于1mol一氧化碳和3mol氢气的总能量。
,1mol甲烷和1mol水蒸气的总能量小于1mol一氧化碳和3mol氢气的总能量。(1)下列表示合成氨反应的速率中,反应最快的是 。
A.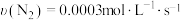 | B. |
C.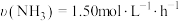 | D. |
A. | B.气体密度不再变化 |
C.每消耗 就同时消耗 就同时消耗 | D.混合气体的平均摩尔质量不再变化 |
 键需吸热
键需吸热 ,断开
,断开 键需吸热
键需吸热 ,断开
,断开 键需吸热
键需吸热 。则氮气与氢气反应,每生成
。则氮气与氢气反应,每生成 需要 。
需要 。A.吸热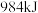 | B.吸热 | C.放热 | D.放热 |
| A.升高温度 | B.降低温度 | C.增大容器体积 | D.缩小容器体积 |
 体积不变的密闭容器中进行反应
体积不变的密闭容器中进行反应 ,测得
,测得 的物质的量浓度随反应时间的变化如图所示,反应进行到
的物质的量浓度随反应时间的变化如图所示,反应进行到 时,生成的
时,生成的 的物质的量为
的物质的量为 表示的平均反应速率为
表示的平均反应速率为 ,则化学平衡将向
,则化学平衡将向(6)如图所示,上述反应进行到10min时,改变外界条件导致如图所示的变化,则所改变的条件可能是

您最近一年使用:0次
2023-04-27更新
|
367次组卷
|
2卷引用:山西省大同市第一中学校2023-2024学年高二上学期9月月考化学试题
名校
解题方法
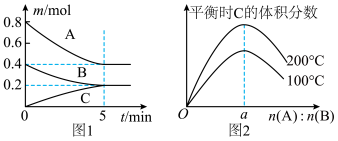
2 . 在体积为 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应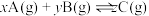 ,图1表示
,图1表示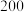 ℃时容器中
℃时容器中 、
、 、
、 物质的量随时间的变化关系,图2表示不同温度下平衡时
物质的量随时间的变化关系,图2表示不同温度下平衡时 的体积分数随起始
的体积分数随起始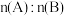 的变化关系。则下列结论正确的是
的变化关系。则下列结论正确的是
 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应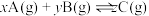 ,图1表示
,图1表示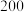 ℃时容器中
℃时容器中 、
、 、
、 物质的量随时间的变化关系,图2表示不同温度下平衡时
物质的量随时间的变化关系,图2表示不同温度下平衡时 的体积分数随起始
的体积分数随起始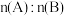 的变化关系。则下列结论正确的是
的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率 |
B.由图2可知反应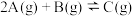 ,正反应吸热且a=2 ,正反应吸热且a=2 |
C.若在图1所示的平衡状态下再向体系中充入 和 和 ,此时 ,此时 |
D.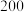 ℃时,向空容器中充入 ℃时,向空容器中充入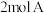 和 和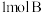 ,达到平衡时 ,达到平衡时 的体积分数小于0.5 的体积分数小于0.5 |
您最近一年使用:0次
2023-04-27更新
|
327次组卷
|
7卷引用:山西省实验中学2023-2024学年高二上学期第一次月考化学试题
山西省实验中学2023-2024学年高二上学期第一次月考化学试题上海市实验学校2021-2022学年高三下学期3月月考化学试题(已下线)卷11 化学反应速率和平衡选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省常德市澧县一中2021-2022学年高三下学期期中考试化学试题湖南省常德市澧县第一中学2021-2022学年高三下学期期中考试化学试题上海市建平中学2023届高三下学期3月月考化学试题湖南省衡阳县2023届高三3月教学质量诊断性检测考试化学试题
名校
3 . 下列关于化学反应速率的说法正确的是
| A.化学反应速率可以衡量化学反应进行的快慢 |
B.化学反应速率为0.2 ,是指反应经过1min后,反应物的浓度是0.2 ,是指反应经过1min后,反应物的浓度是0.2 |
| C.对于任何化学反应来说,反应现象越明显,说明其化学反应速率越快 |
| D.化学反应速率是指在一段时间内反应物物质的量的减少或生成物物质的量的增加量 |
您最近一年使用:0次
2023-04-27更新
|
210次组卷
|
4卷引用:山西省怀仁市第一中学校2022-2023学年高一下学期第二次月考(期中)化学试题
名校
解题方法
4 . 对于可逆反应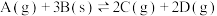 ,在不同条件下的化学反应速率如下,其中表示应速率最快的是
,在不同条件下的化学反应速率如下,其中表示应速率最快的是
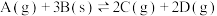 ,在不同条件下的化学反应速率如下,其中表示应速率最快的是
,在不同条件下的化学反应速率如下,其中表示应速率最快的是A. | B.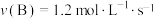 |
C. | D. |
您最近一年使用:0次
2023-04-26更新
|
683次组卷
|
37卷引用:山西省长治市第二中学校2021-2022学年高一下学期期中考试化学试题
山西省长治市第二中学校2021-2022学年高一下学期期中考试化学试题2016-2017学年黑龙江省双鸭山一中高二上9月月考化学卷黑龙江省双鸭山市第一中学2017-2018学年高二9月月考化学试题2019年秋高三化学复习强化练习—— 化学反应速率及化学平衡北京市通州区2019-2020学年高二下学期期末考试化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第3节 化学反应的速率福建省福州市罗源第一中学2020-2021学年高二上学期10月月考化学试题陕西省西安市第一中学2020-2021学年高二上学期第一次月考化学试题甘肃省民勤县第一中学2020-2021学年高二上学期第二次月考化学(理) 试题河北省保定市高碑店市高碑店一中2019---2020学年高一下学期第二次月考化学试题福建省福州市福建师范大学附属中学2020-2021学年高二上学期期中考试化学试题贵州省安顺市大洋实验学校2020-2021学年高二上学期期中考试化学试题(已下线)6.2.1 化学反应速率(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)吉林市第五十五中学2020-2021学年高二上学期期末考试化学试题河北省衡水市第十四中学2020-2021学年高一下学期一调考试化学试题江西省赣州市南康区第三中学2020-2021学年高一下学期期中考试化学试题河北省邯郸市2020-2021学年高一下学期期末考试化学试题(已下线)考点17 化学反应速率及其影响因素-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点17 化学反应速率及其影响因素-备战2022年高考化学一轮复习考点帮(浙江专用)河北省衡水市第十四中学2020-2021学年高一下学期期末考试化学试题重庆市暨华中学校2021-2022学年高二上学期第一次月考化学试题浙江省温州市瑞安市上海新纪元高级中学2021-2022学年高一9月份月考(5-6班)化学试题天津市武清区崔黄口中学2021-2022学年高二上学期第一次练习化学试题安徽省芜湖市第一中学2021-2022学年高二上学期第一次月末诊断测试化学试题河南省中原名校联盟2021-2022学年高二上学期第三次适应性联考化学试题(已下线)6.1.1 化学反应速率(第1课时 化学反应速率的概念和简单计算)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)河北省唐县第一中学2021-2022学年高一下学期期中考试化学试题(已下线)考点21 化学反应速率-备战2023年高考化学一轮复习考点帮(全国通用)江西省宜春市万载中学2021-2022学年高一下学期4月月考化学试卷(已下线)第20讲 化学反应速率(讲)-2023年高考化学一轮复习讲练测(全国通用)北京市顺义区顺义第一中学2022-2023学年高二上学期期中考试化学试题内蒙古自治区呼伦贝尔市鄂温克族自治旗第三中学2021-2022学年高二上学期第一次月考化学试题河北省唐山市迁西县职业技术教育中心2021-2022学年高二(普职融通部)上学期期中考试化学试题(已下线)6.2.1 化学反应速率及影响因素——同步学习必备知识江苏省涟水县第一中学2022-2023学年高一下学期第一次月考化学试卷福建省三明市五县联合质检2022-2023学年高一下学期期中考试化学试题江西省赣州市兴国县联考2022-2023学年高一下学期5月月考化学试题
名校
5 . 已知
 ,回答下列问题:
,回答下列问题:
(1)在100℃时,将 气体充入
气体充入 的密闭容器中,隔一段时间对容器内的物质进行分析得到如下数据:
的密闭容器中,隔一段时间对容器内的物质进行分析得到如下数据:
①表中
___________ (填“>”“<”或“=”,下同) ;a
;a___________ b。
② 时
时 的浓度
的浓度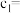
___________ ,在 内
内 的平均反应速率为
的平均反应速率为___________  。
。
(2)一定温度下,体积为 的恒容密闭容器中,各物质的物质的量随时间变化的关系如图所示。
的恒容密闭容器中,各物质的物质的量随时间变化的关系如图所示。

①若上述反应在甲、乙两个相同容器内同时进行,分别测得:甲中 ,乙中
,乙中 ,则
,则___________ 中反应更快。
② 。该反应达最大限度时Y的转化率为
。该反应达最大限度时Y的转化率为___________ ;若初始压强为 ,则平衡时
,则平衡时
___________ (用含 的表达式表示)。
的表达式表示)。
③下列描述能表示该反应达平衡状态的是___________ (填标号)。
A.容器内气体的密度不再发生变化 B.混合气体总的物质的量不再发生变化
C.容器内气体的颜色不再改变 D.容器中X与Y的物质的量相等
E.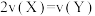 F.容器内气体的平均相对分子质量不再改变
F.容器内气体的平均相对分子质量不再改变

 ,回答下列问题:
,回答下列问题:(1)在100℃时,将
 气体充入
气体充入 的密闭容器中,隔一段时间对容器内的物质进行分析得到如下数据:
的密闭容器中,隔一段时间对容器内的物质进行分析得到如下数据:| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
 | 0.100 |  | 0.050 |  | a | b |
 | 0.000 | 0.060 |  | 0.120 | 0.120 | 0.120 |

 ;a
;a②
 时
时 的浓度
的浓度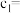
 内
内 的平均反应速率为
的平均反应速率为 。
。(2)一定温度下,体积为
 的恒容密闭容器中,各物质的物质的量随时间变化的关系如图所示。
的恒容密闭容器中,各物质的物质的量随时间变化的关系如图所示。
①若上述反应在甲、乙两个相同容器内同时进行,分别测得:甲中
 ,乙中
,乙中 ,则
,则②
 。该反应达最大限度时Y的转化率为
。该反应达最大限度时Y的转化率为 ,则平衡时
,则平衡时
 的表达式表示)。
的表达式表示)。③下列描述能表示该反应达平衡状态的是
A.容器内气体的密度不再发生变化 B.混合气体总的物质的量不再发生变化
C.容器内气体的颜色不再改变 D.容器中X与Y的物质的量相等
E.
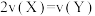 F.容器内气体的平均相对分子质量不再改变
F.容器内气体的平均相对分子质量不再改变
您最近一年使用:0次
2023-04-25更新
|
314次组卷
|
2卷引用:山西省大同市第一中学校2023-2024学年高二上学期10月月考化学试题
名校
6 . 回答下列问题:
(1)将一定量纯净的氨基甲酸铵置于恒容密闭真空容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s) 2NH3(g)+CO2(g)。能判断该反应已经达到化学平衡的是
2NH3(g)+CO2(g)。能判断该反应已经达到化学平衡的是______ 。
①v(NH3)正=2v(CO2)逆
②密闭容器中总压强不变
③密闭容器中混合气体的密度不变
④密闭容器中混合气体的平均相对分子质量不变
⑤密闭容器混合气体的总物质的量不变
⑥密闭容器中CO2的体积分数不变
⑦混合气体总质量不变
(2)一定条件下,在5L密闭容器内,反应2NO2(g) N2O4(g),NO2的物质的量随时间变化如表:
N2O4(g),NO2的物质的量随时间变化如表:
①用N2O4表示0~2s内该反应的平均速率为_______ mol/(L•s)。在第5s时,NO2的转化率为_______ 。在第2s时N2O4的体积分数为_______ 。
②为加快反应速率,可以采取的措施是_______ 。
a.升高温度 b.恒容时充入He(g) c.恒压时充入He(g) d.恒容时充入NO2
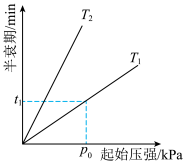
(3)已知:2N2O=2N2+O2,不同温度(T)下,N2O分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度N2O消耗一半时所需的相应时间),则T1______ T2(填“>”、“=”或“<”)。当温度为T1、起始压强为p0,反应至t1min时,此时体系压强p=_______ (用p0表示)。
(1)将一定量纯净的氨基甲酸铵置于恒容密闭真空容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s)
 2NH3(g)+CO2(g)。能判断该反应已经达到化学平衡的是
2NH3(g)+CO2(g)。能判断该反应已经达到化学平衡的是①v(NH3)正=2v(CO2)逆
②密闭容器中总压强不变
③密闭容器中混合气体的密度不变
④密闭容器中混合气体的平均相对分子质量不变
⑤密闭容器混合气体的总物质的量不变
⑥密闭容器中CO2的体积分数不变
⑦混合气体总质量不变
(2)一定条件下,在5L密闭容器内,反应2NO2(g)
 N2O4(g),NO2的物质的量随时间变化如表:
N2O4(g),NO2的物质的量随时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO2)/mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
②为加快反应速率,可以采取的措施是
a.升高温度 b.恒容时充入He(g) c.恒压时充入He(g) d.恒容时充入NO2
(3)已知:2N2O=2N2+O2,不同温度(T)下,N2O分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度N2O消耗一半时所需的相应时间),则T1

您最近一年使用:0次
2023-04-25更新
|
561次组卷
|
3卷引用:山西省大同市第一中学校2022-2023学年高一下学期5月月考化学试题
山西省大同市第一中学校2022-2023学年高一下学期5月月考化学试题 (已下线)【2023】【高一下】【其他】【杭高钱塘】【高中化学】【刘尼尼收集】河北省邢台市2022-2023学年高一下学期6月月考化学试题
名校
解题方法
7 . 一定条件下,将3molA气体和1molB气体混合于固定容积为2L的密闭容器中,发生反应:3A(g)+B(g) 4C(g)+2D(s)。2min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是
4C(g)+2D(s)。2min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是
 4C(g)+2D(s)。2min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是
4C(g)+2D(s)。2min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是
| A.若混合气体的密度不再改变时,该反应不一定达到平衡状态 |
| B.平衡时C的体积分数为40% |
| C.反应过程中A和B的转化率之比为3∶1 |
| D.从开始到平衡,用A表示的化学反应速率为0.6mol•L-1•min-1 |
您最近一年使用:0次
2023-04-25更新
|
43次组卷
|
2卷引用:山西省阳泉市第一中学校2022-2023学年高一下学期期中考试化学试题
9-10高一下·广东·期末
名校
8 . 对可逆反应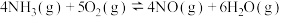 ,下列叙述正确的是
,下列叙述正确的是
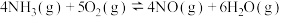 ,下列叙述正确的是
,下列叙述正确的是A.达到化学平衡时,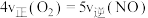 |
B.单位时间内生成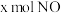 的同时,消耗 的同时,消耗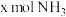 ,则反应达到平衡状态 ,则反应达到平衡状态 |
| C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |
D.化学反应速率关系是: |
您最近一年使用:0次
2023-04-24更新
|
1211次组卷
|
214卷引用:2010-2011学年山西省临汾一中高二上学期期末考试化学试卷
(已下线)2010-2011学年山西省临汾一中高二上学期期末考试化学试卷(已下线)2011-2012学年山西省汾阳市高二10月月考化学试卷(已下线)2011-2012学年山西省汾阳中学高二第二次月考化学试卷山西省运城市康杰中学2017-2018学年高二上学期第一次月考化学试题山西省朔州市平鲁区李林中学2018-2019学年高二上学期第一次月考化学试题山西省朔州市怀仁县第一中学2018-2019学年高二上学期第二次月考化学试题山西省朔州市怀仁市第一中学云东校区2019-2020学年高一期末考试化学试题山西省忻州市第一中学2019-2020学年高一4月月考化学试题山西省大同市浑源县第七中学2020-2021学年高二上学期第一次月考化学试题(已下线)09—10年梅县东山中学高一下学期期末考试化学卷(已下线)2010年江西省高安中学高二上学期期中考试化学卷(已下线)2010-2011学年云南省昆明一中高二下学期期中考试化学试卷(已下线)2010-2011学年广东省潮州金中高一下学期期中考试化学(理科班)化学卷(已下线)2010-2011学年河南省周口市高一下期期末调研考试化学试题(已下线)2011-2012年湖南省浏阳一中高二上学期段考化学试卷(已下线)2012届山东省济宁市邹城二中高三第二次月考化学试卷(已下线)2011-2012学年江西省新余九中高二上学期期中考试化学试卷(已下线)2012届河北省南宫中学高三上学期期中考试化学试卷(已下线)2011-2012学年山东省沂南一中高二上学期期中模块学分认定考试化学试卷(已下线)2012届甘肃省陇东中学高三第四次模拟考试化学试卷(已下线)2011-2012年广东东莞南城中学高二上学期期中考试化学试卷(已下线)2011-2012学年广东省佛山一中高一下学期期中考试化学试卷(已下线)2011-2012学年黑龙江省鹤岗一中高一下学期期末考试化学试卷(已下线)2011-2012学年安徽省舒城晓天中学高二下学期质量测试1化学试卷(已下线)2012-2013学年江西省南昌市第二中学高二第一次月考化学试卷(已下线)2012-2013学年重庆市第七中学高二上学期期中考试化学试卷(已下线)2013-2014学年江西省新余市高二上学期期末考试化学试卷(已下线)2014年高一化学人教版必修二 2-3-2化学反应的限度练习卷(已下线)2014年高中化学鲁科版选修四第2章 反应的方向限度与速率练习卷(已下线)2013-2014学年内蒙古赤峰市元宝山区高二上学期期末化学试卷(已下线)2014届江西省九江一中上学期期中考试高二化学试卷(已下线)2014-2015学年吉林省延边二中高二上学期期中理科化学卷(已下线)2014-2015学年黑龙江哈尔滨第三十二中学高二上学期期中考试化学卷(已下线)2015届北京十中高三第一学期期中化学试卷(已下线)2014-2015河北省石家庄第二实验中学高二上学期期中化学(理)试卷2014-2015学年宁夏育才中学高二上学期期中化学试卷2014-2015学年云南省蒙自市蒙自一中高二上学期期中化学试卷2014-2015江西省赣州市赣县中学北校区高二1月月考化学试卷2014-2015山东省平度市高二上学期期中考试化学试卷2014-2015江西省德镇市高二上学期期末化学试卷2015-2016学年山东省东营市一中高二第一学期开学收心考试化学试卷2015-2016学年辽宁葫芦岛一中高二上期初考试化学试卷 2015-2016学年湖北航天高中、安陆二中等五校高二上期中化学试卷2015-2016学年安徽省铜陵一中高二上期中测试化学试卷2015-2016学年甘肃省会宁一中高二上期中(理)化学试卷2015-2016学年陕西省镇安中学高二上期中质检化学试卷2015-2016学年江西省上高二中高一上期末化学试卷2015-2016学年广西南宁市八中高二下学期期中段考化学试卷2015-2016学年辽宁省沈阳铁路实验中学高一下期中化学试卷2015-2016学年河北省邯郸市曲周一中高一下期中化学试卷2015-2016学年广西宾阳县宾阳中学高二5月月考化学试卷2015-2016学年内蒙古包头九中高一6月月考化学试卷2015-2016学年陕西省黄陵中学高二下学期分班考试化学试卷2015-2016学年吉林长春第十一中高一下期末考化学2016-2017学年广东省潮阳实验学校高二上8月考试化学卷2017届河北省沧州一中高三上学期9.22周测化学卷2016-2017学年陕西省西安中学高二上10月月考化学试卷黑龙江省哈尔滨师大附中2016-2017学年高二10月月考化学卷2016-2017学年黑龙江大庆一中高二上10月月考化学卷2015-2016学年甘肃省白银市靖远一中高二上期中化学试卷2016-2017学年湖南省长沙一中高二上期中化学卷2016-2017学年河北省定州中学高二上期中化学试卷2016-2017学年天津市宝坻区高二11月联考化学试卷2016-2017学年宁夏吴忠中学高二下学期第一次月考化学试卷江西省南昌市八一中学、洪都中学、麻丘中学等六校2016-2017学年高一5月联考化学试题湖南省邵阳市第二中学2016-2017学年高一下学期第三次月考化学试题内蒙古北京八中乌兰察布分校2016-2017学年高一下学期第二次调考化学试题陕西省黄陵中学2016-2017学年高一(重点班)下学期期末考试化学试题江苏省泰州中学2016-2017学年高一下学期期末考试(选修)化学试题(已下线)2.3.1 化学平衡状态黑龙江省双鸭山市第一中学2017-2018学年高二9月月考化学试题湖北省长阳县第一高级中学2017-2018学年高二9月月考化学试题吉林省汪清县第六中学2018届高三9月月考化学试题江西省赣州市崇义中学2017-2018学年高二上学期第一次月考化学试题西藏日喀则市第二高级中学2017-2018学年高二上学期期中考试化学试题四川省成都市实验中学2017-2018学年高二上学期期中考试化学试题四川省乐山沫若中学2017-2018学年高二上学期第二次月考(12月)化学试题湖南省津市一中2017-2018学年高二第一学期期中考试化学(理)试卷内蒙古巴彦淖尔市第一中学2017-2018学年高二上学期期中考试(A卷)化学试题高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第三节 化学平衡 化学平衡第一课时(可逆反应)福建省莆田市第二十五中学2017-2018学年高二12月月考化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二上学期期中考试化学试题(B卷)云南民族大学附属中学2017-2018学年高二下学期第一次月考化学试题江苏省清江中学2017-2018学年高二下学期期中考试化学试题安徽省合肥第六中学2017-2018学年高二下学期期中考试(理科)化学试题【全国校级联考】福建省闽侯第二中学五校教学联合体2017-2018学年高二上学期期末考试化学试题【全国百强校】吉林省长春外国语学校2018-2019学年高二上学期期初考试化学试题湖南省醴陵市第一中学2018-2019学年高二上学期入学考试化学试题苏教版化学高中必修4模块综合检测题辽宁省大连市育明高级中学2018-2019学年高二上学期期初考试化学试题江西省上饶中学2018-2019学年高二上学期开学检测化学试题安徽省黄山市徽州区第一中学2018-2019学年高二上学期开学考试化学试题陕西煤铜川市炭建设公司第一中学2018-2019学年高二上学期10月月考化学试题湖南省娄底市第四中学2018-2019学年高二上学期10月月考化学试题【全国百强校】陕西省西安市第一中学2018-2019学年高二上学期10月月考化学试题【全国百强校】吉林省长春外国语学校2018-2019学年高二上学期期中考试化学试题2【全国百强校】安徽省铜陵市第一中学2018-2019学年高二上学期期中考试化学试题甘肃省岷县一中2018-2019学年高二上学期期中考试化学试题江西省上饶市第二中学2018-2019学年高二上学期期中考试化学试题新疆维吾尔自治区伊宁市生产建设兵团四师一中2018-2019学年高二上学期期中考试化学试题【校级联考】湖北省孝感市七校教学联盟2018-2019学年高二上学期期中联合考试化学试题吉林省长春市九台区师范高级中学2018-2019学年高二上学期期中考试化学试题安徽省定远重点中学2018-2019学年高二上学期第三次月考化学试题云南省景东一中2018-2019学年高二下学期开学考试化学试题(已下线)2019年4月12日《每日一题》 必修2 化学平衡状态标志的判断【区级联考】上海市黄浦区2019届高三下学期等级考二模试卷化学试题河北省定州中学2017届高三(高补班)下学期第一次月考化学试题江西省赣州市十五县(市)2018-2019学年高一下学期期中联考化学试题河北省永清县第一中学2018-2019学年高一下学期第二次月考化学试题【市级联考】贵州省遵义市2018-2019学年高一下学期期中考试化学试题江西省赣州市赣县三中2019-2020学年高二上学期入学考试化学试题云南省保山市第一中学2018-2019学年高二下学期期末化学试题湖南省衡阳市第一中学2019-2020学年高二上学期第一次月考化学试题新疆石河子第二中学2019-2020学年高二上学期第一次阶段考试化学试题广东省揭阳市惠来县第一中学2019-2020学年高二上学期第一次阶段考试化学试题江西省吉安市四校2018-2019学年高一下学期联考化学试题吉林松原乾安七中2019-2020学年高二上学期9月月考化学试题山东省淄博市淄川区般阳中学2019-2020学年高二10月月考化学试题吉林省松原市乾安县七中2019-2020学年高二上学期第一次月考化学试题江西省南城县第二中学2018-2019学年高二上学期第二次月考化学试题广东省揭阳市惠来县第一中学2019-2020学年高二上学期期中考试化学试题甘肃省镇原县镇原中学2019-2020学年高二上学期期中考试化学(理)试题甘肃省镇原县镇原中学2019-2020学年高一上学期期中考试化学(理)试题安徽省滁州市定远县民族中学2019-2020学年高二上学期期中考试化学试题北京市昌平区新学道临川学校2019-2020学年高二上学期期中考试化学试题安徽省淮北市濉溪县2018-2019学年高一上学期期末考试化学试题河北省唐山市遵化市第一中学2019-2020学年高二上学期第一次月考化学试题人教版(2019)高中化学必修第二册第六章《化学反应与能量》检测题2019-2020学年人教版高中化学高考基础复习专题7《化学反应速率与化学平衡》测试卷夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——化学平衡状态的建立及判断天津市西青区2019-2020学年高二上学期期末考试化学试题第2章 化学键化学反应规律 模拟高考——C挑战区 夯实基础(鲁科版(2019)第二册)第2章 化学键 化学反应与能量 模拟高考——C挑战区 夯实基础(鲁科版必修2)四川省乐山市第四中学2019-2020学年高一下学期期中考试化学试题河北省鸡泽县第一中学2019-2020学年高一下学期开学考试化学试题云南省昆明市东川区明月中学2018-2019学年高二下学期期中考试化学试题宁夏贺兰县景博中学2019-2020学年高二上学期第一次月考化学试题辽宁省锦州市黑山县黑山中学2019-2020学年高一6月质量检测化学试题青海省西宁市大通回族土族自治县第一完全中学2019-2020学年高一下学期期中考试化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第五次综合测试化学试题湖北省应城市第一高级中学2019-2020学年高一下学期复学摸底测试化学试题安徽省定远县育才学校2019-2020学年高二下学期期末考试化学试题吉林省长春外国语学校2019-2020学年高一下学期期末考试化学(理)试题黑龙江省肇州县第二中学2019-2020学年高一下学期6月月考化学试题山东省济宁市泗水县2019-2020学年高二上学期期中考试化学试题(已下线)第02章 化学反应速率和化学平衡(A卷基础篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)北京市首都师范大学附属中学2019-2020学年高一下学期结业考试(期末)化学试题辽宁省辽阳市辽阳县集美中学2020-2021学年高二上学期第一次月考化学试题(已下线)第二章 化学反应速率和化学平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)新疆哈密市第十五中学2021届高三上学期第一次质量检测化学试题人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡 教材帮(已下线)2.3.1化学平衡状态(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)山东省新泰市第一中学2020-2021学年高二上学期第一次阶段性考试化学试题河北省邢台市第七中学2019-2020学年高二上学期10月月考化学试题贵州省遵义市航天高级中学2020-2021学年高二上学期第一次月考化学(理)试题陕西省汉中市洋县中学2020-2021学年高二上学期第一次月考化学试题西藏拉萨市第二高级中学2019-2020学年高二上学期期中考试化学试题人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时1 化学平衡状态的特征甘肃省武威第十八中学2020-2021学年高二上学期期中考试化学试题山东省新泰市第一中学2019-2020学年高一下学期阶段测试一化学试题湖北省宜城市第三高级中学2020-2021学年高二上学期10月月考化学试题宁夏回族自治区石嘴山市平罗县平罗中学2020-2021学年高二上学期期中考试化学试题河北省石家庄市康福外国语学校2020-2021学年高二10月月考化学试题吉林省汪清县汪清第四中学2020-2021学年高二上学期第二阶段考试化学试题广西百色市平果县第二中学2020-2021学年高二10月月考理综化学试题山东省聊城市茌平区第二中学2020-2021学年高二上学期第二次月考化学试题新疆哈密市第十五中学2020-2021学年高二上学期期末考试化学试题高中化学苏教2019版必修第二册-专题6 本专题达标检测吉林省长春市清蒲中学2020-2021学年度高二上学期期末化学试题(已下线)专题10 化学反应速率与平衡-备战2021届高考化学二轮复习题型专练陕西省西安电子科技大学附属中学2020-2021学年高一下学期期中考试化学试题江苏省邳州市宿羊山高级中学2020-2021学年高二下学期第一次学情检测化学试题(已下线)第六章 化学反应与能量(培优提升卷)-2020-2021学年高一化学章末集训必刷卷(人教版2019必修第二册)云南省水富县云天化中学2020-2021学年高二下学期期中考试化学试题青海省海南州贵德高级中学2020-2021学年高二下学期期中化学试题陕西省西安市高新一中2020-2021学年高一下学期5月月考化学试题黑龙江省哈尔滨工业大学附属中学2020-2021学年度高二下学期期末考试化学试题江苏省苏州实验中学2020-2021学年高二下学期3月份学情调研考试化学试题选择性必修1(SJ)专题2第二单元课时2 化学平衡状态山东省曲阜市第一中学2017-2018学年高二上学期第一次月考化学试题河南省新乡县高级中学2021-2022学年高二上学期第一次月考化学试题西藏自治区拉萨那曲第二高级中学2021-2022学年高三上学期第一次月考化学试题吉林省长春市第二十九中学2021-2022学年高二上学期第一学程考试化学试题广东省惠州市第一中学2021-2022学年高二上学期第二次考试化学试题山东省淄博市第七中学2019-2020学年高二上学期第一次月考化学试题辽宁省滨海实验中学2019-2020学年高二上学期期末化学试题黑龙江省五校(嫩江市第一中学、嫩江市职业高中、伊拉哈中学、海江中学等)2021-2022学年高二上学期期中联考化学试题广东省惠州市第一中学2021-2022学年高二上学期期中考试化学试题甘肃省兰州市教育局第四片区2021-2022学年高二上学期期末考试化学(理)试题(已下线)2.2.2 化学平衡状态(1)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)四川省遂宁市射洪中学校2021—2022学年高二上学期第三次(12月)月考化学试题内蒙古自治区第二地质中学2020-2021学年高二下学期第二次阶段检测化学试题四川省雅安中学2021-2022学年高一下学期期中考试化学试题河南省禹州市2021-2022学年高一下学期期末调研考试化学试题安徽师范大学附属中学2022-2023学年高二上学期开学考试化学试题河南省中原名校2021-2022学年高二上学期期末联考化学试题重庆市天星桥中学2021-2022学年高二上学期第二次月考化学试题云南省昆明市第十中学2021-2022学年高二下学期3月月考化学试题重庆市巫山县官渡中学2020-2021年高二下学期第一次月考化学试题贵州省黔东南州从江县第一民族中学2021-2022学年高一下学期第二次月考化学试题甘肃省武威市古浪县第二中学2021-2022学年高二上学期期中化学试题陕西省安康市汉滨区五里高级中学2021-2022学年高二上学期期中考试化学试题辽宁省恒仁满族自治县第二高级中学2021-2022学年高二上学期期中考试化学试题(已下线)第七章 化学反应速率与化学平衡 第43练 化学平衡移动原理及应用河北省石家庄市辛集市2022-2023学年高二上学期期末教学质量监测化学试题福建省福州高级中学2022-2023学年高一下学期期中考试化学试题北京市第八中学2022-2023学年高一下学期期中考试(选考班)化学试题2.2.2化学平衡状态 课中(已下线)合格考汇编13化学反应速率和限度上海市延安中学2023-2024学年高二上学期期中考试(等级考)化学试题广东省广州市实验外国语高中2023-2024学年高二上学期10月月考化学试题福建省福州格致中学2023-2024学年高二上学期10月期中考试化学试题广西钦州市第四中学2023-2024学年高一下学期3月份考试化学试卷天津北京师范大学静海附属学校2023-2024学年高三上学期第三次月考化学试题
9 . 铁及铁的氧化物广泛应用于生产、生活、航天、科研等领域。回答下列问题:
(1)铁通过对 、
、 吸附和解吸可作为合成氨的固体催化剂,原理为
吸附和解吸可作为合成氨的固体催化剂,原理为
 。
。
①若用 、
、 、
、 和
和 分别表示
分别表示 、
、 、
、 和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示,吸附后能量状态最低的是
和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示,吸附后能量状态最低的是___________ (填标号)。

②在三个1L的恒容密闭容器中,分别加入 和
和 发生上述反应,实验a、b、c中
发生上述反应,实验a、b、c中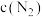 随时间(t)的变化如图所示(T表示温度),与实验b相比,实验a、实验c分别改变的实验条件可能为
随时间(t)的变化如图所示(T表示温度),与实验b相比,实验a、实验c分别改变的实验条件可能为___________ 、___________ (仅改变一个条件)。

(2) 与
与 反应可制备“纳米铁粉”,其反应为
反应可制备“纳米铁粉”,其反应为
 。
。
①一定温度下,将一定量的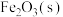 和
和 置于恒容密闭容器中反应,能说明反应达到平衡状态的是
置于恒容密闭容器中反应,能说明反应达到平衡状态的是___________ (填标号)。
A.混合气体的密度不再改变 B.铁的物质的量不再改变
C.CO和 的浓度之比为1:2 D.
的浓度之比为1:2 D.
②T℃时,向体积为2L的密闭容器中加入 和
和 进行上述反应,反应起始时压强为
进行上述反应,反应起始时压强为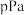 ,反应进行至5min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍,5min内用
,反应进行至5min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍,5min内用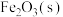 表示的平均反应速率为
表示的平均反应速率为___________ 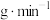 ;T℃该反应的
;T℃该反应的
___________  (气体分压=气体总压×气体体积分数)。
(气体分压=气体总压×气体体积分数)。
(3)“纳米铁粉”可用于处理地下水中的污染物,其中与 发生反应的离子方程式为
发生反应的离子方程式为 ,研究发现,相同条件下,纳米铁粉去除不同水样中
,研究发现,相同条件下,纳米铁粉去除不同水样中 的速率有较大差异(如下图),产生该差异的原因可能是
的速率有较大差异(如下图),产生该差异的原因可能是___________ (答一条即可)。

(1)铁通过对
 、
、 吸附和解吸可作为合成氨的固体催化剂,原理为
吸附和解吸可作为合成氨的固体催化剂,原理为
 。
。①若用
 、
、 、
、 和
和 分别表示
分别表示 、
、 、
、 和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示,吸附后能量状态最低的是
和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示,吸附后能量状态最低的是
②在三个1L的恒容密闭容器中,分别加入
 和
和 发生上述反应,实验a、b、c中
发生上述反应,实验a、b、c中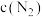 随时间(t)的变化如图所示(T表示温度),与实验b相比,实验a、实验c分别改变的实验条件可能为
随时间(t)的变化如图所示(T表示温度),与实验b相比,实验a、实验c分别改变的实验条件可能为
(2)
 与
与 反应可制备“纳米铁粉”,其反应为
反应可制备“纳米铁粉”,其反应为
 。
。①一定温度下,将一定量的
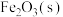 和
和 置于恒容密闭容器中反应,能说明反应达到平衡状态的是
置于恒容密闭容器中反应,能说明反应达到平衡状态的是A.混合气体的密度不再改变 B.铁的物质的量不再改变
C.CO和
 的浓度之比为1:2 D.
的浓度之比为1:2 D.
②T℃时,向体积为2L的密闭容器中加入
 和
和 进行上述反应,反应起始时压强为
进行上述反应,反应起始时压强为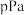 ,反应进行至5min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍,5min内用
,反应进行至5min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍,5min内用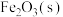 表示的平均反应速率为
表示的平均反应速率为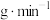 ;T℃该反应的
;T℃该反应的
 (气体分压=气体总压×气体体积分数)。
(气体分压=气体总压×气体体积分数)。(3)“纳米铁粉”可用于处理地下水中的污染物,其中与
 发生反应的离子方程式为
发生反应的离子方程式为 ,研究发现,相同条件下,纳米铁粉去除不同水样中
,研究发现,相同条件下,纳米铁粉去除不同水样中 的速率有较大差异(如下图),产生该差异的原因可能是
的速率有较大差异(如下图),产生该差异的原因可能是
您最近一年使用:0次
解题方法
10 . 甲醇是重要的化工原料,应用前景广泛。研究表明,二氧化碳与氢气反应可以合成甲醇,反应如下:
 kJ⋅mol
kJ⋅mol 。在550 K下,向容积为2 L的恒容密闭容器中充入2 mol
。在550 K下,向容积为2 L的恒容密闭容器中充入2 mol  和6 mol
和6 mol  ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。

回答下列问题:
(1)从反应开始到平衡,平均反应速率
_______ , 的平衡转化率为
的平衡转化率为_______ ,550 K下该反应的平衡常数K的数值为_______ (保留两位小数)。
(2)有利于提高 平衡转化率的措施有
平衡转化率的措施有_______ 。(填字母)
A.使用催化剂 B.加压 C.增大 和
和 的初始投料比
的初始投料比
(3)保持其他条件不变,温度升高时,甲醇的平衡产率将_______ (填“增大”、“减小”或“不变”),判断依据是_______ 。

 kJ⋅mol
kJ⋅mol 。在550 K下,向容积为2 L的恒容密闭容器中充入2 mol
。在550 K下,向容积为2 L的恒容密闭容器中充入2 mol  和6 mol
和6 mol  ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
回答下列问题:
(1)从反应开始到平衡,平均反应速率

 的平衡转化率为
的平衡转化率为(2)有利于提高
 平衡转化率的措施有
平衡转化率的措施有A.使用催化剂 B.加压 C.增大
 和
和 的初始投料比
的初始投料比(3)保持其他条件不变,温度升高时,甲醇的平衡产率将
您最近一年使用:0次



