名校
解题方法
1 . 工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol ΔS=-200J·K-1·mol-1。
2NH3(g) ΔH=-92.4kJ/mol ΔS=-200J·K-1·mol-1。
回答下列问题:
(1)合成氨反应在常温下___________  填“能”或“不能”
填“能”或“不能” 自发。
自发。
(2)某小组进行工业合成氨N2(g)+3H2(g) 2NH3(g) ΔH<0的模拟研究,在1 L密闭容器中,分别加入0.1 mol N2和0.3 mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
2NH3(g) ΔH<0的模拟研究,在1 L密闭容器中,分别加入0.1 mol N2和0.3 mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。

与实验①相比,实验②所改变的外界条件可能是___________ ,实验③所改变的外界条件可能为 ___________ 。
(3)400℃时,N2(g)+3H2(g) 2NH3(g) ΔH<0,K1=0.5,则对于反应2NH3(g)
2NH3(g) ΔH<0,K1=0.5,则对于反应2NH3(g)  N2(g)+3H2(g)的化学平衡常数K2=
N2(g)+3H2(g)的化学平衡常数K2=___________ ,若某时刻测得NH3、N2和H2物质的量浓度均为1mol•L-1时,则该反应的v正___________ v逆(填“<”、“>”或“=”)。
(4)某小组往一恒温恒压容器中充入9molN2和23molH2模拟合成氨的反应,如图为不同温度下平衡混合物中氨气的体积分数与总压强(P)的关系图。
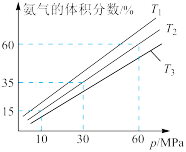
①温度T1、T2、T3中,最大的是___________ 。
②若体系在T2、60MPa下达到平衡如图所示,计算此时N2的平衡转化率为___________ 。
(5)某合成氨速率方程为: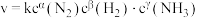 ,根据表中数据,
,根据表中数据,
___________ ;
 2NH3(g) ΔH=-92.4kJ/mol ΔS=-200J·K-1·mol-1。
2NH3(g) ΔH=-92.4kJ/mol ΔS=-200J·K-1·mol-1。 回答下列问题:
(1)合成氨反应在常温下
 填“能”或“不能”
填“能”或“不能” 自发。
自发。(2)某小组进行工业合成氨N2(g)+3H2(g)
 2NH3(g) ΔH<0的模拟研究,在1 L密闭容器中,分别加入0.1 mol N2和0.3 mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
2NH3(g) ΔH<0的模拟研究,在1 L密闭容器中,分别加入0.1 mol N2和0.3 mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
与实验①相比,实验②所改变的外界条件可能是
(3)400℃时,N2(g)+3H2(g)
 2NH3(g) ΔH<0,K1=0.5,则对于反应2NH3(g)
2NH3(g) ΔH<0,K1=0.5,则对于反应2NH3(g)  N2(g)+3H2(g)的化学平衡常数K2=
N2(g)+3H2(g)的化学平衡常数K2=(4)某小组往一恒温恒压容器中充入9molN2和23molH2模拟合成氨的反应,如图为不同温度下平衡混合物中氨气的体积分数与总压强(P)的关系图。

①温度T1、T2、T3中,最大的是
②若体系在T2、60MPa下达到平衡如图所示,计算此时N2的平衡转化率为
(5)某合成氨速率方程为:
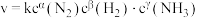 ,根据表中数据,
,根据表中数据,
| 实验 | c(N2)/mol/L | c(H2)/mol/L | c(NH3)/mol/L | v/mol·L-1·s-1 |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 2.828q |
您最近一年使用:0次
解题方法
2 . 在 的密闭容器内充入
的密闭容器内充入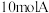 气体和
气体和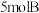 气体发生如下反应:
气体发生如下反应: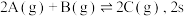 后达到平衡,此时测得平衡混合物中
后达到平衡,此时测得平衡混合物中 的浓度为
的浓度为 。则:
。则:
(1)用 的浓度变化表示该反应的平均反应速率
的浓度变化表示该反应的平均反应速率___________ ;
(2)达到平衡后 的转化率为
的转化率为___________ ;
(3)平衡混合物中 的浓度为
的浓度为___________ ;
(4)平衡混合物中 气体的体积分数为
气体的体积分数为___________ 。
(5)已知该反应能自发进行,则
___________ 。
 的密闭容器内充入
的密闭容器内充入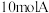 气体和
气体和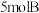 气体发生如下反应:
气体发生如下反应: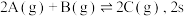 后达到平衡,此时测得平衡混合物中
后达到平衡,此时测得平衡混合物中 的浓度为
的浓度为 。则:
。则:(1)用
 的浓度变化表示该反应的平均反应速率
的浓度变化表示该反应的平均反应速率(2)达到平衡后
 的转化率为
的转化率为(3)平衡混合物中
 的浓度为
的浓度为(4)平衡混合物中
 气体的体积分数为
气体的体积分数为(5)已知该反应能自发进行,则

您最近一年使用:0次
名校
解题方法
3 . 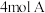 气体和
气体和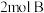 气体在
气体在 的容器中混合并在一定条件下发生如下反应:
的容器中混合并在一定条件下发生如下反应: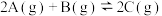 。若经
。若经 后测得C的浓度为
后测得C的浓度为 ,现有下列几种说法:
,现有下列几种说法:
①用物质A表示的反应平均速率为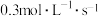
②用物质B表示的反应的平均速率为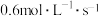
③ 时物质A的转化率为70%
时物质A的转化率为70%
④ 时物质B的浓度为
时物质B的浓度为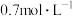
其中正确的是
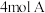 气体和
气体和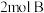 气体在
气体在 的容器中混合并在一定条件下发生如下反应:
的容器中混合并在一定条件下发生如下反应: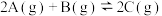 。若经
。若经 后测得C的浓度为
后测得C的浓度为 ,现有下列几种说法:
,现有下列几种说法:①用物质A表示的反应平均速率为
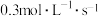
②用物质B表示的反应的平均速率为
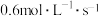
③
 时物质A的转化率为70%
时物质A的转化率为70%④
 时物质B的浓度为
时物质B的浓度为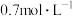
其中正确的是
| A.①③ | B.①④ | C.②③ | D.③④ |
您最近一年使用:0次
2023-09-17更新
|
442次组卷
|
10卷引用:陕西省西安市鄠邑区2023-2024学年高二上学期期中质量检测化学试题
陕西省西安市鄠邑区2023-2024学年高二上学期期中质量检测化学试题北京市顺义区牛栏山第一中学2021-2022学年高一下学期阶段性检测化学试题(已下线)第12练 用“三段式”模型突破化学平衡的计算-2022年【暑假分层作业】高二化学(2023届一轮复习通用)浙江省舟山中学2021-2022学年高一下学期学考考前质量检测化学试题 河南大学附属中学2022-2023学年高一下学期期中考试 化学试题广东省佛山市三水中学2022-2023学年高二上学期10月第一次统测化学试题北京市育才学校2023-2024学年高二上学期10月月考化学试题广东省松湖莞中、深大附中两校2023-2024学年高二上学期10月联考化学试题海南省海口市第一中学2023-2024学年高三上学期期末考试化学试题(非重点班)河南省濮阳市南乐县第一高级中学2023-2024学年高一下学期模拟预测化学试题
4 . 二甲醚( )是一种新型能源。工业上,在催化剂作用下,合成二甲醚的化学方程式为
)是一种新型能源。工业上,在催化剂作用下,合成二甲醚的化学方程式为
 。回答下列问题:
。回答下列问题:
(1)几种共价键的键能如下表所示:

___________  。
。
(2)若其他条件不变,升高温度, 的转化率
的转化率___________ (填“增大”“减小”或“不变”)。恒温条件下,能提高二甲醚产率的措施有___________ (写一条)。
(3)500℃时,在体积为2L的密闭容器中充入2mol (g)和6mol
(g)和6mol  (g),10min后测得体系压强不再变化,此时
(g),10min后测得体系压强不再变化,此时 。则用
。则用 表示的平均反应速率为
表示的平均反应速率为___________ , 的转化率为
的转化率为___________ ,在该温度下反应的化学平衡常数K为___________ (用分数表示)。
(4)在密闭容器中进行反应 ,
, 的转化率
的转化率 与温度、压强的关系如图所示。
与温度、压强的关系如图所示。

X代表___________ (填“温度”或“压强”),
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
 )是一种新型能源。工业上,在催化剂作用下,合成二甲醚的化学方程式为
)是一种新型能源。工业上,在催化剂作用下,合成二甲醚的化学方程式为
 。回答下列问题:
。回答下列问题:(1)几种共价键的键能如下表所示:
| 化学键 | C=O( ) ) | H-H | C-H | C-O | H-O |
键能( ) ) | 803 | 436 | 414 | 326 | 463 |

 。
。(2)若其他条件不变,升高温度,
 的转化率
的转化率(3)500℃时,在体积为2L的密闭容器中充入2mol
 (g)和6mol
(g)和6mol  (g),10min后测得体系压强不再变化,此时
(g),10min后测得体系压强不再变化,此时 。则用
。则用 表示的平均反应速率为
表示的平均反应速率为 的转化率为
的转化率为(4)在密闭容器中进行反应
 ,
, 的转化率
的转化率 与温度、压强的关系如图所示。
与温度、压强的关系如图所示。
X代表

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
解题方法
5 . 合成氨是人类科学技术发展史上的一项重大突破。回答下列问题:
(1) 与
与 反应的能量变化如图所示,则反应
反应的能量变化如图所示,则反应 的
的 为
为___________ 。

(2)在773K时,分别将 和
和 充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中
充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中 、
、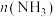 与反应时间t的关系如下表:
与反应时间t的关系如下表:
①该温度下,若向相同容积的另一容器中充入的 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 ,则此时
,则此时
___________ (填“>”“=”或“<”) 。
。
②由上表中的实验数据计算得到“浓度-时间”的关系可用图中的曲线表示,表示 的曲线是
的曲线是___________ (填“甲”“乙”或“丙”);在此温度下,若起始充入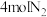 和
和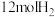 ,则反应刚达到平衡时,表示
,则反应刚达到平衡时,表示 的曲线上相应的点为
的曲线上相应的点为___________ (填字母)。

(3)T℃时,在2L恒容密闭容器中通入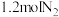 和
和 模拟一定条件下工业固氮[
模拟一定条件下工业固氮[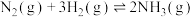 ],体系中
],体系中 随时间的变化如图。T℃时,该反应的平衡常数为
随时间的变化如图。T℃时,该反应的平衡常数为___________ 。

(4)合成氨反应中,正反应速率 ,逆反应速率
,逆反应速率 ,
, 、
、 为速率常数,只与温度有关。正反应和逆反应的平衡常数与温度的关系如图所示:
为速率常数,只与温度有关。正反应和逆反应的平衡常数与温度的关系如图所示:

①表示逆反应的平衡常数与温度变化关系的曲线为___________ (填“ ”或“
”或“ ”),理由为
”),理由为___________ 。
② ℃时,
℃时,
___________ 。
(5)以氨作为燃料的燃料电池,具有能量效率高的特点。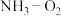 燃料电池的结构如图所示。负极的电极反应式为
燃料电池的结构如图所示。负极的电极反应式为___________ 。

(1)
 与
与 反应的能量变化如图所示,则反应
反应的能量变化如图所示,则反应 的
的 为
为
(2)在773K时,分别将
 和
和 充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中
充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中 、
、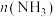 与反应时间t的关系如下表:
与反应时间t的关系如下表:| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
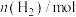 | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
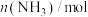 | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 ,则此时
,则此时
 。
。②由上表中的实验数据计算得到“浓度-时间”的关系可用图中的曲线表示,表示
 的曲线是
的曲线是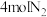 和
和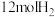 ,则反应刚达到平衡时,表示
,则反应刚达到平衡时,表示 的曲线上相应的点为
的曲线上相应的点为
(3)T℃时,在2L恒容密闭容器中通入
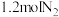 和
和 模拟一定条件下工业固氮[
模拟一定条件下工业固氮[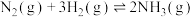 ],体系中
],体系中 随时间的变化如图。T℃时,该反应的平衡常数为
随时间的变化如图。T℃时,该反应的平衡常数为
(4)合成氨反应中,正反应速率
 ,逆反应速率
,逆反应速率 ,
, 、
、 为速率常数,只与温度有关。正反应和逆反应的平衡常数与温度的关系如图所示:
为速率常数,只与温度有关。正反应和逆反应的平衡常数与温度的关系如图所示:
①表示逆反应的平衡常数与温度变化关系的曲线为
 ”或“
”或“ ”),理由为
”),理由为②
 ℃时,
℃时,
(5)以氨作为燃料的燃料电池,具有能量效率高的特点。
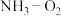 燃料电池的结构如图所示。负极的电极反应式为
燃料电池的结构如图所示。负极的电极反应式为
您最近一年使用:0次
名校
解题方法
6 . 用 合成燃料甲醇(
合成燃料甲醇( )是碳减排的新方向。现进行如下实验:某温度下在体积为1L的密闭容器中,充入2mol
)是碳减排的新方向。现进行如下实验:某温度下在体积为1L的密闭容器中,充入2mol 和6mol
和6mol 发生反应:
发生反应: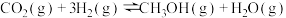 ,请回答下列问题:
,请回答下列问题:
(1)能判断该反应已达化学平衡状态的标志是___________(填字母)。
(2)现测得 和
和 的浓度随时间变化如图所示,回答下列问题:
的浓度随时间变化如图所示,回答下列问题:
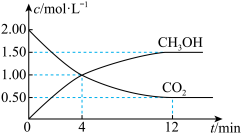
①从反应开始到平衡,氢气的平均反应速率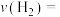
___________ 。
②平衡时甲醇的体积分数为___________ ,反应过程中 的最大转化率为
的最大转化率为___________ 。
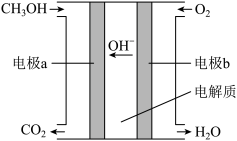
(3)下图是以 为电解质溶液的甲醇燃料电池示意图:
为电解质溶液的甲醇燃料电池示意图: ,通入氧气的电极为燃料电池的
,通入氧气的电极为燃料电池的___________ 极(填“正”或“负”),其电极反应式为___________ ,随着电池工作,电解质溶液的 如何变化
如何变化___________ 。
A.变大 B.变小 C.不变 D.无法判断
 合成燃料甲醇(
合成燃料甲醇( )是碳减排的新方向。现进行如下实验:某温度下在体积为1L的密闭容器中,充入2mol
)是碳减排的新方向。现进行如下实验:某温度下在体积为1L的密闭容器中,充入2mol 和6mol
和6mol 发生反应:
发生反应: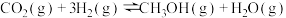 ,请回答下列问题:
,请回答下列问题:(1)能判断该反应已达化学平衡状态的标志是___________(填字母)。
| A.CO2百分含量保持不变 | B.容器中H2浓度与CO2浓度之比为3:1 |
| C.容器中混合气体的密度保持不变 | D.CO2的生成速率与CH3OH的生成速率相等 |
(2)现测得
 和
和 的浓度随时间变化如图所示,回答下列问题:
的浓度随时间变化如图所示,回答下列问题:
①从反应开始到平衡,氢气的平均反应速率
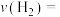
②平衡时甲醇的体积分数为
 的最大转化率为
的最大转化率为(3)下图是以
 为电解质溶液的甲醇燃料电池示意图:
为电解质溶液的甲醇燃料电池示意图: ,通入氧气的电极为燃料电池的
,通入氧气的电极为燃料电池的 如何变化
如何变化
A.变大 B.变小 C.不变 D.无法判断
您最近一年使用:0次
名校
7 . 某校课外活动小组利用草酸( )溶液和酸性
)溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为
溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为 ,实验记录如表。
,实验记录如表。
回答下列问题:
(1)通过实验①、②可探究草酸浓度的改变对反应速率的影响,则
_______ ;通过实验_______ 可探究温度变化对化学反应速率的影响。由实验②③可推断
_______ (填“>”“<”或“=”)10s。
(2)若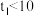 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是_______ ;利用实验②中数据,用 的浓度变化表示的反应平均速率为
的浓度变化表示的反应平均速率为_______  (保留2位有效数字)。
(保留2位有效数字)。
(3)某同学取1支试管加入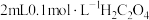 溶液,另取1支试管加入
溶液,另取1支试管加入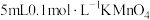 酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是
酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是_______ 。
(4)已知一定条件下40℃时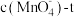 的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时
的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时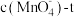 的变化曲线示意图
的变化曲线示意图_______ 。

 )溶液和酸性
)溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为
溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为 ,实验记录如表。
,实验记录如表。| 实验序号 | 实验温度/℃ |  溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | 溶液颜色褪至无色时所需时间/s | ||
| V/mL | 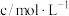 | V/mL | 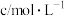 | V/mL | |||
| ① | 20 | 2 | 0.02 | 5 | 0.1 | 5 |  |
| ② | 20 | 2 | 0.02 | 4 | 0.1 |  | 10 |
| ③ | 40 | 2 | 0.02 | 4 | 0.1 | 6 |  |
(1)通过实验①、②可探究草酸浓度的改变对反应速率的影响,则


(2)若
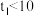 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应平均速率为
的浓度变化表示的反应平均速率为 (保留2位有效数字)。
(保留2位有效数字)。(3)某同学取1支试管加入
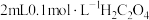 溶液,另取1支试管加入
溶液,另取1支试管加入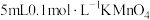 酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是
酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是(4)已知一定条件下40℃时
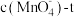 的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时
的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时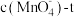 的变化曲线示意图
的变化曲线示意图
您最近一年使用:0次
2023-09-08更新
|
168次组卷
|
5卷引用:陕西省榆林市“府、靖、绥、横、定“五校联考2023-2024学年高二上学期11月期中化学试题
解题方法
8 . 一定条件下,H2O(g)在某催化剂表面上发生分解反应生成H2和O2,测得的实验结果如图所示。下列叙述正确的是

已知:化学上,将反应物消耗一半所用的时间称为半衰期(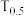 )。
)。

已知:化学上,将反应物消耗一半所用的时间称为半衰期(
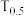 )。
)。| A.H2O(g)在该催化剂表面的分解反应是可逆反应 |
| B.H2O(g)的半衰期与起始浓度成反比 |
| C.在该催化剂表面H2O(g)分解反应先快后慢 |
D.ab段O2的平均生成速率为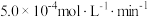 |
您最近一年使用:0次
2023-08-31更新
|
192次组卷
|
3卷引用:陕西省部分学校2024届高三上学期8月入学考试化学试题
解题方法
9 . 研究氮的氧化物\碳的氧化物等大气污染物的处理有重要意义。
(1)汽车尾气中NO生成过程中的能量变化如图所示。___________ (填“吸收”或“放出”)___________ kJ的热量。
(2)汽车排气管内安装的催化转化器可使尾气的主要污染物(NO和CO)转化为无毒的大气循环物质。一定温度下,在恒容密闭容器中发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是___________(填序号)。
2CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是___________(填序号)。
(3)某温度时,在2 L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。请回答下列问题:___________ 。
②反应从开始至2 min,用Z的浓度变化表示的平均反应速率v(Z)=___________ 。
③2 min后反应达到平衡,容器内混合气体的密度比起始时___________ 。 (填“增大”“减小”或“不变”,下同);
④下列措施能加快反应速率的是___________ (填序号,下同)。
A.恒压时充入He B.恒容时充入He C.恒容时充入X D.及时分离出Z E.升高温度
(1)汽车尾气中NO生成过程中的能量变化如图所示。

(2)汽车排气管内安装的催化转化器可使尾气的主要污染物(NO和CO)转化为无毒的大气循环物质。一定温度下,在恒容密闭容器中发生反应:2NO(g)+2CO(g)
 2CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是___________(填序号)。
2CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是___________(填序号)。| A.反应速率v(NO)=v(CO) | B.混合气体中NO的物质的量分数保持不变 |
| C.混合气体的密度不再改变 | D.混合气体的压强不再改变 |
(3)某温度时,在2 L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。请回答下列问题:

②反应从开始至2 min,用Z的浓度变化表示的平均反应速率v(Z)=
③2 min后反应达到平衡,容器内混合气体的密度比起始时
④下列措施能加快反应速率的是
A.恒压时充入He B.恒容时充入He C.恒容时充入X D.及时分离出Z E.升高温度
您最近一年使用:0次
解题方法
10 . 在四个不同的容器中,不同条件下进行的合成氨反应N2+3H2 2NH3,其中生成氨气速率最快的是
2NH3,其中生成氨气速率最快的是
 2NH3,其中生成氨气速率最快的是
2NH3,其中生成氨气速率最快的是| A.v(N2)=0.3 mol·L-1·min-1 | B.v(NH3)=0.5 mol·L-1·min-1 |
| C.v(H2)=0.01 mol·L-1·s-1 | D.v(N2)=0.2 mol·L-1·min-1 |
您最近一年使用:0次
2023-08-31更新
|
260次组卷
|
4卷引用:陕西省商洛市洛南中学2022-2023学年高一下学期4月期中考试化学试题
陕西省商洛市洛南中学2022-2023学年高一下学期4月期中考试化学试题(已下线)6.2.1化学反应的速率课后作业提高篇(已下线)期中测试卷二【测试范围:第五、六章】-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)6.2.1 化学反应的速率 随堂练习



