1 . 中国科学家设计构建了结构封装双钯活性位点—纳米“蓄水”膜反应器,实现了 一步无副反应高效稳定制乙醇。回答下列问题:
一步无副反应高效稳定制乙醇。回答下列问题:
(1)已知乙醇、氢气的标准燃烧热 分别为
分别为 、
、 ,则反应
,则反应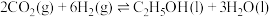 的
的
___________  ,该反应在
,该反应在___________ (填“高温下”“低温下”或“任何温度下均”)有利于自发进行。
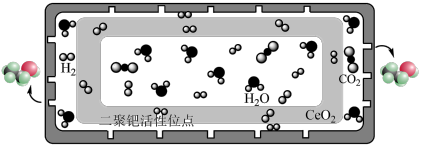
(2)结构封装双钯活性位点—纳米“蓄水”膜反应器结构(如图所示)类似于一个胶囊,胶囊内部封装了二氧化铈载体分散的双钯催化剂,胶囊的壳层具有高选择性、疏水性,可及时分离出产物乙醇。该反应器可使 高效稳定地转化为乙醇,请分析可能原因:
高效稳定地转化为乙醇,请分析可能原因:___________ 。
(3)在一恒压密闭容器中充入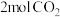 、
、 ,发生主反应I
,发生主反应I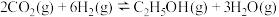 、副反应II
、副反应II 。已知初始压强为
。已知初始压强为 ,反应
,反应 时,测得
时,测得 下,总共生成
下,总共生成 水。甲醇与乙醇的选择性[如
水。甲醇与乙醇的选择性[如 的选择性
的选择性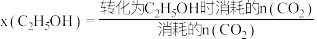 ]随温度和反应时间的变化关系如图。
]随温度和反应时间的变化关系如图。
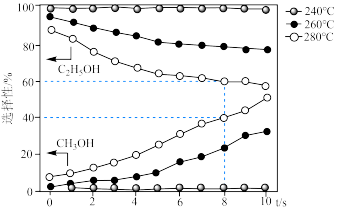
①在 下,当温度为
下,当温度为 时,乙醇的选择性能保持在近
时,乙醇的选择性能保持在近 的水平,但温度为
的水平,但温度为 和
和 时选择性大幅下降,其原因可能为
时选择性大幅下降,其原因可能为___________ 。
② 下,
下, 内
内 的转化率为
的转化率为___________ %,氢气分压的平均变化率为___________  。
。
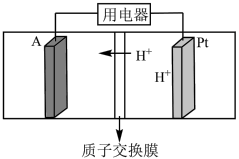
(4)酸性 燃料电池的装置图如图所示,A极输入的物质为
燃料电池的装置图如图所示,A极输入的物质为___________ (填化学式), 极的电极反应式为
极的电极反应式为___________ 。
 一步无副反应高效稳定制乙醇。回答下列问题:
一步无副反应高效稳定制乙醇。回答下列问题:(1)已知乙醇、氢气的标准燃烧热
 分别为
分别为 、
、 ,则反应
,则反应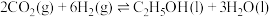 的
的
 ,该反应在
,该反应在(2)结构封装双钯活性位点—纳米“蓄水”膜反应器结构(如图所示)类似于一个胶囊,胶囊内部封装了二氧化铈载体分散的双钯催化剂,胶囊的壳层具有高选择性、疏水性,可及时分离出产物乙醇。该反应器可使
 高效稳定地转化为乙醇,请分析可能原因:
高效稳定地转化为乙醇,请分析可能原因:
(3)在一恒压密闭容器中充入
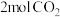 、
、 ,发生主反应I
,发生主反应I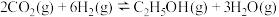 、副反应II
、副反应II 。已知初始压强为
。已知初始压强为 ,反应
,反应 时,测得
时,测得 下,总共生成
下,总共生成 水。甲醇与乙醇的选择性[如
水。甲醇与乙醇的选择性[如 的选择性
的选择性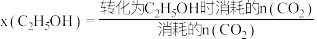 ]随温度和反应时间的变化关系如图。
]随温度和反应时间的变化关系如图。
①在
 下,当温度为
下,当温度为 时,乙醇的选择性能保持在近
时,乙醇的选择性能保持在近 的水平,但温度为
的水平,但温度为 和
和 时选择性大幅下降,其原因可能为
时选择性大幅下降,其原因可能为②
 下,
下, 内
内 的转化率为
的转化率为 。
。(4)酸性
 燃料电池的装置图如图所示,A极输入的物质为
燃料电池的装置图如图所示,A极输入的物质为 极的电极反应式为
极的电极反应式为
您最近一年使用:0次
2024-03-31更新
|
119次组卷
|
2卷引用:2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学
解题方法
2 . 羰基硫( ,沸点:
,沸点: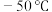 )又称氧硫化碳,其结构与
)又称氧硫化碳,其结构与 类似.回答下列问题:
类似.回答下列问题:
(1)实验室中通常用粉状硫氰化钾、水和浓硫酸反应制备 ,同时生成两种硫酸氢盐。写出该反应的化学方程式:
,同时生成两种硫酸氢盐。写出该反应的化学方程式:__________________________________ .
(2)以 为原料制备其他含硫物质的流程如下(部分产物已略去):
为原料制备其他含硫物质的流程如下(部分产物已略去):
 溶液
溶液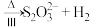
①反应Ⅰ中另一种产物是_____________ 。
②写出反应Ⅲ的离子方程式:_____________________________________________ 。
(3) 和
和 反应是制备
反应是制备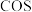 的另一种方法。恒温下,向体积为
的另一种方法。恒温下,向体积为 密闭容器中分别充入
密闭容器中分别充入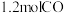 和
和 ,发生反应:
,发生反应: 后达到平衡状态,测得混合体系中含
后达到平衡状态,测得混合体系中含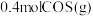 。
。
①平衡时, 的浓度为
的浓度为_____________  ;
; 内用
内用 表示的化学反应速率
表示的化学反应速率_____________  。
。
②下列描述中能说明上述反应已达平衡状态的是_____________ (填字母)。
a.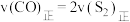
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器内气体压强保持不变
 ,沸点:
,沸点: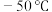 )又称氧硫化碳,其结构与
)又称氧硫化碳,其结构与 类似.回答下列问题:
类似.回答下列问题:(1)实验室中通常用粉状硫氰化钾、水和浓硫酸反应制备
 ,同时生成两种硫酸氢盐。写出该反应的化学方程式:
,同时生成两种硫酸氢盐。写出该反应的化学方程式:(2)以
 为原料制备其他含硫物质的流程如下(部分产物已略去):
为原料制备其他含硫物质的流程如下(部分产物已略去): 溶液
溶液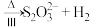
①反应Ⅰ中另一种产物是
②写出反应Ⅲ的离子方程式:
(3)
 和
和 反应是制备
反应是制备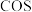 的另一种方法。恒温下,向体积为
的另一种方法。恒温下,向体积为 密闭容器中分别充入
密闭容器中分别充入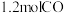 和
和 ,发生反应:
,发生反应: 后达到平衡状态,测得混合体系中含
后达到平衡状态,测得混合体系中含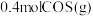 。
。①平衡时,
 的浓度为
的浓度为 ;
; 内用
内用 表示的化学反应速率
表示的化学反应速率 。
。②下列描述中能说明上述反应已达平衡状态的是
a.
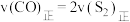
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器内气体压强保持不变
您最近一年使用:0次
解题方法
3 . 2022年北京冬奥会开幕式于2022年2月4日在国家体育场鸟巢隆重举行,其中奥运圣火的燃料为氢燃料,具有热值高、耐寒、环保无污染等优点。工业上可以通过催化重整二氧化碳和水蒸气制氢,主要有如下三个反应:
Ⅰ. ;
;
Ⅱ. ;
;
Ⅲ. 。
。
回答下列问题:
(1)反应
_____________ 。
(2)将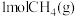 与
与 充入初始体积为
充入初始体积为 的恒压反应容器中,平衡时,各含碳物质的物质的量分数与温度之间的变化关系如图所示。
的恒压反应容器中,平衡时,各含碳物质的物质的量分数与温度之间的变化关系如图所示。

①曲线a代表的物质为_____________ (填化学式,下同);曲线c代表的物质为_____________ 。
② 至
至 ,曲线b代表物质的物质的量分数先随温度升高而增大的主要原因是
,曲线b代表物质的物质的量分数先随温度升高而增大的主要原因是___________________________________________________ 。
③ 时,反应进行
时,反应进行 后,甲烷的物质的量浓度为
后,甲烷的物质的量浓度为 内
内 表示的化学反应速率为
表示的化学反应速率为_____________  ;平衡时,容器中气体总物质的量为
;平衡时,容器中气体总物质的量为 ,容器体积为
,容器体积为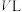 ,则反应Ⅰ的平衡常数
,则反应Ⅰ的平衡常数
_____________ (通过反应Ⅰ、Ⅱ计算即可,反应Ⅲ不影响计算结果,用含有n、V的代数式表示,不需要化简)。
Ⅰ.
 ;
;Ⅱ.
 ;
;Ⅲ.
 。
。回答下列问题:
(1)反应

(2)将
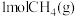 与
与 充入初始体积为
充入初始体积为 的恒压反应容器中,平衡时,各含碳物质的物质的量分数与温度之间的变化关系如图所示。
的恒压反应容器中,平衡时,各含碳物质的物质的量分数与温度之间的变化关系如图所示。
①曲线a代表的物质为
②
 至
至 ,曲线b代表物质的物质的量分数先随温度升高而增大的主要原因是
,曲线b代表物质的物质的量分数先随温度升高而增大的主要原因是③
 时,反应进行
时,反应进行 后,甲烷的物质的量浓度为
后,甲烷的物质的量浓度为 内
内 表示的化学反应速率为
表示的化学反应速率为 ;平衡时,容器中气体总物质的量为
;平衡时,容器中气体总物质的量为 ,容器体积为
,容器体积为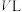 ,则反应Ⅰ的平衡常数
,则反应Ⅰ的平衡常数
您最近一年使用:0次
4 . 科研、生产中常涉及碳的化合物。回答下列问题:
(1) 时,向容积为
时,向容积为 的恒容密闭容器中充入一定量的
的恒容密闭容器中充入一定量的 和
和 ,发生反应:
,发生反应: ,反应过程中测定的部分数据见下表:
,反应过程中测定的部分数据见下表:
①反应前 内的平均反应速率
内的平均反应速率
_________ ;表中 的值为
的值为___________ 。
②判定 时达到平衡状态的理由是
时达到平衡状态的理由是___________ 。
(2)工业上可利用煤的气化产物(水煤气)合成二甲醚: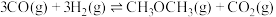
 。一定条件下的密闭容器中,该反应达到平衡,要提高
。一定条件下的密闭容器中,该反应达到平衡,要提高 的转化率,可以采取的措施是___________(填字母)。
的转化率,可以采取的措施是___________(填字母)。
(3)高炉炼铁中发生的主要反应为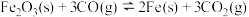 。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式
。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式
___________ ,
___________ 0(填“>”“<”或“=”)。

(4) 和
和 通入聚焦太阳能反应器中,发生反应:
通入聚焦太阳能反应器中,发生反应:
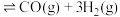 ,将等物质的量的
,将等物质的量的 和
和 充入
充入 恒容密闭反应器中,某温度下反应达到平衡,平衡常数
恒容密闭反应器中,某温度下反应达到平衡,平衡常数 ,此时测得
,此时测得 ,则
,则 的平衡转化率为
的平衡转化率为___________ (保留两位有效数字)。
(1)
 时,向容积为
时,向容积为 的恒容密闭容器中充入一定量的
的恒容密闭容器中充入一定量的 和
和 ,发生反应:
,发生反应: ,反应过程中测定的部分数据见下表:
,反应过程中测定的部分数据见下表:反应时间 | 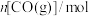 |  |
| 0 | 1.8 | 0.9 |
| 2 | 1.2 |  |
| 4 |  | 0.3 |
 内的平均反应速率
内的平均反应速率
 的值为
的值为②判定
 时达到平衡状态的理由是
时达到平衡状态的理由是(2)工业上可利用煤的气化产物(水煤气)合成二甲醚:
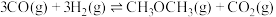
 。一定条件下的密闭容器中,该反应达到平衡,要提高
。一定条件下的密闭容器中,该反应达到平衡,要提高 的转化率,可以采取的措施是___________(填字母)。
的转化率,可以采取的措施是___________(填字母)。| A.升高温度 | B.加入催化剂 |
C.减小 的浓度 的浓度 | D.增大压强(缩小容器体积) |
(3)高炉炼铁中发生的主要反应为
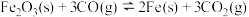 。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式
。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式


(4)
 和
和 通入聚焦太阳能反应器中,发生反应:
通入聚焦太阳能反应器中,发生反应:
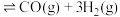 ,将等物质的量的
,将等物质的量的 和
和 充入
充入 恒容密闭反应器中,某温度下反应达到平衡,平衡常数
恒容密闭反应器中,某温度下反应达到平衡,平衡常数 ,此时测得
,此时测得 ,则
,则 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
2024-02-07更新
|
34次组卷
|
2卷引用:陕西省榆林市府谷县第一中学2023-2024学年高二上学期12月月考化学试题
5 . 一定条件下,在容积为 的密闭容器中,发生反应
的密闭容器中,发生反应 ,在不同温度下甲醇的物质的量随时间的变化如图所示。下列叙述正确的是
,在不同温度下甲醇的物质的量随时间的变化如图所示。下列叙述正确的是

 的密闭容器中,发生反应
的密闭容器中,发生反应 ,在不同温度下甲醇的物质的量随时间的变化如图所示。下列叙述正确的是
,在不同温度下甲醇的物质的量随时间的变化如图所示。下列叙述正确的是
A.平行常数 |
| B.300℃时,加入催化剂,甲醇的平衡浓度不变 |
C.在其他条件不变的情况下,将处于 点体系的容积压缩到原来的一半,氢气的浓度减小 点体系的容积压缩到原来的一半,氢气的浓度减小 |
D.500℃时,从反应开始到平衡,氢气的平均反应速率 |
您最近一年使用:0次
名校
解题方法
6 . 甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、 和
和 )在催化剂作用下可合成甲醇,发生的主要反应如下:
)在催化剂作用下可合成甲醇,发生的主要反应如下:
Ⅰ.
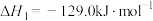 ;
;
Ⅱ.
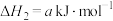 ;
;
Ⅲ.
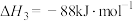 。
。
(1)
______ 。
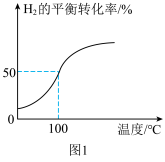
(2)将2.0 mol 和3.0mol
和3.0mol  通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得
通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得 的平衡转化率与温度的关系如图1所示。
的平衡转化率与温度的关系如图1所示。
①100℃时反应达到平衡所需的时间为5 min,则反应从起始至5 min内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为______  ;平衡后向容器中再通入3 mol Ar,平衡
;平衡后向容器中再通入3 mol Ar,平衡______ (填“正向”“逆向”或“不”)移动。
②100℃时,反应Ⅱ的平衡常数
______ 。
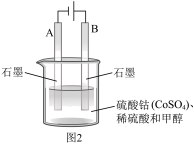
(3)甲醇会对水质造成一定的污染,有一种电化学法可消除这种污染,其原理如下:通电后,将 氧化成
氧化成 ,然后以
,然后以 作氧化剂,将水中的甲醇氧化成
作氧化剂,将水中的甲醇氧化成 而净化。实验室用如图2装置模拟上述过程。
而净化。实验室用如图2装置模拟上述过程。
①图2中石墨A的电极名称为______ ;写出阳极的电极反应式:______ 。
②写出除去甲醇的离子方程式:______ 。
 和
和 )在催化剂作用下可合成甲醇,发生的主要反应如下:
)在催化剂作用下可合成甲醇,发生的主要反应如下:Ⅰ.

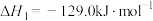 ;
;Ⅱ.

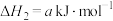 ;
;Ⅲ.

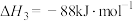 。
。(1)

(2)将2.0 mol
 和3.0mol
和3.0mol  通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得
通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得 的平衡转化率与温度的关系如图1所示。
的平衡转化率与温度的关系如图1所示。①100℃时反应达到平衡所需的时间为5 min,则反应从起始至5 min内,用
 表示该反应的平均反应速率为
表示该反应的平均反应速率为 ;平衡后向容器中再通入3 mol Ar,平衡
;平衡后向容器中再通入3 mol Ar,平衡②100℃时,反应Ⅱ的平衡常数



(3)甲醇会对水质造成一定的污染,有一种电化学法可消除这种污染,其原理如下:通电后,将
 氧化成
氧化成 ,然后以
,然后以 作氧化剂,将水中的甲醇氧化成
作氧化剂,将水中的甲醇氧化成 而净化。实验室用如图2装置模拟上述过程。
而净化。实验室用如图2装置模拟上述过程。①图2中石墨A的电极名称为
②写出除去甲醇的离子方程式:
您最近一年使用:0次
名校
7 . 对于可逆反应A(s)+3B(g) 2C(g)+2D(g),下列在不同条件下表示的反应速率中最快的是
2C(g)+2D(g),下列在不同条件下表示的反应速率中最快的是
| A.v(A)=0.5mol·L-1·min-1 | B.v(B)=0.2mol·L-1·s-1 |
| C.v(D)=0.4mol·L-1·min-1 | D.v(C)=0.2mol·L-1·s-1 |
您最近一年使用:0次
2023-10-11更新
|
192次组卷
|
3卷引用:陕西省榆林市第十中学2023-2024学年高二上学期12月月考化学试题
解题方法
8 . 合成氨是人类科学技术发展史上的一项重大突破。回答下列问题:
(1) 与
与 反应的能量变化如图所示,则反应
反应的能量变化如图所示,则反应 的
的 为
为___________ 。

(2)在773K时,分别将 和
和 充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中
充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中 、
、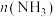 与反应时间t的关系如下表:
与反应时间t的关系如下表:
①该温度下,若向相同容积的另一容器中充入的 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 ,则此时
,则此时
___________ (填“>”“=”或“<”) 。
。
②由上表中的实验数据计算得到“浓度-时间”的关系可用图中的曲线表示,表示 的曲线是
的曲线是___________ (填“甲”“乙”或“丙”);在此温度下,若起始充入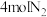 和
和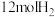 ,则反应刚达到平衡时,表示
,则反应刚达到平衡时,表示 的曲线上相应的点为
的曲线上相应的点为___________ (填字母)。

(3)T℃时,在2L恒容密闭容器中通入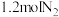 和
和 模拟一定条件下工业固氮[
模拟一定条件下工业固氮[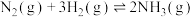 ],体系中
],体系中 随时间的变化如图。T℃时,该反应的平衡常数为
随时间的变化如图。T℃时,该反应的平衡常数为___________ 。

(4)合成氨反应中,正反应速率 ,逆反应速率
,逆反应速率 ,
, 、
、 为速率常数,只与温度有关。正反应和逆反应的平衡常数与温度的关系如图所示:
为速率常数,只与温度有关。正反应和逆反应的平衡常数与温度的关系如图所示:

①表示逆反应的平衡常数与温度变化关系的曲线为___________ (填“ ”或“
”或“ ”),理由为
”),理由为___________ 。
② ℃时,
℃时,
___________ 。
(5)以氨作为燃料的燃料电池,具有能量效率高的特点。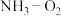 燃料电池的结构如图所示。负极的电极反应式为
燃料电池的结构如图所示。负极的电极反应式为___________ 。

(1)
 与
与 反应的能量变化如图所示,则反应
反应的能量变化如图所示,则反应 的
的 为
为
(2)在773K时,分别将
 和
和 充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中
充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中 、
、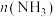 与反应时间t的关系如下表:
与反应时间t的关系如下表:| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
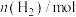 | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
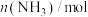 | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 ,则此时
,则此时
 。
。②由上表中的实验数据计算得到“浓度-时间”的关系可用图中的曲线表示,表示
 的曲线是
的曲线是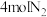 和
和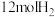 ,则反应刚达到平衡时,表示
,则反应刚达到平衡时,表示 的曲线上相应的点为
的曲线上相应的点为
(3)T℃时,在2L恒容密闭容器中通入
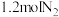 和
和 模拟一定条件下工业固氮[
模拟一定条件下工业固氮[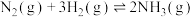 ],体系中
],体系中 随时间的变化如图。T℃时,该反应的平衡常数为
随时间的变化如图。T℃时,该反应的平衡常数为
(4)合成氨反应中,正反应速率
 ,逆反应速率
,逆反应速率 ,
, 、
、 为速率常数,只与温度有关。正反应和逆反应的平衡常数与温度的关系如图所示:
为速率常数,只与温度有关。正反应和逆反应的平衡常数与温度的关系如图所示:
①表示逆反应的平衡常数与温度变化关系的曲线为
 ”或“
”或“ ”),理由为
”),理由为②
 ℃时,
℃时,
(5)以氨作为燃料的燃料电池,具有能量效率高的特点。
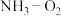 燃料电池的结构如图所示。负极的电极反应式为
燃料电池的结构如图所示。负极的电极反应式为
您最近一年使用:0次
名校
9 . 某校课外活动小组利用草酸( )溶液和酸性
)溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为
溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为 ,实验记录如表。
,实验记录如表。
回答下列问题:
(1)通过实验①、②可探究草酸浓度的改变对反应速率的影响,则
_______ ;通过实验_______ 可探究温度变化对化学反应速率的影响。由实验②③可推断
_______ (填“>”“<”或“=”)10s。
(2)若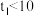 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是_______ ;利用实验②中数据,用 的浓度变化表示的反应平均速率为
的浓度变化表示的反应平均速率为_______  (保留2位有效数字)。
(保留2位有效数字)。
(3)某同学取1支试管加入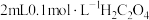 溶液,另取1支试管加入
溶液,另取1支试管加入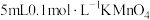 酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是
酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是_______ 。
(4)已知一定条件下40℃时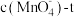 的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时
的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时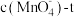 的变化曲线示意图
的变化曲线示意图_______ 。

 )溶液和酸性
)溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为
溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为 ,实验记录如表。
,实验记录如表。| 实验序号 | 实验温度/℃ |  溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | 溶液颜色褪至无色时所需时间/s | ||
| V/mL | 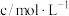 | V/mL | 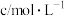 | V/mL | |||
| ① | 20 | 2 | 0.02 | 5 | 0.1 | 5 |  |
| ② | 20 | 2 | 0.02 | 4 | 0.1 |  | 10 |
| ③ | 40 | 2 | 0.02 | 4 | 0.1 | 6 |  |
(1)通过实验①、②可探究草酸浓度的改变对反应速率的影响,则


(2)若
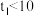 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应平均速率为
的浓度变化表示的反应平均速率为 (保留2位有效数字)。
(保留2位有效数字)。(3)某同学取1支试管加入
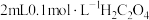 溶液,另取1支试管加入
溶液,另取1支试管加入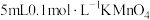 酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是
酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是(4)已知一定条件下40℃时
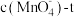 的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时
的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时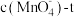 的变化曲线示意图
的变化曲线示意图
您最近一年使用:0次
2023-09-08更新
|
168次组卷
|
5卷引用:陕西省榆林市“府、靖、绥、横、定“五校联考2023-2024学年高二上学期11月期中化学试题
名校
10 . 在四个不同的容器中,在不同的条件下进行合成氨反应 ,根据下列在相同时间内测得的结果判断,生成氨的化学反应速率最快的是
,根据下列在相同时间内测得的结果判断,生成氨的化学反应速率最快的是
 ,根据下列在相同时间内测得的结果判断,生成氨的化学反应速率最快的是
,根据下列在相同时间内测得的结果判断,生成氨的化学反应速率最快的是A. | B. |
C. | D. |
您最近一年使用:0次
2023-07-16更新
|
177次组卷
|
4卷引用:陕西省榆林市2023-2024学年高二上学期10月月考化学试题



