1 . I.T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如(Ⅱ)所示:
(1)反应的化学方程式为___________ 。
(2)当反应达到平衡后升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量___________ (填“变大”、“变小”或“不变”)。
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(3)一般说化学平衡常数数值K___________ ,通常认为该反应进行较完全。
(4)该反应为___________ 反应(填“吸热”或“放热”)。
(5)能判断该反应是否达到化学平衡状态的依据是___________。
(6)某温度下,在2L的密闭容器中,加入1molCO2和1molH2充分反应达平衡时,CO平衡浓度为0.25mol/L,试判断此时的温度为___________ 。
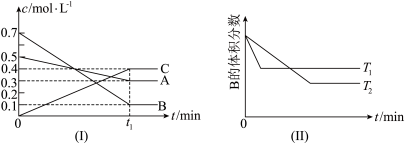
(1)反应的化学方程式为
(2)当反应达到平衡后升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)一般说化学平衡常数数值K
(4)该反应为
(5)能判断该反应是否达到化学平衡状态的依据是___________。
| A.v正(H2) = v逆(H2O) | B.反应停止,正、逆反应速率都等于零 |
| C.容器中压强不再发生变化 | D.混合气体中c(CO2)不变 |
(6)某温度下,在2L的密闭容器中,加入1molCO2和1molH2充分反应达平衡时,CO平衡浓度为0.25mol/L,试判断此时的温度为
您最近一年使用:0次
名校
解题方法
2 . t℃时,将1mol气体A和1mol气体B充入容积为2L的恒容密闭容器中,发生反应: ,测得4min时体系中有0.4molB和
,测得4min时体系中有0.4molB和 C。请回答下列问题:
C。请回答下列问题:
(1)
______ ,0~4min内用A(g)表示的平均反应速率为______  。
。
(2)下列表述能说明上述反应已经达到平衡状态的是______ (填字母)。
a.相同时间内,消耗A(g)和生成C(g)的物质的量之比为1:2
b.物质B(g)的质量分数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.混合气体的密度不再发生变化
(3)某化学兴趣小组的同学为了研究上述反应的反应速率,将A(g)、B(g)在一定条件下反应,测得C(g)的反应速率随时间的变化如图所示。______ (填“放热”或“吸热”)反应,后测得速率为0的原因是______ 。
(4)已知:1molA(g)、B(g)、C(g)中的化学键全部断裂形成气态原子所需要的能量如下表所示。
上述反应在6min时达到平衡,此时测得A的物质的量浓度为 。
。
①A的平衡转化率为______ ( )。
)。
②根据表中数据计算出该反应达到平衡过程中的能量变化为______ kJ(用含x、y、z的代数式表示)。
 ,测得4min时体系中有0.4molB和
,测得4min时体系中有0.4molB和 C。请回答下列问题:
C。请回答下列问题:(1)

 。
。(2)下列表述能说明上述反应已经达到平衡状态的是
a.相同时间内,消耗A(g)和生成C(g)的物质的量之比为1:2
b.物质B(g)的质量分数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.混合气体的密度不再发生变化
(3)某化学兴趣小组的同学为了研究上述反应的反应速率,将A(g)、B(g)在一定条件下反应,测得C(g)的反应速率随时间的变化如图所示。

(4)已知:1molA(g)、B(g)、C(g)中的化学键全部断裂形成气态原子所需要的能量如下表所示。
物质 | A | B | C |
能量/( | x | y | z |
 。
。①A的平衡转化率为
 )。
)。②根据表中数据计算出该反应达到平衡过程中的能量变化为
您最近一年使用:0次
名校
3 . 化学在生产生活中无处不在。
I.某汽车安全气囊的气体发生剂主要含有叠氮化钠(NaN3)、三氧化二铁(Fe2O3)、硝酸铵等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,是___________ (填“离子”或“共价”)化合物。
(2)汽车受到猛烈碰撞时,点火器点火引发NaN3迅速分解,生成氮气和金属钠,同时释放大量的热。下列关于该反应过程中的能量变化示意图正确的是___________ (填字母)。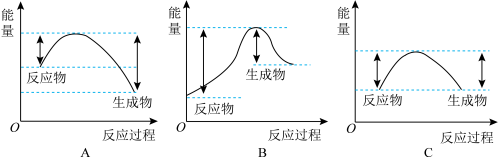
Ⅱ.CH4、CH3OH既是重要的化工原料,又是重要的能源物质。
(3)将2.0 mol CH4和4.0 mol H2O(g)通入容积为4 L的反应器,保持容器容积不变,在一定温度下发生反应CH4(g)+H2O(g) CO(g)+3H2(g),测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用H2表示该反应的平均反应速率为
CO(g)+3H2(g),测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用H2表示该反应的平均反应速率为___________ 。
(4)一定条件下,将1.0 mol CH4与2.0 mol H2O(g)充入密闭容器中发生反应CH4(g)+H2O(g) CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是
CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是___________ (填字母)。
a.恒容条件下充入He b.增大体积 c.升高温度 d.保持恒容投入更多的H2O(g) e.加入合适的催化剂
(5)用CH4设计燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为CH4+2O2+2KOH=K2CO3+3H2O。___________ (填“A”或“B”)电极入口通甲烷。
②当消耗甲烷的体积为33.6 L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为___________ 。
I.某汽车安全气囊的气体发生剂主要含有叠氮化钠(NaN3)、三氧化二铁(Fe2O3)、硝酸铵等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,是
(2)汽车受到猛烈碰撞时,点火器点火引发NaN3迅速分解,生成氮气和金属钠,同时释放大量的热。下列关于该反应过程中的能量变化示意图正确的是

Ⅱ.CH4、CH3OH既是重要的化工原料,又是重要的能源物质。
(3)将2.0 mol CH4和4.0 mol H2O(g)通入容积为4 L的反应器,保持容器容积不变,在一定温度下发生反应CH4(g)+H2O(g)
 CO(g)+3H2(g),测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用H2表示该反应的平均反应速率为
CO(g)+3H2(g),测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用H2表示该反应的平均反应速率为(4)一定条件下,将1.0 mol CH4与2.0 mol H2O(g)充入密闭容器中发生反应CH4(g)+H2O(g)
 CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是
CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是a.恒容条件下充入He b.增大体积 c.升高温度 d.保持恒容投入更多的H2O(g) e.加入合适的催化剂
(5)用CH4设计燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为CH4+2O2+2KOH=K2CO3+3H2O。
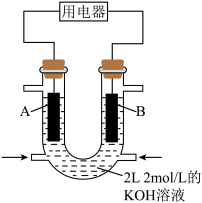
②当消耗甲烷的体积为33.6 L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为
您最近一年使用:0次
4 . 某科研团队利用 和
和 反应使之转化为水煤气,对争取2060年前实现“碳中和”、减缓燃料危机和减轻温室效应具有重要的意义。请回答下列问题:
反应使之转化为水煤气,对争取2060年前实现“碳中和”、减缓燃料危机和减轻温室效应具有重要的意义。请回答下列问题:
(1)已知:①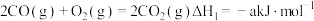
②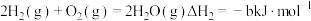
③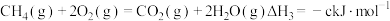
则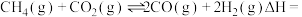
___________ (用含 的式子表示)。
的式子表示)。
(2) 均为
均为 的恒容密闭容器,向
的恒容密闭容器,向 容器中充入
容器中充入 和
和 ,向
,向 容器中充入
容器中充入 和
和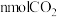 ,在催化剂存在下发生反应:
,在催化剂存在下发生反应: ,测得
,测得 的平衡转化率随温度的变化如图甲所示.
的平衡转化率随温度的变化如图甲所示.

① 容器中在温度为
容器中在温度为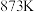 时,
时, 到达
到达 点,用
点,用 表示
表示 内的化学反应速率为
内的化学反应速率为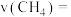
___________ ,此时的化学平衡常数 为
为___________ (保留两位小数),若在此温度下时向 容器的平衡体系中再充入
容器的平衡体系中再充入 各
各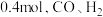 各
各 ,重新达到平衡前,
,重新达到平衡前,
___________  (填“
(填“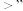 “
“ ”或
”或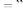 )。
)。
② 点时该反应的平衡常数为
点时该反应的平衡常数为 ,则
,则
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③ 两点处容器内气体总压强分别是
两点处容器内气体总压强分别是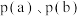 ,则
,则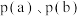 的大小顺序为
的大小顺序为___________ 。
(3)对于反应③: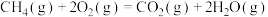 ,在使用不同催化剂时,相同时间内测得
,在使用不同催化剂时,相同时间内测得 的转化率随温度的变化如图乙所示.
的转化率随温度的变化如图乙所示.
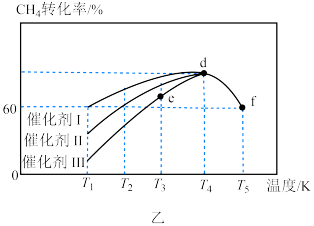
则催化效果最佳的是催化剂___________ (填“Ⅰ”“Ⅱ”或“Ⅲ”).如果 点已经达到平衡状态,则
点已经达到平衡状态,则 点的
点的
___________  (填“>”“<”或“=”),
(填“>”“<”或“=”), 点转化率比
点转化率比 点低的原因是
点低的原因是______________________ 。
 和
和 反应使之转化为水煤气,对争取2060年前实现“碳中和”、减缓燃料危机和减轻温室效应具有重要的意义。请回答下列问题:
反应使之转化为水煤气,对争取2060年前实现“碳中和”、减缓燃料危机和减轻温室效应具有重要的意义。请回答下列问题:(1)已知:①
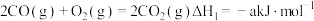
②
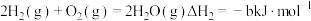
③
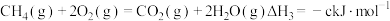
则
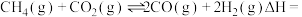
 的式子表示)。
的式子表示)。(2)
 均为
均为 的恒容密闭容器,向
的恒容密闭容器,向 容器中充入
容器中充入 和
和 ,向
,向 容器中充入
容器中充入 和
和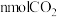 ,在催化剂存在下发生反应:
,在催化剂存在下发生反应: ,测得
,测得 的平衡转化率随温度的变化如图甲所示.
的平衡转化率随温度的变化如图甲所示.
①
 容器中在温度为
容器中在温度为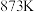 时,
时, 到达
到达 点,用
点,用 表示
表示 内的化学反应速率为
内的化学反应速率为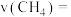
 为
为 容器的平衡体系中再充入
容器的平衡体系中再充入 各
各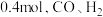 各
各 ,重新达到平衡前,
,重新达到平衡前,
 (填“
(填“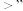 “
“ ”或
”或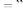 )。
)。②
 点时该反应的平衡常数为
点时该反应的平衡常数为 ,则
,则
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③
 两点处容器内气体总压强分别是
两点处容器内气体总压强分别是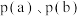 ,则
,则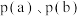 的大小顺序为
的大小顺序为(3)对于反应③:
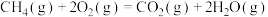 ,在使用不同催化剂时,相同时间内测得
,在使用不同催化剂时,相同时间内测得 的转化率随温度的变化如图乙所示.
的转化率随温度的变化如图乙所示.
则催化效果最佳的是催化剂
 点已经达到平衡状态,则
点已经达到平衡状态,则 点的
点的
 (填“>”“<”或“=”),
(填“>”“<”或“=”), 点转化率比
点转化率比 点低的原因是
点低的原因是
您最近一年使用:0次
名校
解题方法
5 . 工业上采用多种还原剂NH3、CO、H2等还原NO气体。
Ⅰ.NH3还原法。已知:
①
②
(1) 的逆反应活化能与正反应活化能之差等于
的逆反应活化能与正反应活化能之差等于_______ kJ/mol。
(2)在密闭容器中充入4 mol NH3和6 mol NO,发生反应: 。平衡时NO的体积分数与温度、压强的关系如图所示。
。平衡时NO的体积分数与温度、压强的关系如图所示。
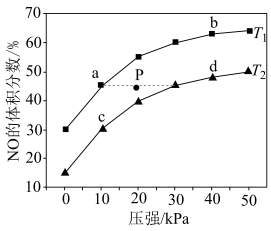
若P点对应的反应容器降温的同时扩大容器体积,重新达到平衡时可能是图中点a、b、c、d中的_______ 点。
Ⅱ.还原法。汽车尾气中的处理原理如图所示:
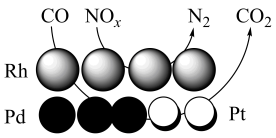
(3)当x=1时,CO和NOx反应中N2与NOx的速率之比为_______ 。其他条件相同,增大催化剂比表面积,反应速率_______ (填“增大”“减小”或“不变”)。
Ⅲ.H2还原法。在某催化剂作用下, 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关,m、n为反应级数)。
(k为速率常数,只与温度、催化剂有关,m、n为反应级数)。
(4)为了测定反应级数,测得实验数据如下:
由此推知,m=_______ ,n=_______ 。
(5)研究发现H2和NO反应分两步进行:第一步:2NO+H2=N2+H2O2 (很慢);第二步:_______ (补充反应式)(很快),其中,第_______ 步反应控制总反应速率。
(6)一定温度下,向恒容密闭反应器中充入0.4 mol NO和0.8 mol H2,发生反应: 。体系的总压强与时间的关系如图所示。
。体系的总压强与时间的关系如图所示。
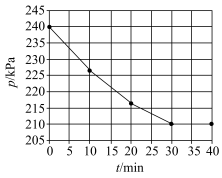
①0~30 min内用H2的分压表示的平均反应速率v(H2)为_______ kPa·min-1。
②该温度下,平衡常数Kp=_______ kPa-1 (Kp为用平衡分压计算的平衡常数,分压=总压×物质的量分数)。
Ⅰ.NH3还原法。已知:
①

②

(1)
 的逆反应活化能与正反应活化能之差等于
的逆反应活化能与正反应活化能之差等于(2)在密闭容器中充入4 mol NH3和6 mol NO,发生反应:
 。平衡时NO的体积分数与温度、压强的关系如图所示。
。平衡时NO的体积分数与温度、压强的关系如图所示。
若P点对应的反应容器降温的同时扩大容器体积,重新达到平衡时可能是图中点a、b、c、d中的
Ⅱ.还原法。汽车尾气中的处理原理如图所示:

(3)当x=1时,CO和NOx反应中N2与NOx的速率之比为
Ⅲ.H2还原法。在某催化剂作用下,
 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关,m、n为反应级数)。
(k为速率常数,只与温度、催化剂有关,m、n为反应级数)。(4)为了测定反应级数,测得实验数据如下:
| 实验 |  |  | 反应速率 |
| a | 0.1 | 0.1 | v |
| b | 0.2 | 0.1 | 2v |
| c | 0.2 | 0.2 | 8v |
(5)研究发现H2和NO反应分两步进行:第一步:2NO+H2=N2+H2O2 (很慢);第二步:
(6)一定温度下,向恒容密闭反应器中充入0.4 mol NO和0.8 mol H2,发生反应:
 。体系的总压强与时间的关系如图所示。
。体系的总压强与时间的关系如图所示。
①0~30 min内用H2的分压表示的平均反应速率v(H2)为
②该温度下,平衡常数Kp=
您最近一年使用:0次
2024-02-08更新
|
82次组卷
|
2卷引用:河南省南阳市六校2023-2024学年高二上学期1月期末联考化学试题
名校
6 . 已知有以下有机反应(图1)与反应装置(图2):
下列说法不正确的是

 |  | 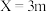 | 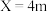 | 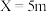 | 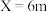 | 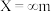 | |
| 物质A | 40% | 30% | 10% | 5% | 4% | 2% | 0% |
| 物质B | 40% | 30% | 10% | 5% | 4% | 2% | 0% |
| 物质C | 15% | 30% | 65% | 60% | 40% | 20% | 1% |
| 物质D | 5% | 10% | 15% | 30% | 52% | 76% | 99% |
| A.物质D相比于物质C在该反应中更稳定 |
| B.反应1的活化能小于反应2的活化能 |
C.增大B气流的流速,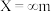 处 处 的比值不变 的比值不变 |
| D.若需提高物质C的产率,可将管道的出口设计相对更远 |
您最近一年使用:0次
2024-02-03更新
|
377次组卷
|
3卷引用:河南省南阳市邓州市第六高级中学校2023-2024学年高二下学期开学测试化学试题
河南省南阳市邓州市第六高级中学校2023-2024学年高二下学期开学测试化学试题 浙江省义乌中学2024届高三上学期首考适应性考试化学试题(已下线)专题06 化学反应速率与化学平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
名校
7 . 在工业生产中,常常在200℃~450℃的温度范围内,将氨气作为脱硝剂喷入高温烟气脱硝装置中,在催化剂的作用下将烟气中NOx分解成为N2和H2O,脱硝效率可以达到90%以上。请回答下列问题:
(1)在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应: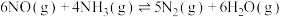
①不能说明该反应已达到平衡状态的是_______ (填标号)。
a.反应速率 b.1 mol N-H键断裂的同时生成1 mol O-H键
b.1 mol N-H键断裂的同时生成1 mol O-H键
c.容器内压强不再随时间而发生变化 d.容器内混合气体平均相对分子质量不再变化
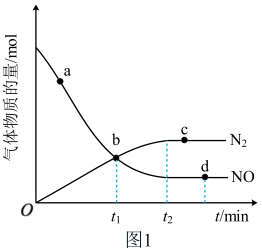
②某次实验中测得容器内NO及N2的物质的量随时间的变化如图1所示,图中b点对应的反应速率关系是
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)一定温度下,在2 L恒容密闭容器内发生反应 ,
,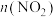 随时间的变化如表:
随时间的变化如表:
①根据表中数据可以看出,随着反应进行,反应速率逐渐减小,其原因是_______ 。
②该温度下,反应 的平衡常数
的平衡常数
_______  。
。
(3)对于反应 ,用平衡时各组分压强关系表达的平衡常数为
,用平衡时各组分压强关系表达的平衡常数为 。在一定条件下NO2与N2O4的消耗速率与自身压强间存在关系:
。在一定条件下NO2与N2O4的消耗速率与自身压强间存在关系: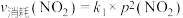 ,
,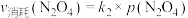 。其中
。其中 、
、 是与反应及温度有关的常数。相应的消耗速率跟压强的关系如图2所示,一定温度下,
是与反应及温度有关的常数。相应的消耗速率跟压强的关系如图2所示,一定温度下, 、
、 与平衡常数
与平衡常数 的关系是
的关系是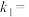
_______ 。在图中标出的点中,指出能表示反应达到平衡态的点_______ ,并请说明理由:_______ 。

(1)在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:
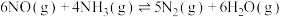
①不能说明该反应已达到平衡状态的是
a.反应速率
 b.1 mol N-H键断裂的同时生成1 mol O-H键
b.1 mol N-H键断裂的同时生成1 mol O-H键c.容器内压强不再随时间而发生变化 d.容器内混合气体平均相对分子质量不再变化
②某次实验中测得容器内NO及N2的物质的量随时间的变化如图1所示,图中b点对应的反应速率关系是

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)一定温度下,在2 L恒容密闭容器内发生反应
 ,
,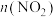 随时间的变化如表:
随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO2)/mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
②该温度下,反应
 的平衡常数
的平衡常数
 。
。(3)对于反应
 ,用平衡时各组分压强关系表达的平衡常数为
,用平衡时各组分压强关系表达的平衡常数为 。在一定条件下NO2与N2O4的消耗速率与自身压强间存在关系:
。在一定条件下NO2与N2O4的消耗速率与自身压强间存在关系: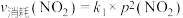 ,
,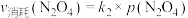 。其中
。其中 、
、 是与反应及温度有关的常数。相应的消耗速率跟压强的关系如图2所示,一定温度下,
是与反应及温度有关的常数。相应的消耗速率跟压强的关系如图2所示,一定温度下, 、
、 与平衡常数
与平衡常数 的关系是
的关系是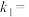

您最近一年使用:0次
2023-12-20更新
|
225次组卷
|
2卷引用:河南省南阳市第一中学校2023-2024学年高二上学期第三次月考化学试题
8 . 在3个容积均为 的密闭容器中分别放入
的密闭容器中分别放入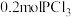 和
和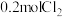 ,在不同条件下发生反应
,在不同条件下发生反应 。各容器内气体总压强随时间的变化如图所示。下列说法错误的是
。各容器内气体总压强随时间的变化如图所示。下列说法错误的是

 的密闭容器中分别放入
的密闭容器中分别放入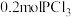 和
和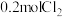 ,在不同条件下发生反应
,在不同条件下发生反应 。各容器内气体总压强随时间的变化如图所示。下列说法错误的是
。各容器内气体总压强随时间的变化如图所示。下列说法错误的是
A.实验a从反应开始至 的平均速率 的平均速率 |
| B.与实验a相比,实验b使用了催化剂,实验c是在较高温度下进行的 |
C.实验c中反应的平衡常数为 |
D.三组实验中反应的平衡转化率: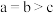 |
您最近一年使用:0次
名校
解题方法
9 . 体积恒定的 密闭容器中加入
密闭容器中加入 和
和 各
各 ,发生反应:
,发生反应: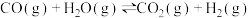
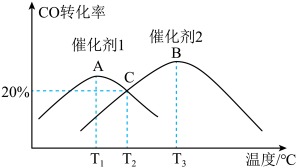
 ,反应分别在不同的温度和催化剂下进行,保持其他初始实验条件不变,经
,反应分别在不同的温度和催化剂下进行,保持其他初始实验条件不变,经 测得
测得 气体转化率如图所示,
气体转化率如图所示, 温度下两曲线相交,下列说法正确的是
温度下两曲线相交,下列说法正确的是
 密闭容器中加入
密闭容器中加入 和
和 各
各 ,发生反应:
,发生反应: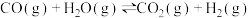
 ,反应分别在不同的温度和催化剂下进行,保持其他初始实验条件不变,经
,反应分别在不同的温度和催化剂下进行,保持其他初始实验条件不变,经 测得
测得 气体转化率如图所示,
气体转化率如图所示, 温度下两曲线相交,下列说法正确的是
温度下两曲线相交,下列说法正确的是
| A.在A点时,反应恰好达到平衡 |
| B.相同条件下,催化剂2比催化剂1的效率高 |
C.C点时,两种催化剂下反应速率相同,该化学反应速率为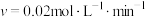 |
D.温度为 时,该反应平衡常数 时,该反应平衡常数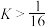 |
您最近一年使用:0次
2023-10-27更新
|
326次组卷
|
4卷引用:河南省南阳市第一中学校2023-2024学年高二上学期第二次月考化学试题
名校
解题方法
10 . 合成氨反应N2(g)+3H2(g) 2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。
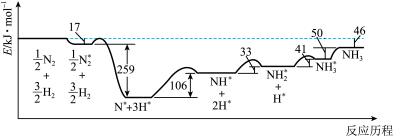
该历程中反应速率最慢的步骤的方程式为________ 。
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入 =3的混合气体,体系中各气体的含量与时间变化关系如图所示:
=3的混合气体,体系中各气体的含量与时间变化关系如图所示:

①以下叙述不能 说明该条件下反应达到平衡状态的是_________ (填字母)。
a.氨气的体积分数保持不变
b.容器中 保持不变
保持不变
c.气体平均相对分子质量保持不变
d.气体密度保持不变
e.3v(H2)=v(N2)
②反应20min时达到平衡,则0~20min内v(H2)=________ MPa•min-1,该反应的Kp=_______ MPa-2(保留小数点后两位)。(Kp为以分压表示的平衡常数)
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中_________ 点(填“d”“e”“f”或“g”)。
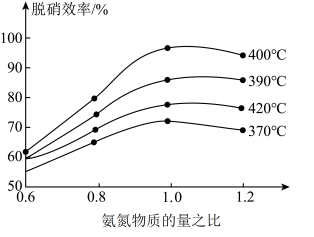
(3)氨化脱硝过程发生反应4NO(g)+4NH3(g)+O2(g)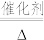 4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因_________ 。
(4)25℃用甲酸吸收氨气可得到HCOONH4溶液。已知:25℃时甲酸的Ka=1.75×10-5,NH3•H2O的Kb=2×10-5。则反应NH3•H2O+HCOOH HCOO-+NH
HCOO-+NH +H2O的平衡常数K=
+H2O的平衡常数K=________ 。
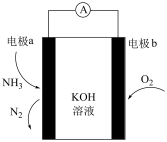
(5)化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图NH3如图。电极a上的电极反应式为:________ 。
 2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。
2NH3(g)是目前最有效的工业固氮方法,解决数亿人口生存问题。(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。

该历程中反应速率最慢的步骤的方程式为
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入
 =3的混合气体,体系中各气体的含量与时间变化关系如图所示:
=3的混合气体,体系中各气体的含量与时间变化关系如图所示:
①以下叙述
a.氨气的体积分数保持不变
b.容器中
 保持不变
保持不变c.气体平均相对分子质量保持不变
d.气体密度保持不变
e.3v(H2)=v(N2)
②反应20min时达到平衡,则0~20min内v(H2)=
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中
(3)氨化脱硝过程发生反应4NO(g)+4NH3(g)+O2(g)
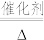 4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
4N2(g)+6H2O(g) △H<0,分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
(4)25℃用甲酸吸收氨气可得到HCOONH4溶液。已知:25℃时甲酸的Ka=1.75×10-5,NH3•H2O的Kb=2×10-5。则反应NH3•H2O+HCOOH
 HCOO-+NH
HCOO-+NH +H2O的平衡常数K=
+H2O的平衡常数K=(5)化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图NH3如图。电极a上的电极反应式为:

您最近一年使用:0次
2023-10-17更新
|
209次组卷
|
3卷引用:河南省南阳市第一中学校2023-2024学年高三上学期第三次月考化学试题

 )
)

