解题方法
1 . Ⅰ.某同学做如图实验(如图),以检验反应中的能量变化。

(1)实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是_______ 热反应;该反应中_______ 能转化成_______ 能。
(2)图1所示实验中,能正确表示实验(b)涉及的化学反应的能量变化关系的是_______ 。
Ⅱ.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图:
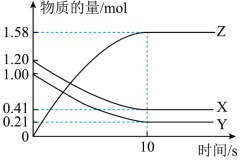
(3)反应开始到10s,用Z表示的反应速率为_______ mol/(L•s)。
(4)反应开始到10s时,Y的物质的量浓度减少了_______ mol/L。
(5)反应的化学方程式为_______ 。

(1)实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是
(2)图1所示实验中,能正确表示实验(b)涉及的化学反应的能量变化关系的是
A.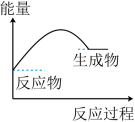 | B.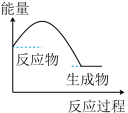 |
C. | D. |
Ⅱ.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图:

(3)反应开始到10s,用Z表示的反应速率为
(4)反应开始到10s时,Y的物质的量浓度减少了
(5)反应的化学方程式为
您最近一年使用:0次
2 . N2O俗名:笑气,曾被用作麻醉剂。回答下列问题:
(1)N2O分子与下列粒子所含原子总数和电子总数均相等的是___________(填字母)。
(2)在稀硝酸中加入镁粉会放出笑气,写出该反应的离子方程式:___________ 。
(3)一定温度下,N2O在金箔表面分解生成N2和O2,c(N2O)与金箔面积,时间的关系如图1所示。

①根据直线Ⅰ、Ⅱ可得出的结论是___________ 。
②在Ⅱ条件下,50 min内N2O分解速率为___________ mol·L-1·min-1。
(4)体积相等的甲、乙密闭容器中分别充入1 mol CO和1 mol N2O,在“恒温恒容”、“绝热恒容”条件下发生反应:N2O(g)+CO(g) N2(g)+CO2(g) △H<0,测得压强与时间的关系如图2所示。
N2(g)+CO2(g) △H<0,测得压强与时间的关系如图2所示。

①在“绝热恒容”条件下反应的容器是___________ (填“甲”或“乙”),判断依据是___________ 。
②一定达到平衡状态的点是___________ (填“a”或“b”),判断依据是_____________________ 。
(1)N2O分子与下列粒子所含原子总数和电子总数均相等的是___________(填字母)。
| A.CO2 | B.SCN- | C.CNO- | D.C2H4 |
(2)在稀硝酸中加入镁粉会放出笑气,写出该反应的离子方程式:
(3)一定温度下,N2O在金箔表面分解生成N2和O2,c(N2O)与金箔面积,时间的关系如图1所示。

①根据直线Ⅰ、Ⅱ可得出的结论是
②在Ⅱ条件下,50 min内N2O分解速率为
(4)体积相等的甲、乙密闭容器中分别充入1 mol CO和1 mol N2O,在“恒温恒容”、“绝热恒容”条件下发生反应:N2O(g)+CO(g)
 N2(g)+CO2(g) △H<0,测得压强与时间的关系如图2所示。
N2(g)+CO2(g) △H<0,测得压强与时间的关系如图2所示。
①在“绝热恒容”条件下反应的容器是
②一定达到平衡状态的点是
您最近一年使用:0次
解题方法
3 . 一定温度下,向2L密闭容器中加入 ,发生反应
,发生反应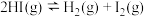 物质的量随时间的变化如图所示。
物质的量随时间的变化如图所示。

(1)0~2min内的平均反应速率
___________ ,该温度下, 的平衡常数K=
的平衡常数K=___________ 。
(2)相同温度下,若开始加入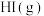 的物质的量是原来的2倍,则
的物质的量是原来的2倍,则___________ 是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时 的体积分数
的体积分数
(3)在 反应中,正反应速率为
反应中,正反应速率为 ,逆反应速率为
,逆反应速率为 。其中
。其中 、
、 为速率常数,则
为速率常数,则
___________ (以K和 表示)。
表示)。
(4)实验室用Zn和稀硫酸制取 ,加入少量下列试剂中的
,加入少量下列试剂中的___________ ,产生 的速率将增大。
的速率将增大。
a. b.
b. c.
c. d.
d.
(5)氢气用于工业合成氨;
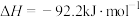 ,一定温度下,在容积恒定的密闭容器中,一定量的
,一定温度下,在容积恒定的密闭容器中,一定量的 和
和 反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示。
反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示。

其中 时刻所对应的实验条件改变是
时刻所对应的实验条件改变是___________ ,平衡常数最大的时间段是___________ 。
 ,发生反应
,发生反应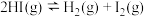 物质的量随时间的变化如图所示。
物质的量随时间的变化如图所示。
(1)0~2min内的平均反应速率

 的平衡常数K=
的平衡常数K=(2)相同温度下,若开始加入
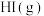 的物质的量是原来的2倍,则
的物质的量是原来的2倍,则a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时
 的体积分数
的体积分数(3)在
 反应中,正反应速率为
反应中,正反应速率为 ,逆反应速率为
,逆反应速率为 。其中
。其中 、
、 为速率常数,则
为速率常数,则
 表示)。
表示)。(4)实验室用Zn和稀硫酸制取
 ,加入少量下列试剂中的
,加入少量下列试剂中的 的速率将增大。
的速率将增大。a.
 b.
b. c.
c. d.
d.
(5)氢气用于工业合成氨;

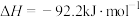 ,一定温度下,在容积恒定的密闭容器中,一定量的
,一定温度下,在容积恒定的密闭容器中,一定量的 和
和 反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示。
反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示。
其中
 时刻所对应的实验条件改变是
时刻所对应的实验条件改变是
您最近一年使用:0次
名校
解题方法
4 . 在容积不变的密闭容器中,M与N反应生成W,其化学反应速率分别用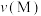 、
、 、
、 表示。已知:
表示。已知: ,
, ,则此反应可表示为
,则此反应可表示为
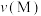 、
、 、
、 表示。已知:
表示。已知: ,
, ,则此反应可表示为
,则此反应可表示为A. | B. |
C. | D. |
您最近一年使用:0次
2023-11-11更新
|
266次组卷
|
4卷引用:河南省开封市2023-2024学年高二上学期11月期中考试化学试题
名校
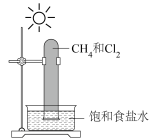
5 . 用下列装置进行实验,实验装置正确且能达到相应实验目的的是
|
|
| 甲 | 乙 |
|
|
| 丙 | 丁 |
| A.用装置甲探究甲烷的取代反应 |
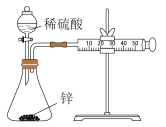
| B.用装置乙测定锌与稀硫酸反应生成氢气的速率 |
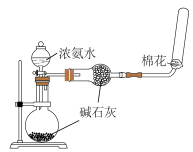
| C.用装置丙制备并收集氨气 |
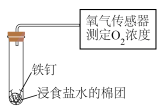
| D.用装置丁验证铁钉的吸氧腐蚀 |
您最近一年使用:0次
2023-11-08更新
|
104次组卷
|
2卷引用:河南省周口市项城市2023-2024学年高三上学期11月期中联考化学试题
名校
6 .  可用于合成甲醇,化学方程式为
可用于合成甲醇,化学方程式为 。
。
(1)在不同温度下 的转化率随时间变化的曲线如图:
的转化率随时间变化的曲线如图:
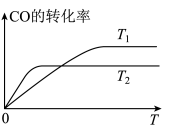
反应 的
的
___________ (填“>”、“<”或“=”,下同)0,由图判断T1___________ T2,平衡常数K的大小关系:
___________  。
。
(2)在T1温度下,向容积为2L的恒容密闭容器中充入2mol 和amol
和amol ,实验测得
,实验测得 和
和 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:
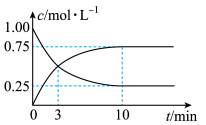
在T1温度下,0~10min内,H2(g)的平均反应速率为___________ mol⋅L-1⋅min-1,3min时CO(g)的转化率为___________ ;若T1温度下的平衡常数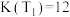 ,则a=
,则a=___________ 。
(3)在容积为10L的恒容密闭容器中,研究在三种不同温度(210℃、230℃和250℃)下 合成甲醇的规律。这三种不同温度下
合成甲醇的规律。这三种不同温度下 和
和 的起始投料比与
的起始投料比与 平衡转化率的关系如图[已知:起始时
平衡转化率的关系如图[已知:起始时 的物质的量均为1mol]:
的物质的量均为1mol]:
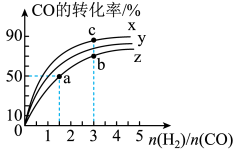
曲线x对应的温度是___________ ℃;曲线z对应温度下,上述反应的化学平衡常数K=___________ 。
 可用于合成甲醇,化学方程式为
可用于合成甲醇,化学方程式为 。
。(1)在不同温度下
 的转化率随时间变化的曲线如图:
的转化率随时间变化的曲线如图:
反应
 的
的

 。
。(2)在T1温度下,向容积为2L的恒容密闭容器中充入2mol
 和amol
和amol ,实验测得
,实验测得 和
和 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:
在T1温度下,0~10min内,H2(g)的平均反应速率为
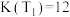 ,则a=
,则a=(3)在容积为10L的恒容密闭容器中,研究在三种不同温度(210℃、230℃和250℃)下
 合成甲醇的规律。这三种不同温度下
合成甲醇的规律。这三种不同温度下 和
和 的起始投料比与
的起始投料比与 平衡转化率的关系如图[已知:起始时
平衡转化率的关系如图[已知:起始时 的物质的量均为1mol]:
的物质的量均为1mol]:
曲线x对应的温度是
您最近一年使用:0次
2023-11-08更新
|
276次组卷
|
4卷引用:河南省部分名校2023-2024学年高二上学期11月期中考试化学试题
名校
7 . 一定温度下,10mL0.8
 溶液发生催化分解。不同时刻测得生成的
溶液发生催化分解。不同时刻测得生成的 的体积(已折算为标准状况下)如表。
的体积(已折算为标准状况下)如表。
下列叙述正确的是(溶液体积变化忽略不计)

 溶液发生催化分解。不同时刻测得生成的
溶液发生催化分解。不同时刻测得生成的 的体积(已折算为标准状况下)如表。
的体积(已折算为标准状况下)如表。| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
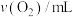 | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
A.反应到6min时,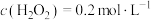 |
| B.第4min时的瞬时速率小于第6min时的瞬时速率 |
C.反应至6min时, 分解率为50% 分解率为50% |
D.0~6min的平均反应速率: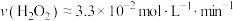 |
您最近一年使用:0次
2023-11-05更新
|
217次组卷
|
4卷引用:河南省新乡市原阳县第一高级中学2023-2024学年高一下学期4月月考化学试题
河南省新乡市原阳县第一高级中学2023-2024学年高一下学期4月月考化学试题甘肃省酒泉市四校联考2023-2024学年高二上学期11月期中化学试题甘肃省定西市临洮中学2023-2024学年高二上学期期中考试化学试题(已下线)期中测试卷一【测试范围:第五、六章】-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
8 . 某研究性学习小组探究影响反应速率的因素及反应速率的大小,测得的实验数据如表所示(忽略溶液体积变化),下列说法错误的是
| 组号 | 反应温度/℃ | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 10 | 2 | 0.1 | 1 | 0.4 | 3 |
| ② | 30 | 2 | 0.1 | 2 | 0.2 | 2 |
| ③ | 30 | 1 | 0.2 | 2 | 0.1 | 3 |
| ④ | 30 | 1 | 0.1 | 2 | 0.1 | 3 |
| A.实验①②探究温度对反应速率的影响 |
| B.实验②④探究Na2S2O3浓度对反应速率的影响 |
| C.四组实验中实验②的反应速率最大 |
D.实验③完全反应需要tmin,平均反应速率v(Na2S2O3)= mol/(L•min) mol/(L•min) |
您最近一年使用:0次
2023-11-03更新
|
493次组卷
|
5卷引用:河南省普高联考2023-2024学年高三上学期测评(三)化学试题
河南省普高联考2023-2024学年高三上学期测评(三)化学试题【精品卷】2.1.2 影响化学反应速率的因素课堂例题-人教版2023-2024学年选择性必修1【定心卷】2.1.2 影响化学反应速率的因素随堂练习-人教版2023-2024学年选择性必修1(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)通关练08 聚焦反应热、速率及化学平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
9 . 我国科学家团队打通了温和条件下草酸二甲酯【(COOCH3)2】催化加氢制乙二醇的技术难关,反应为 。如图所示,在恒容密闭容器中,反应温度为T1时,c(HOCH2CH2OH)和c(H2)随时间t的变化分别为曲线I和Ⅱ,反应温度为T2时,c(H2)随时间t的变化为曲线Ⅲ。下列判断正确的是
。如图所示,在恒容密闭容器中,反应温度为T1时,c(HOCH2CH2OH)和c(H2)随时间t的变化分别为曲线I和Ⅱ,反应温度为T2时,c(H2)随时间t的变化为曲线Ⅲ。下列判断正确的是

 。如图所示,在恒容密闭容器中,反应温度为T1时,c(HOCH2CH2OH)和c(H2)随时间t的变化分别为曲线I和Ⅱ,反应温度为T2时,c(H2)随时间t的变化为曲线Ⅲ。下列判断正确的是
。如图所示,在恒容密闭容器中,反应温度为T1时,c(HOCH2CH2OH)和c(H2)随时间t的变化分别为曲线I和Ⅱ,反应温度为T2时,c(H2)随时间t的变化为曲线Ⅲ。下列判断正确的是
| A.ΔH>0 |
| B.a、b两时刻生成乙二醇的速率:v(a)=v(b) |
C.在T2温度下,反应在0~t2内的平均速率为 |
| D.其他条件相同,在T1温度下,起始时向该容器中充入一定量的氮气,则反应达到平衡的时间小于t1 |
您最近一年使用:0次
2023-11-01更新
|
1432次组卷
|
6卷引用:河南省信阳高级中学2023-2024学年高三上学期11月一模考试化学试题
河南省信阳高级中学2023-2024学年高三上学期11月一模考试化学试题广东省湛江市2024届高三上学期毕业班调研考试化学试题2024届广东省湛江市普通高中毕业班调研测试化学试题(已下线)题型04 化学反应速率与平衡图像分析-2024年高考化学答题技巧与模板构建(已下线)选择题6-10(已下线)专题06 化学反应速率与化学平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
解题方法
10 . 二甲醚(CH3OCH3)常用作溶剂、冷冻剂、喷雾剂等,易燃烧。 回答下列问题:
(1)25 ℃、101 kPa时,92g气态二甲醚完全燃烧生成CO2(g)、H2O(l)放出 2912 kJ热量,则表示气态二甲醚燃烧 热的热化学方程式为___________ 。当 CH3OCH3(g)完全燃烧生成 CO2(g)、H2O(l)放出 728 kJ热量时,转移的电子数为___________ (用NA 表示阿伏加德罗常数的值)。
(2)已知 H2(g)和CO(g)的燃烧热 △H 分别是
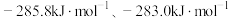
 则反应
则反应
 的反应热△H =
的反应热△H =___________
 。
。
(3)在 2 L 的恒容密闭容器中,充入 6 mol H2 和2 mol CO2合成二甲醚,其反应为
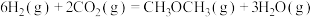 ,在不同温度下,5min时,水蒸气的体积分数如图所示。
,在不同温度下,5min时,水蒸气的体积分数如图所示。
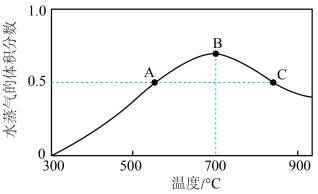
①该反应的 △H=___________ 0(填“>”“<”或“=”)。
②A 点 CO2的逆反应速率___________ (填“>”“<”或“=”)B点 CO2 的逆反应速率;A点对应温度下,0 ~ 5 min 内,平均反应速率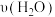 =
=____________ 。
③B点的平衡常数___________ (填“>”“<”或“=”)C点的平衡常数。
(1)25 ℃、101 kPa时,92g气态二甲醚完全燃烧生成CO2(g)、H2O(l)放出 2912 kJ热量,则表示气态二甲醚燃
(2)已知 H2(g)和CO(g)的燃烧热 △H 分别是
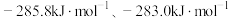
 则反应
则反应 的反应热△H =
的反应热△H = 。
。(3)在 2 L 的恒容密闭容器中,充入 6 mol H2 和2 mol CO2合成二甲醚,其反应为
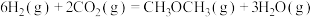 ,在不同温度下,5min时,水蒸气的体积分数如图所示。
,在不同温度下,5min时,水蒸气的体积分数如图所示。
①该反应的 △H=
②A 点 CO2的逆反应速率
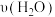 =
=③B点的平衡常数
您最近一年使用:0次