1 . 铵盐是大气气溶胶中的一种组分,其中存在反应而消耗铵盐: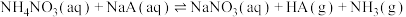 ,已知:
,已知: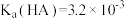 ,
,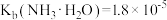 。下列说法错误的是
。下列说法错误的是
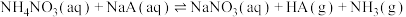 ,已知:
,已知: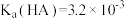 ,
,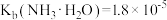 。下列说法错误的是
。下列说法错误的是A.该反应的 |
| B.气溶胶可产生丁达尔效应 |
C.同浓度溶液的碱性强弱: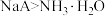 |
| D.大气中铵盐的形成与自然固氮有关 |
您最近一年使用:0次
名校
2 . 对于反应4HCl(g)+O2(g) 2Cl2(g)+2H2O(g),下列说法正确的是
2Cl2(g)+2H2O(g),下列说法正确的是
 2Cl2(g)+2H2O(g),下列说法正确的是
2Cl2(g)+2H2O(g),下列说法正确的是| A.该反应△S>0 |
| B.使用催化剂能降低该反应的△H |
| C.反应中每消耗1molO2转移电子数约为4×6.02×1023 |
D.反应的平衡常数为K=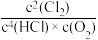 |
您最近一年使用:0次
2022-04-09更新
|
742次组卷
|
9卷引用:湖北省武汉市第十一中学2023-2024学年高三上学期10月月考化学试题
湖北省武汉市第十一中学2023-2024学年高三上学期10月月考化学试题天津市和平区2022届高三一模化学试题(已下线)三轮冲刺卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)(已下线)第22讲 化学平衡常数及转化率的计算(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)T3-物质反应及转化(已下线)选择题6-10(已下线)选择题1-5江苏省苏州市实验中学2023-2024学年高二上学期10月月考化学试题黑龙江省哈尔滨市第三中学校2023-2024学年高二上学期期中考试化学试题
名校
3 . 以下说法中正确的是
A.已知: 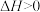 ,则该反应在任何条件都可以自发进行 ,则该反应在任何条件都可以自发进行 |
| B.对于有气体参加的可逆反应,加压可增大单位体积活化分子百分数,从而加快反应速率 |
| C.冰在室温下自动融化成水,是熵增的重要结果 |
| D.吸热反应都必须加热才能发生 |
您最近一年使用:0次
2021-12-09更新
|
401次组卷
|
4卷引用:湖北省武汉市新洲区第一中学2024届高二上学期12月诊断测试化学试题
湖北省武汉市新洲区第一中学2024届高二上学期12月诊断测试化学试题重庆市育才中学2021-2022学年度高二上学期期中测试化学试题重庆市万州第二高级中学2020-2021学年高二上学期期末考试化学试题(已下线)寒假作业04 化学反应的方向及调控-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
4 . 研究CO、CO2的转化既可减少碳排放,又可获得许多实用的含碳物质。回答下列问题:
(1)以CO2、H2为原料,在铜基催化剂作用下可合成甲醇,反应如下(不考虑副反应):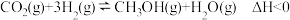 ,反应在恒容密闭容器中进行。反应时间一定,甲醇的产率随温度的变化如图所示(不考虑此过程中催化剂活性的变化)。
,反应在恒容密闭容器中进行。反应时间一定,甲醇的产率随温度的变化如图所示(不考虑此过程中催化剂活性的变化)。
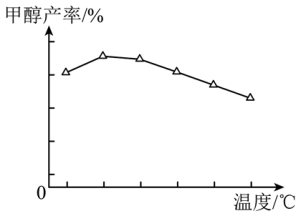
①该反应自发进行的条件是___________ (填“高温”“低温”或“任意温度”)。
②甲醇产率随温度升高先增大后减小的原因是___________ 。
(2)以CO、H2为原料在一定条件下也可合成甲醇,发生的反应如下:
主反应:
副反应:
一定条件下,向体积为V L的恒容密闭容器中投入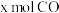 和
和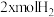 ,发生上述反应,平衡时容器内CH3OH的物质的量为
,发生上述反应,平衡时容器内CH3OH的物质的量为 ,C的物质的量为
,C的物质的量为 。则主反应的平衡常数K=
。则主反应的平衡常数K=___________ 。
(3)我国科学家设计 熔盐捕获与转化装置如图所示:
熔盐捕获与转化装置如图所示:
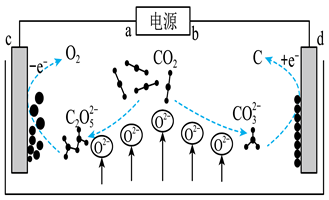
①d极的电极反应式为___________ 。
②若电源使用铅蓄电池,当电路中转移2 mol电子时,Pb电极的质量理论上___________ (填“增加”或“减少”)了____ g。
(4)水煤气变换是重要的化工过程,反应为: 。已知该反应的平衡常数K与热力学温度T的关系为
。已知该反应的平衡常数K与热力学温度T的关系为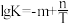 (m、n均为正数)。
(m、n均为正数)。
①水煤气变换是____ (填“吸热”或“放热”)反应。
②热力学温度为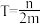 时,在恒温密闭容器中将等物质的量的CO和H2O(g)混合,选择适当的催化剂进行反应。平衡时体系中H2的物质的量分数为
时,在恒温密闭容器中将等物质的量的CO和H2O(g)混合,选择适当的催化剂进行反应。平衡时体系中H2的物质的量分数为 ,则
,则____ (填标号)。
A.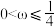 B.
B.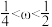 C.
C.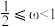
(1)以CO2、H2为原料,在铜基催化剂作用下可合成甲醇,反应如下(不考虑副反应):
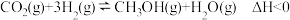 ,反应在恒容密闭容器中进行。反应时间一定,甲醇的产率随温度的变化如图所示(不考虑此过程中催化剂活性的变化)。
,反应在恒容密闭容器中进行。反应时间一定,甲醇的产率随温度的变化如图所示(不考虑此过程中催化剂活性的变化)。
①该反应自发进行的条件是
②甲醇产率随温度升高先增大后减小的原因是
(2)以CO、H2为原料在一定条件下也可合成甲醇,发生的反应如下:
主反应:

副反应:

一定条件下,向体积为V L的恒容密闭容器中投入
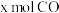 和
和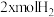 ,发生上述反应,平衡时容器内CH3OH的物质的量为
,发生上述反应,平衡时容器内CH3OH的物质的量为 ,C的物质的量为
,C的物质的量为 。则主反应的平衡常数K=
。则主反应的平衡常数K=(3)我国科学家设计
 熔盐捕获与转化装置如图所示:
熔盐捕获与转化装置如图所示:
①d极的电极反应式为
②若电源使用铅蓄电池,当电路中转移2 mol电子时,Pb电极的质量理论上
(4)水煤气变换是重要的化工过程,反应为:
 。已知该反应的平衡常数K与热力学温度T的关系为
。已知该反应的平衡常数K与热力学温度T的关系为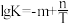 (m、n均为正数)。
(m、n均为正数)。①水煤气变换是
②热力学温度为
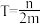 时,在恒温密闭容器中将等物质的量的CO和H2O(g)混合,选择适当的催化剂进行反应。平衡时体系中H2的物质的量分数为
时,在恒温密闭容器中将等物质的量的CO和H2O(g)混合,选择适当的催化剂进行反应。平衡时体系中H2的物质的量分数为 ,则
,则A.
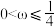 B.
B.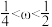 C.
C.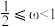
您最近一年使用:0次
5 . 下列有关说法正确的是
①太阳光催化分解水制氢:2H2O(g)=2H2(g)+O2(g) ΔH1=+571.6kJ/mol
②碳的“气化”:C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3kJ/mol
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH3=+206.1kJ/mol
①太阳光催化分解水制氢:2H2O(g)=2H2(g)+O2(g) ΔH1=+571.6kJ/mol
②碳的“气化”:C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3kJ/mol
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH3=+206.1kJ/mol
| A.由反应①可知H2的燃烧热为571.6kJ/mol |
| B.碳的“气化”反应过程熵不变 |
| C.甲烷与水反应制氢过程中使用催化剂,反应的活化能Ea、ΔH3都减小 |
D.反应CH4(g)+  O2(g)=CO(g)+2H2(g)的ΔH4=-79.7kJ/mol O2(g)=CO(g)+2H2(g)的ΔH4=-79.7kJ/mol |
您最近一年使用:0次
2021-10-25更新
|
188次组卷
|
2卷引用:湖北省武汉市部分学校2021-2022学年高二上学期12月联考化学试题
名校
6 . 工业上用催化氧化法制取SO3,再用浓硫酸吸收SO3得到发烟硫酸(H2SO4·SO3),发烟硫酸加水可以得到浓硫酸。催化氧化法制取SO3的反应为:2SO2(g)+O2(g)⇌2SO3(g) 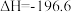 kJ·mol-1,下列关于工业上制取浓硫酸的说法正确的是
kJ·mol-1,下列关于工业上制取浓硫酸的说法正确的是
 kJ·mol-1,下列关于工业上制取浓硫酸的说法正确的是
kJ·mol-1,下列关于工业上制取浓硫酸的说法正确的是| A.2molSO2(g)和1molO2(g)所含化学键的键能总和比2molSO3(g)大196.6kJ·mol-1 |
| B.催化氧化法制取SO3能够自发进行的原因是∆S>0 |
| C.工业上用浓硫酸吸收SO3时是将SO3从吸收塔底部通入,浓硫酸从塔顶喷淋下来,这样操作的目的是为了提高SO3的吸收率 |
| D.将1molH2SO4·SO3全部转化为H2SO4需消耗水2mol |
您最近一年使用:0次
名校
7 . 下列说法中正确的是
| A.2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g)在低温下能自发进行,则该反应的ΔH<0 |
| B.NH4Cl(s)= NH3(g)+HCl(g)在室温下不能自发进行,则该反应的ΔH<0 |
| C.若ΔH>0,ΔS<0,化学反应在任何温度下都能自发进行 |
| D.加入合适的催化剂能降低反应的活化能,从而改变反应的焓变 |
您最近一年使用:0次
2021-10-11更新
|
532次组卷
|
8卷引用:湖北省武汉市江夏实验高级中学2021-2022学年高二上学期10月考试化学试题
湖北省武汉市江夏实验高级中学2021-2022学年高二上学期10月考试化学试题安徽省宿州市砀山中学2021-2022学年高二上学期第一次质量检测化学试题(已下线)必考点04 化学反应的方向和调控-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)山东省泰安第二中学2021-2022学年高二上学期期中考试化学试题甘肃省永昌县第一高级中学2020-2021学年高二上学期期中考试化学(理)试题陕西省西安市蓝田县2022-2023学年高二上学期期末考试化学试题广西南宁第二十六中2023-2024学年高二上学期第一次月考化学试题内蒙古赤峰学院附属中学2023-2024学年高二上学期12月期中考试化学试题
名校
8 . 二甲醚是一种重要的化工原料,回答下列问题:
(1)已知:①C(s)+ O2(g)=CO(g) ∆H1=-111. 8 kJ/mol;
O2(g)=CO(g) ∆H1=-111. 8 kJ/mol;
②C(s)+ H2O(g)=CO(g) +H2(g) ∆H2 =130 kJ/mol;
③CO(g)+ 2H2(g)=CH3OH(g) ∆H3=- 90.1 kJ/mol;
④2CH3OH(g)=CH3OCH3(g)+H2O(g) ∆H4= -134 kJ/mol。
则CH3OCH3(g)+ O2 (g)=2CO(g)+3H2(g) ∆H=
O2 (g)=2CO(g)+3H2(g) ∆H=______ kJ/mol;该反应能够自发进行所采用的有利条件是______ (填“高温”“低温”或“任意温度”)。
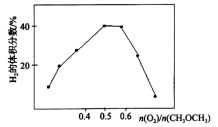
(2)在恒温恒压条件下,化工生产上利用二甲醚与氧气为原料制备合成气,实际生产过程中常常添加一定量的水蒸气,其目的是______ ;研究发现,所得平衡混合气体中H2的体积分数随n(O2)/n(CH3OCH3)变化如图所示,试解释该曲线先变大后减小的原因______ 。
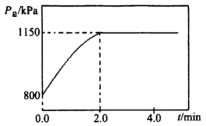
(3)某温度下,在VL的刚性容器中充入4.0molCH3OCH3、2.0molO2及2.0molH2O(g),在催化剂作用下仅发生反应CH3OCH3(g)+ O2(g)
O2(g) 2CO(g)+3H2(g),实验测得容器中压强与时间变化如图所示。则前2.0min内该反应速率v(CH3OCH3)=
2CO(g)+3H2(g),实验测得容器中压强与时间变化如图所示。则前2.0min内该反应速率v(CH3OCH3)=______ mol·min-1;该温度下其分压平衡常数Kp=______ (kPa)3.5(已知 =12.2)。
=12.2)。
(4)二甲醚燃料电池常采用磺酸类质子溶剂,其工作原理如图所示,则负极的电极反应式为______ ,若消耗标准状况下5.6LO2,则理论上左右两室溶液质量变化的差为______ g。

(1)已知:①C(s)+
 O2(g)=CO(g) ∆H1=-111. 8 kJ/mol;
O2(g)=CO(g) ∆H1=-111. 8 kJ/mol;②C(s)+ H2O(g)=CO(g) +H2(g) ∆H2 =130 kJ/mol;
③CO(g)+ 2H2(g)=CH3OH(g) ∆H3=- 90.1 kJ/mol;
④2CH3OH(g)=CH3OCH3(g)+H2O(g) ∆H4= -134 kJ/mol。
则CH3OCH3(g)+
 O2 (g)=2CO(g)+3H2(g) ∆H=
O2 (g)=2CO(g)+3H2(g) ∆H=(2)在恒温恒压条件下,化工生产上利用二甲醚与氧气为原料制备合成气,实际生产过程中常常添加一定量的水蒸气,其目的是

(3)某温度下,在VL的刚性容器中充入4.0molCH3OCH3、2.0molO2及2.0molH2O(g),在催化剂作用下仅发生反应CH3OCH3(g)+
 O2(g)
O2(g) 2CO(g)+3H2(g),实验测得容器中压强与时间变化如图所示。则前2.0min内该反应速率v(CH3OCH3)=
2CO(g)+3H2(g),实验测得容器中压强与时间变化如图所示。则前2.0min内该反应速率v(CH3OCH3)= =12.2)。
=12.2)。
(4)二甲醚燃料电池常采用磺酸类质子溶剂,其工作原理如图所示,则负极的电极反应式为

您最近一年使用:0次
2021-04-04更新
|
648次组卷
|
5卷引用:湖北省华大新高考联盟2021届高三下学期3月教学质量测评(全国卷)理综化学试题
解题方法
9 . 下列关于化学反应方向的说法正确的是
| A.凡是放热反应都是自发反应 | B.凡是熵增大的反应都是自发反应 |
| C.凡是吸热反应都不是自发反应 | D.反应是否自发,需要综合考虑反应焓变和熵变 |
您最近一年使用:0次
2021-02-20更新
|
187次组卷
|
2卷引用:湖北省武汉市青山区2021-2022学年高二上学期期末考试化学试题
13-14高二上·江苏南通·期末
名校
解题方法
10 . 下列对于化学反应方向说法正确的是
| A.反应2A(g)+B(g)=3C(s)+D(g)在一定条件下能自发进行,说明该反应的ΔH>0 |
| B.常温下反应2Na2SO3(s)+O2(g)=2Na2SO4(s)能自发进行,则ΔH<0 |
| C.反应2Mg(s)+CO2(g)=C(s)+2MgO(s)在一定条件下能自发进行,则该反应的ΔH>0 |
| D.一定温度下,反应2NaCl(s)=2Na(s)+Cl2(g)的ΔH<0,ΔS>0 |
您最近一年使用:0次
2020-12-28更新
|
598次组卷
|
19卷引用:湖北省武汉市蔡甸区实验高级中学2020-2021学年高二上学期10月联合考试化学试题
湖北省武汉市蔡甸区实验高级中学2020-2021学年高二上学期10月联合考试化学试题(已下线)2012-2013学年江苏省启东市高二上学期期末考试化学试卷2015-2016学年福建省厦门市海沧中学高一下学期期末化学试卷云南省勐海县第三中学2019-2020学年高二上学期期末考试化学试题山东省枣庄市第八中学(东校区)2020-2021学年高二上学期9月月考化学试题山东省滨州市博兴县第三中学2020-2021学年高二上学期第一次月考化学试题内蒙古包头市第一中学2020-2021学年高二上学期第一次月考化学试题北京首都师范大学附属中学2020-2021学年高二上学期期中考试化学试题甘肃省武威市民勤县第一中学2020-2021学年高二上学期12月月考化学试题(理科)(已下线)【浙江新东方】绍兴qw118广东省台山市华侨中学2020-2021学年高二上学期期中考试化学试题山东省济南德润高级中学2021-2022学年高二上学期10月月考化学试题(已下线)第05练 化学反应的方向-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)(已下线)第28练 化学反应的方向-2023年高考化学一轮复习小题多维练(全国通用)(已下线)2.1 化学反应的方向-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)江苏省高邮市第一中学2021-2022学年高二上学期阶段测化学试题江西省丰城市第九中学2021-2022学年高二上学期第二次月考(日新班)化学试题江苏省连云港高级中学2022-2023高二上学期第一次阶段测试化学试题江苏省扬州大学附属中学2023-2024学年高二上学期11月期中化学试题



