解题方法
1 . 合成氨工艺是人工固氮最重要的途径。下图是合成氨的简要流程和反应方程式:

(1)图中X的主要成分是___________ ,这样操作的目的是___________ 。
(2)有利于提高合成氨平衡产率的条件为
A.低温 B.高温 C.低压 D.高压 E.催化剂
(3)T℃时,若在容积为 的密闭恒容容器中充入
的密闭恒容容器中充入 和
和 ,
, 后达到平衡,测得
后达到平衡,测得 的浓度为
的浓度为 。
。
①计算此段时间的反应速率
___________ , 的转化率为
的转化率为___________ 。
②已知300℃时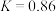 ,则(3)中的反应温度T
,则(3)中的反应温度T___________ 300(填“>”“<”或“=”)。
③若向平衡后的体系中同时加入 、
、 、
、 ,该反应是否处于平衡状态
,该反应是否处于平衡状态___________ (填“是”或“否”),此时
___________  。(填“>”或“<”或“=”)
。(填“>”或“<”或“=”)
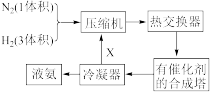


(1)图中X的主要成分是
(2)有利于提高合成氨平衡产率的条件为
A.低温 B.高温 C.低压 D.高压 E.催化剂
(3)T℃时,若在容积为
 的密闭恒容容器中充入
的密闭恒容容器中充入 和
和 ,
, 后达到平衡,测得
后达到平衡,测得 的浓度为
的浓度为 。
。①计算此段时间的反应速率

 的转化率为
的转化率为②已知300℃时
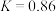 ,则(3)中的反应温度T
,则(3)中的反应温度T③若向平衡后的体系中同时加入
 、
、 、
、 ,该反应是否处于平衡状态
,该反应是否处于平衡状态
 。(填“>”或“<”或“=”)
。(填“>”或“<”或“=”)
您最近一年使用:0次
名校
解题方法
2 . 下列关于工业合成氨的叙述错误的是
| A.反应在高压下进行,有利于提高转化率 |
| B.温度越高越有利于工业合成氨 |
| C.在工业合成氨中,N2、H2的循环利用可降低成本 |
| D.及时从反应体系中分离出氨气有利于平衡向正反应方向移动 |
您最近一年使用:0次
名校
3 . 下列事实不能用平衡移动原理解释的是
A.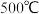 左右比室温更有利于合成 左右比室温更有利于合成 的反应 的反应 | B.夏天打开啤酒瓶,有许多气泡冒出 |
C.加压有利于 与 与 生成 生成 的反应 的反应 | D.催化剂的使用提高了合成 的产率 的产率 |
您最近一年使用:0次
名校
解题方法
4 . 以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料合成新型的环保催化剂(OMS—2)的工艺流程如图:

(1)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示。为减少MnS2O6的生成,“浸锰”的适宜温度是___ ;调pH后再过滤主要除去___ 元素。

(2)Mn12O19中氧元素化合价均为—2价,锰元素的化合价有两种,则Mn(Ⅲ)、Mn(Ⅳ)物质的量之比为__ 。生产过程中KMnO4、MnSO4•H2O按物质的量比1:5与K2S2O8反应,产物中硫元素全部以SO 的形式存在,该反应的离子方程式为
的形式存在,该反应的离子方程式为__ 。
(3)滤液X可进一步分离出多种化合物,其一为盐类,该盐在农业生产中可用作__ 。
(4)OMS—2是一种纳米级的分子筛。分别用OMS—2和MnOx对甲醛进行催化氧化,在相同时间内甲醛转化率和温度的关系如图:

由图可知,OMS—2与MnOx相比,催化效率较高是__ ,原因是__ 。

(1)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示。为减少MnS2O6的生成,“浸锰”的适宜温度是

(2)Mn12O19中氧元素化合价均为—2价,锰元素的化合价有两种,则Mn(Ⅲ)、Mn(Ⅳ)物质的量之比为
 的形式存在,该反应的离子方程式为
的形式存在,该反应的离子方程式为(3)滤液X可进一步分离出多种化合物,其一为盐类,该盐在农业生产中可用作
(4)OMS—2是一种纳米级的分子筛。分别用OMS—2和MnOx对甲醛进行催化氧化,在相同时间内甲醛转化率和温度的关系如图:

由图可知,OMS—2与MnOx相比,催化效率较高是
您最近一年使用:0次
名校
解题方法
5 . (1)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM﹣5催化下合成ETBE,反应的化学方程式为: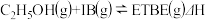 。回答下列问题:反应物被催化剂HZSM﹣5吸附的顺序与反应历程的关系如图所示,
。回答下列问题:反应物被催化剂HZSM﹣5吸附的顺序与反应历程的关系如图所示,
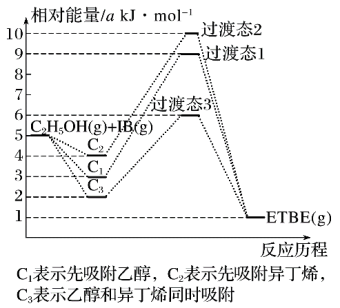
该反应的ΔH=_____ kJ•mol﹣1。反应历程的最优途径是______ (填C1、C2或C3)。
(2)一定条件下,用Fe2O3、NiO或Cr2O3作催化剂对燃煤烟气回收。反应为
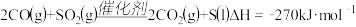 。
。
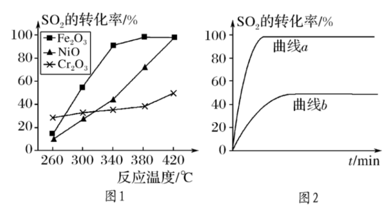
①其他条件相同、催化剂不同,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是:______ 。
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了n(CO):n(SO2)为1:1、3:1时SO2转化率的变化情况(图2)。则图2中表示n(CO):n(SO2)=3:1的变化曲线为______ 。
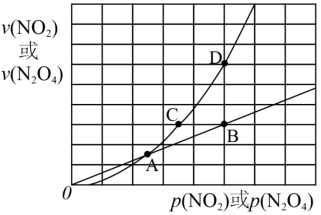
(3)已知NO2存在如下平衡: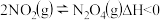 ,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:
,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系: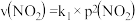 ,
,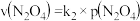 ,相应的速率与其分压关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
,相应的速率与其分压关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=____ ;在图标出点中,指出能表示反应达到平衡状态的点是______ ,理由是_______ 。
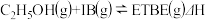 。回答下列问题:反应物被催化剂HZSM﹣5吸附的顺序与反应历程的关系如图所示,
。回答下列问题:反应物被催化剂HZSM﹣5吸附的顺序与反应历程的关系如图所示,
该反应的ΔH=
(2)一定条件下,用Fe2O3、NiO或Cr2O3作催化剂对燃煤烟气回收。反应为
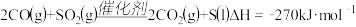 。
。

图3
①其他条件相同、催化剂不同,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是:
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了n(CO):n(SO2)为1:1、3:1时SO2转化率的变化情况(图2)。则图2中表示n(CO):n(SO2)=3:1的变化曲线为
(3)已知NO2存在如下平衡:
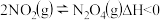 ,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:
,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系: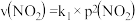 ,
,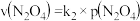 ,相应的速率与其分压关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
,相应的速率与其分压关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
您最近一年使用:0次
名校
6 . 某化工厂生产硝酸的流程如图1所示,其他条件相同时,装置③中催化剂铂网的成分、温度与氧化率的关系如图2所示,下列说法错误的是
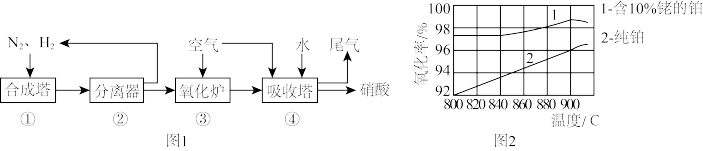

| A.该流程中,装置①③④中发生了氧化还原反应 |
B.装置②中利用氨气易液化的性质分离出 ,既加快了正反应速率又提高了合成氨的产率 ,既加快了正反应速率又提高了合成氨的产率 |
| C.装置③中最佳反应条件是铂网的成分为含10%铑的铂、温度为900℃ |
D.装置④中排出的废气含 、 、 等,可以用烧碱溶液吸收 等,可以用烧碱溶液吸收 |
您最近一年使用:0次
2020-12-19更新
|
418次组卷
|
4卷引用:江西省景德镇市景德镇一中2022届高三10月月考化学试题
江西省景德镇市景德镇一中2022届高三10月月考化学试题湖北省荆州市2021届高三上学期第一次质量检查化学试题(已下线)热点5 常见元素及其化合物的性质与应用-2021年高考化学专练【热点·重点·难点】山西省怀仁市2021-2022学年高二上学期期末调研化学试题
名校
解题方法
7 . 以天然气(CH4)为原料合成甲醇(CH3OH)。有关热化学方程式如下:
①2CH4(g)+O2(g)= 2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
②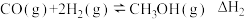
③
(1)ΔH2=________ kJ·mol-1。 反应①自发进行的条件是_________ (填序号)。
a 高温 b 低温 c 任何环境都自发 d 任何环境都不自发
(2)若在一定温度下的恒压容器中只投入1 mol CO和1 mol H2只发生反应②,下列量不再变化时可以判断反应达到平衡的是_________ 。
a 压强 b 密度 c 混合气的平均摩尔质量 d CO的体积分数
(3)在体积可变的密闭容器中投入1 mol CO和2 mol H2,在不同条件下发生反应: 。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。
。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。
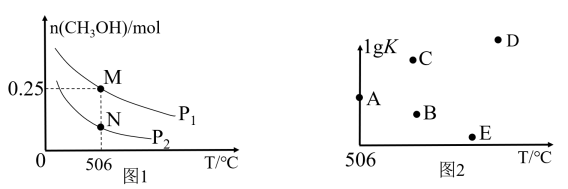
①M点时,H2的转化率为__________ ;压强:p1_______ p2 (填“>”、“<”或“=”)。
②反应速率:N点ʋ正 (CO)________ M点ʋ逆 (CO)(填“>”、“<”或“=”)。
③温度为506 ℃时,若压强为p1、在密闭容器中进行上述反应(起始投料不变),平衡时容器体积为1L,则平衡常数K=__________ (用分数表示)。在不同温度下上述反应的平衡常数的对数(lg K)如图2所示,则B、C、D、E四点中能正确表示该反应的lg K与T的关系的点为_______ (填字母)。
④在2 L恒容密闭容器中充入a(a>0) mol H2、2 mol CO和6 mol CH3OH(g),在506 ℃下进行上述反应。为了使该反应逆向进行,a的范围为____________ 。
①2CH4(g)+O2(g)= 2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
②
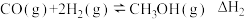
③

(1)ΔH2=
a 高温 b 低温 c 任何环境都自发 d 任何环境都不自发
(2)若在一定温度下的恒压容器中只投入1 mol CO和1 mol H2只发生反应②,下列量不再变化时可以判断反应达到平衡的是
a 压强 b 密度 c 混合气的平均摩尔质量 d CO的体积分数
(3)在体积可变的密闭容器中投入1 mol CO和2 mol H2,在不同条件下发生反应:
 。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。
。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。
①M点时,H2的转化率为
②反应速率:N点ʋ正 (CO)
③温度为506 ℃时,若压强为p1、在密闭容器中进行上述反应(起始投料不变),平衡时容器体积为1L,则平衡常数K=
④在2 L恒容密闭容器中充入a(a>0) mol H2、2 mol CO和6 mol CH3OH(g),在506 ℃下进行上述反应。为了使该反应逆向进行,a的范围为
您最近一年使用:0次
2020-12-01更新
|
158次组卷
|
2卷引用:江西景德镇市浮梁一中2020-2021学年高二下学期4月月考争优部化学试题
名校
解题方法
8 . 2019年9月,我国科研人员研制出Ti-H-Fe双温区催化剂,其中Ti-H区域和Fe区域的温度差可超过100℃。Ti-H-Fe双温区催化合成氨的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法错误的是( )
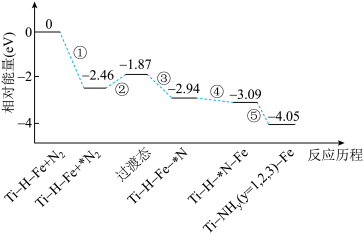

| A.①②③在高温区发生,④⑤在低温区发生 |
| B.该历程中能量变化最大的是2.46eV,是氮分子中氮氮三键的断裂过程 |
| C.在高温区加快了反应速率,低温区提高了氨的产率 |
| D.使用Ti-H-Fe双温区催化合成氨,不会改变合成氨反应的反应热 |
您最近一年使用:0次
2020-07-07更新
|
878次组卷
|
15卷引用:江西省景德镇市乐平中学20222-2023学年高二上学期第一次月考化学试题
江西省景德镇市乐平中学20222-2023学年高二上学期第一次月考化学试题河南省郑州市2020届高三第二次质检理综试卷湖南省长沙市雅礼中学2020届高考6月模拟卷(一)理综化学试题安徽省六安市舒城中学2019-2020学年高二下学期第三次月考化学试题(已下线)第六单元 化学反应速率和化学平衡测试题-2021年高考化学一轮复习名师精讲练【学科网名师堂】重庆市2021届高三上学期第一次预测性考试化学试题黑龙江省大庆实验中学2020-2021学年高二10月月考化学试题江西省南昌市第二中学2020-2021学年高二上学期期中考试化学试题江苏省南通市新高考2021届高三上学期期中考试化学(ⅱ卷)试题(已下线)【南昌新东方】3. 2020 高二上 南昌二中 期中考试 吴丹江西省南昌市南昌县莲塘第三中学2020-2021学年高二上学期第二次月考化学试题河南省信阳高级中学2020-2021学年高二下学期回顾测试化学试题湖南省常德市第二中学2020届高三临考冲刺理科综合化学试题河南省重点高中2021-2022学年高二上学期阶段性调研联考二化学试题(已下线)化学(九省联考考后提升卷,安徽卷)-2024年1月“九省联考”真题完全解读与考后提升
名校
解题方法
9 . 2018年北京市公交行业迈入氢能源时代。“制氢”“储氢”“用氢”等一直都是能源研究的热点。工业上制取H2有多种方法.如:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=+131.5kJ·mol-1
②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2=+206.2kJ·mol-1
③CH4(g)+CO2(g)=2CO(g)+2H2(g) △H3=+247.4kJ·mol-1
④2H2O(g)=2H2(g)+O2(g) △H4=+483.6kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:____________________ .
(2)氢气燃料电池能大幅度提高能量的转化率。相同条件下,其能量密度(能量密度之比等于单位质量的可燃物转移电子数之比)是甲醇燃料电池的_______ 倍(计算结果保留两位有效数字)。
(3)科学家研发的“全氢电池"的工作原理如图所示,该电池工作一段时间后,右池溶液的导电 能力几乎不变。下列有关该电 池的说法正确的是_____ (填字母代号)。
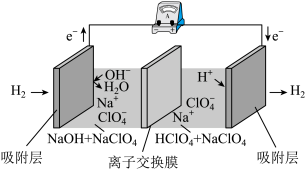
a.电池的总反应是2H2 +O2 = 2H2O
b.左边电极上的电势高于右边电极上的电势
c.负极的电极反应是H2 - 2e- + 2OH- = 2H2O
d.装置中所用的是阴离子交换膜
e.产生能源的源泉是酸和碱的中和能
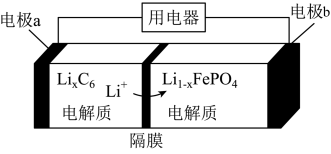
(4)LiFePO4电池稳定性高、安全、对环境友好,该电池的总反应式是Li1-xFePO4+LixC6 LiFePO4+C6,其放电时的工作原理如图所示。则:充电时,电极a的电极名称为
LiFePO4+C6,其放电时的工作原理如图所示。则:充电时,电极a的电极名称为_______________ ; 放电时电极b的电极反应式为______________________________ .
①C(s)+H2O(g)=CO(g)+H2(g) △H1=+131.5kJ·mol-1
②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2=+206.2kJ·mol-1
③CH4(g)+CO2(g)=2CO(g)+2H2(g) △H3=+247.4kJ·mol-1
④2H2O(g)=2H2(g)+O2(g) △H4=+483.6kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:
(2)氢气燃料电池能大幅度提高能量的转化率。相同条件下,其能量密度(能量密度之比等于单位质量的可燃物转移电子数之比)是甲醇燃料电池的
(3)科学家研发的“全氢电池"的工作原理如图所示,该电池工作一段时间后,右池溶液的导电 能力几乎不变。下列有关该电 池的说法正确的是

a.电池的总反应是2H2 +O2 = 2H2O
b.左边电极上的电势高于右边电极上的电势
c.负极的电极反应是H2 - 2e- + 2OH- = 2H2O
d.装置中所用的是阴离子交换膜
e.产生能源的源泉是酸和碱的中和能
(4)LiFePO4电池稳定性高、安全、对环境友好,该电池的总反应式是Li1-xFePO4+LixC6
 LiFePO4+C6,其放电时的工作原理如图所示。则:充电时,电极a的电极名称为
LiFePO4+C6,其放电时的工作原理如图所示。则:充电时,电极a的电极名称为
您最近一年使用:0次
2019-10-05更新
|
202次组卷
|
2卷引用:江西省景德镇市浮梁一中2020-2021学年高二下学期4月月考化学试题
真题
名校
10 . 据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g),下列叙述错误的是
CH3CH2OH(g)+3H2O(g),下列叙述错误的是
 CH3CH2OH(g)+3H2O(g),下列叙述错误的是
CH3CH2OH(g)+3H2O(g),下列叙述错误的是| A.使用Cu-Zn-Fe催化剂可大大提高生产效率 |
| B.反应需在300℃进行可推测该反应是吸热反应 |
| C.充入大量CO2气体可提高H2的转化率 |
| D.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率 |
您最近一年使用:0次
2019-01-30更新
|
669次组卷
|
46卷引用:江西省乐平中学2022-2023学年高二上学期11月期中考试化学试题
江西省乐平中学2022-2023学年高二上学期11月期中考试化学试题2010年全国普通高等学校招生统一考试上海卷化学试题(已下线)2010年6月浙江省金温七校高二化学期末卷2010年高考化学试题分项专题七 化学反应中的能量变化2010年高考化学试题分项专题八 化学反应速率和化学平衡(已下线)2010年黑龙江省双鸭山一中高三上学期期中考试(化学)(已下线)2011届上海市吴淞中学高三上学期期中考试化学试卷(已下线)2011-2012年广东省汕头市金山中学高二上学期期中考试化学试卷(理科)(已下线)2013-2014学年广东省执信中学高二上学期期中考试理科化学试卷2014-2015学年甘肃省武威六中高二上学期第二次月考化学试卷2014-2015学年江西省高安中学高一重点班下期末化学试卷2016届江西省上饶市余干二中高三上学期教学质检化学试卷2015-2016学年山东省淄博市淄川一中等三校高二上期末联考化学试卷2015-2016学年辽宁师大附中高一下学期6月月考化学试卷2016-2017学年河南省师大附中高二上期中化学试卷上海市格致中学2016-2017学年高一下学期第二次测验化学试题山西省大同市第一中学2017-2018学年高二上学期期中考试化学试题天津市红桥区2017-2018学年高二上学期期末考试化学试题新疆昌吉市2017-2018学年高二上学期期末考试化学试题【全国百强校】北京101中学2017-2018学年高二下学期期中考试化学试题吉林省长春市田家炳实验中学2018-2019学年高二上学期第一学程检测化学试题【全国百强校】贵州省思南中学2018-2019学年高二上学期期中考试化学试题新疆乌鲁木齐市二十三中学2018-2019学年高二10月月考化学试题湖南省永州市东安县第一中学2019-2020学年高二上学期第一次月考化学试题江西省南城县第二中学2018-2019学年高二上学期第二次月考化学试题安徽省亳州市第十八中学2019-2020学年高二上学期第一次月考化学试题山西省朔州市怀仁县第一中学2018-2019学年高二上学期第二次月考化学试题2020届高三化学选修4二轮专题练——焓变及反应热综合【选择精编25题】贵州省长顺县二中2019-2020学年高二上学期期末考试化学试题山西省忻州市第一中学2019-2020学年高一4月月考化学试题河北省黄骅中学2020-2021学年高二上学期第一次月考化学试题湖南省娄底市第一中学2020-2021学年高二上学期期中考试化学(高考班)试题湖北省汉川市第二中学2020-2021学年高二上学期期中考试化学试题江苏省镇江市第一中学2020-2021学年高二下学期4月分阶段测化学试题河南省南阳市一中2021-2022学年高二上学期第一次月考化学试题山西省运城市康杰中学2021-2022学年高二上学期期中化学试题浙江省山河联盟2021-2022学年高二上学期12月考试化学试题宁夏银川市第二中学2021-2022学年高二下学期第一次月考化学试题(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)河北省唐山市迁西县职业技术教育中心2021-2022学年高二(普职融通部)上学期期中考试化学试题(已下线)化学预测卷(四)-预测卷(浙江专版)湖南省常德市西洞庭管理区第一中学2022-2023学年高二上学期第二次月考化学试题第2课时 温度、浓度对化学平衡的影响(已下线)专题06 化学反应的方向及调控【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)新疆实验中学2023-2024学年高二上学期期中考试化学试题(已下线)第04讲 化学反应的方向、化学反应的调控(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)



