名校
解题方法
1 . X、Y、Z是三种气态物质,在一定温度下其变化符合下图。下列说法一定正确的是
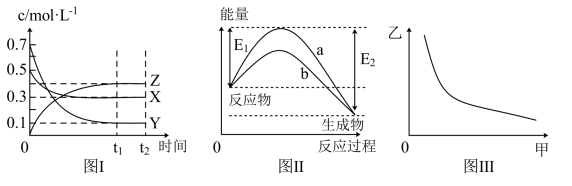

A.该反应的热化学方程式为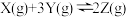 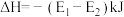 |
B.该温度下,反应的平衡常数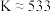 ,且若升高温度,K值减小 ,且若升高温度,K值减小 |
| C.图Ⅱ曲线b表示加入催化剂使反应活化能减小,焓变减小 |
| D.若图Ⅲ中甲表示压强,乙表示Z的含量,则其变化符合图Ⅲ中曲线 |
您最近一年使用:0次
名校
2 . 如图表示合成氨反应过程中的能量变化。关于合成氨反应 ,下列说法
,下列说法不 正确的是
 ,下列说法
,下列说法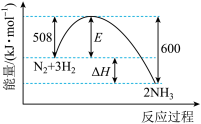
A.升高温度有利于提高 的平衡转化率 的平衡转化率 |
B.提高 与 与 的投料比可增大 的投料比可增大 的转化率 的转化率 |
C.增大压强能提高 的反应速率和转化率 的反应速率和转化率 |
| D.使用催化剂能缩短该反应到达平衡的时间 |
您最近一年使用:0次
2022-11-18更新
|
293次组卷
|
8卷引用:江苏省扬州市2020-2021学年高二下学期期末考试化学(选修)试题
江苏省扬州市2020-2021学年高二下学期期末考试化学(选修)试题(已下线)第二章 第三节化学平衡(第2课时 化学平衡的影响因素)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(原卷版)(已下线)第2章 化学反应速率和化学平衡(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)云南昆明师范专科学校附属中学2021-2022学年高二上学期期中考试化学试题(已下线)2.4 化学反应的调控(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)江苏省马坝高级中学2022-2023学年高二上学期期中考试化学试题江苏省南京市五校(秦淮中学,溧水二高,江浦文昌)2023-2024学年高二下学期期中联考化学试题(已下线)第二章 化学反应速率与化学平衡(B卷·能力提升练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)
名校
解题方法
3 . 通过下列反应合成CO和CH4,可实现CO2的再转化:
①CO2(g)+4H2(g) CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
②CO2(g)+H2(g) CO(g)+H2O(g) △H>0
CO(g)+H2O(g) △H>0
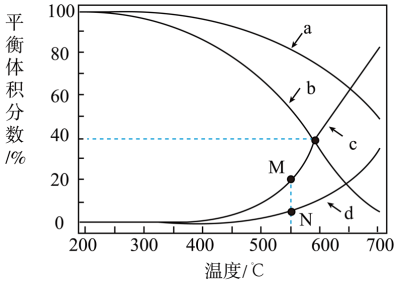
在密闭容器中通入3 mol的H2和1 mol的CO2,分别在压强为1 MPa 和10 MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。
下列说法不正确的是
①CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0②CO2(g)+H2(g)
 CO(g)+H2O(g) △H>0
CO(g)+H2O(g) △H>0在密闭容器中通入3 mol的H2和1 mol的CO2,分别在压强为1 MPa 和10 MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。

下列说法不正确的是
| A.曲线a表示10 MPa条件下CH4的体积分数随温度的变化 |
| B.曲线a、d交点纵坐标可能为40% |
| C.550°C时M点位于N点上方是由于压强降低时,平衡①逆向移动导致平衡②正向移动 |
| D.由曲线b、c的交点可计算该温度下反应②的平衡常数为2.4 |
您最近一年使用:0次
2022-09-02更新
|
211次组卷
|
2卷引用:江苏省南师附中、天一中学、海安中学、海门中学四校2021-2022学年高三12月联考化学试题
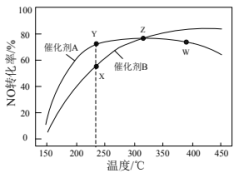
4 . 燃煤电厂锅炉尾气中含有氮氧化物(主要成分NO),可通过主反应4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H=-1627.7kJ·mol-1除去。温度高于300℃时会发生副反应:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-904.7kJ·mol-1。在恒压、反应物起始物质的量之比一定的条件下,反应相同时间,NO的转化率在不同催化剂作用下随温度变化的曲线如图所示。下列有关说法一定正确的是

| A.N2(g)+O2(g)=2NO(g) △H=-180.7kJ·mol-1 |
| B.图中X点所示条件下,反应时间足够长,NO的转化率能达到Y点的值 |
| C.关于X、Y、Z三点,KX=KY,Z点反应达到化学平衡状态 |
| D.图中Z点到W点NO的转化率降低的原因是主反应的平衡逆向移动 |
您最近一年使用:0次
名校
5 . 将一定量纯净的X置于某10L容积恒定的真空容器中(假设固体试样体积忽略不计),在恒定温度下使其达到分解平衡: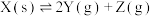 ,实验测得不同温度下的分解平衡常数列于下表,下列说法中不正确的是
,实验测得不同温度下的分解平衡常数列于下表,下列说法中不正确的是
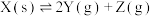 ,实验测得不同温度下的分解平衡常数列于下表,下列说法中不正确的是
,实验测得不同温度下的分解平衡常数列于下表,下列说法中不正确的是| 温度(°C) | 15.0 | 25.0 | 30.0 | 35.0 |
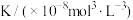 | 0.205 | 1.64 | 4.68 | 10.8 |
A.该反应 |
| B.若气体密度不再随时间变化时表示反应达平衡状态 |
| C.若在恒温下,压缩容器体积,再次达平衡后,X的物质的量比原平衡大 |
| D.35℃时,达平衡时,X分解了0.02mol |
您最近一年使用:0次
6 . 氨是化肥生产工业的重要原料。传统的Haber—Bosch法目前仍是合成氨的主要方式,反应原理为N2(g)+3H2(g) 2NH3(g),其生产条件需要高温高压。近来电催化氮气合成氨因节能、环境友好等优势,受到广泛关注,下列有关Haber-Bosch法合成氨反应的说法正确的是
2NH3(g),其生产条件需要高温高压。近来电催化氮气合成氨因节能、环境友好等优势,受到广泛关注,下列有关Haber-Bosch法合成氨反应的说法正确的是
 2NH3(g),其生产条件需要高温高压。近来电催化氮气合成氨因节能、环境友好等优势,受到广泛关注,下列有关Haber-Bosch法合成氨反应的说法正确的是
2NH3(g),其生产条件需要高温高压。近来电催化氮气合成氨因节能、环境友好等优势,受到广泛关注,下列有关Haber-Bosch法合成氨反应的说法正确的是| A.该反应的ΔH>0、ΔS<0 |
| B.将氨气及时液化分离可加快化学反应速率 |
| C.当2v(H2)正=3v(NH3)逆时,反应达到平衡状态 |
| D.提高体系的压强可增大反应的化学平衡常数 |
您最近一年使用:0次
2021-11-20更新
|
411次组卷
|
6卷引用:江苏省常州市部分重点中学2021-2022学年高三上学期期中考试化学试题
江苏省常州市部分重点中学2021-2022学年高三上学期期中考试化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)回归教材重难点06 化学反应速率与化学平衡-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点06 化学反应速率与化学平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)黑龙江省哈尔滨师范大学附属中学2022-2023学年高二上学期10月月考化学试题
名校
解题方法
7 . 通过反应Ⅰ: 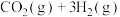

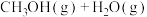
 ,可以实现温室气体资源化利用。该反应通过如下步骤实现:
,可以实现温室气体资源化利用。该反应通过如下步骤实现:
反应Ⅱ:
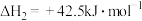
反应Ⅲ:
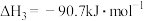
密闭容器中,反应物起始物质的量比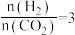 时,在不同条件下(分别在温度为250℃下压强变化和在压强为
时,在不同条件下(分别在温度为250℃下压强变化和在压强为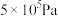 下温度变化)达到平衡时
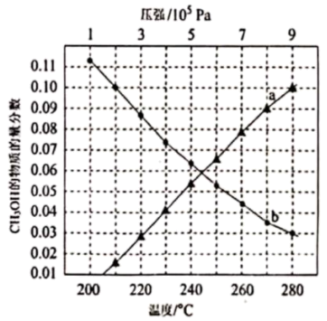
下温度变化)达到平衡时 物质的量分数变化如图所示。下列有关说法正确的是
物质的量分数变化如图所示。下列有关说法正确的是
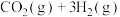

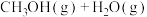
 ,可以实现温室气体资源化利用。该反应通过如下步骤实现:
,可以实现温室气体资源化利用。该反应通过如下步骤实现:反应Ⅱ:

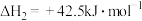
反应Ⅲ:

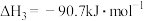
密闭容器中,反应物起始物质的量比
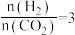 时,在不同条件下(分别在温度为250℃下压强变化和在压强为
时,在不同条件下(分别在温度为250℃下压强变化和在压强为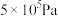 下温度变化)达到平衡时
下温度变化)达到平衡时 物质的量分数变化如图所示。下列有关说法正确的是
物质的量分数变化如图所示。下列有关说法正确的是
A.反应Ⅰ的平衡常数可表示为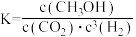 |
B.曲线 表示CH3OH的物质的量分数随温度变化 表示CH3OH的物质的量分数随温度变化 |
| C.提高CO2转化为CH3OH的转化率,需要研发在低温区高效的催化剂 |
D.在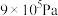 、280℃条件下,平衡时CH3OH的物质的量分数为0.10 、280℃条件下,平衡时CH3OH的物质的量分数为0.10 |
您最近一年使用:0次
2021-09-11更新
|
386次组卷
|
3卷引用:江苏省苏州市2021-2022学年高三上学期期初调研考试化学试题
8 . 下列关于2SO2(g)+O2(g)⇌2SO3(g) ∆H=-197kJ∙mol-1的说法正确的是
| A.该反应的∆S>0 |
| B.该反应中,反应物的总能量小于生成物的总能量 |
| C.生产过程中将SO3分离出去,逆反应速率减慢 |
| D.其他条件不变,增大压强,平衡右移,平衡常数增大 |
您最近一年使用:0次
2021-12-14更新
|
530次组卷
|
5卷引用:江苏省南通市海门区2021-2022学年高三第二次诊断测试化学试题
江苏省南通市海门区2021-2022学年高三第二次诊断测试化学试题江苏省苏州市重点中学2022-2023学年高三上学期10月月考化学试题江苏省灌南高级中学2023-2024学年高三上学期第一次月考化学试题(已下线)第22讲 化学平衡常数及转化率的计算(练)-2023年高考化学一轮复习讲练测(全国通用)黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期末考试化学试题
名校
9 . 工业上利用炭和水蒸气反应:C(s)+H2O(g)  CO(g)+H2(g)、CO(g)+H2O(g)
CO(g)+H2(g)、CO(g)+H2O(g)  CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO
CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO 能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关说法正确的是
能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关说法正确的是
 CO(g)+H2(g)、CO(g)+H2O(g)
CO(g)+H2(g)、CO(g)+H2O(g)  CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO
CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO 能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关说法正确的是
能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关说法正确的是| A.增大压强有利于提高上述反应中焦炭的利用率 |
B.NaHCO3溶液中,HCO 能形成多聚体是因为氢键的作用 能形成多聚体是因为氢键的作用 |
| C.若反应体系中,c(CO)=a mol·L-1,c(CO2)=b mol·L-1,则c(H2)=(a+b) mol·L-1 |
| D.析出NaHCO3的反应属于氧化还原反应 |
您最近一年使用:0次
名校
解题方法
10 . 对于反应2SO2(g)+O2(g) 2SO3(g),下列有关说法不正确的是
2SO3(g),下列有关说法不正确的是
 2SO3(g),下列有关说法不正确的是
2SO3(g),下列有关说法不正确的是| A.使用催化剂能缩短该反应到达平衡的时间 |
| B.升高温度有利于提高SO2的平衡转化率 |
C.提高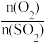 的值可增大SO2的转化率 的值可增大SO2的转化率 |
| D.增大体系的压强能提高SO2的反应速率和转化率 |
您最近一年使用:0次
2021-06-23更新
|
479次组卷
|
6卷引用:江苏省盐城市东台创新高级中学2020-2021学年高二4月份月检测化学试题
江苏省盐城市东台创新高级中学2020-2021学年高二4月份月检测化学试题江苏省苏州市相城区陆慕高级中学2021-2022学年高三上学期第一次阶段性诊断测试化学试题(已下线)2.3.2 影响化学平衡状态的因素-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)2.4 化学反应的调控(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)江苏省常州市第一中学2022-2023学年高二上学期期末考试化学试题江苏省常州市第一中学2023-2024学年高二上学期10月月考化学试题



