名校
1 . 已知反应式: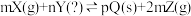 ,已知反应已达平衡,此时
,已知反应已达平衡,此时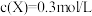 ,其他条件不变,若容器缩小到原来的
,其他条件不变,若容器缩小到原来的 ,
,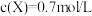 ,下列说法不正确的是
,下列说法不正确的是
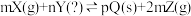 ,已知反应已达平衡,此时
,已知反应已达平衡,此时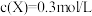 ,其他条件不变,若容器缩小到原来的
,其他条件不变,若容器缩小到原来的 ,
,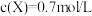 ,下列说法不正确的是
,下列说法不正确的是A.系数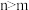 | B.反应向逆方向移动 |
| C.Y可能是固体或液体 | D.Z的体积分数减小 |
您最近一年使用:0次
2021-11-05更新
|
771次组卷
|
7卷引用:安徽省滁州市定远县育才学校2021-2022学年高二上学期期中考试化学试题
安徽省滁州市定远县育才学校2021-2022学年高二上学期期中考试化学试题广东省广州市部分学校2021-2022学年高二上学期期中联考化学试题广东省广州市六校联考2021-2022学年高二上学期期中考试化学试题新疆维吾尔自治区喀什市2021-2022学年高三上学期全真模拟化学试题(已下线)上海市华东师范大学第二附属中学2021-2022学年高一下学期期末线上测试化学试题广东省广州市2022-2023学年高二上学期期中考试化学试题(已下线)第05讲 影响化学平衡的因素-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)
名校
解题方法
2 . 温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1molNO2,发生反应:2C(s)+2NO2(g) N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
 N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。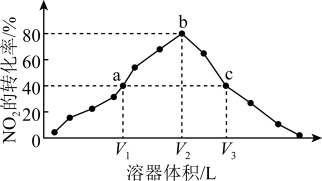
A.T℃时,该反应的化学平衡常数为Kc= mol·L-1 mol·L-1 |
| B.由图可知,c点V正>V逆 |
| C.向a点平衡体系中充入一定量的NO2,达到平衡时,NO2的转化率比原平衡小 |
| D.容器内的压强:pa∶pb=6∶7 |
您最近一年使用:0次
2021-09-06更新
|
1443次组卷
|
16卷引用:安徽省六安市第一中学2022届高三上学期第三次月考化学试题
安徽省六安市第一中学2022届高三上学期第三次月考化学试题安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题重庆育才中学2022届高考适应性考试二化学试题江西省抚州市临川一中、临川一中实验学校2022届高三第一次月考化学试题吉林省洮南市第一中学2021-2022学年高二上学期第一次月考化学试题河北省保定市定州市2021-2022学年高二上学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高三上学期期中考试化学试题四川省成都市树德中学2021-2022学年高二上学期11月阶段性测试(期中)化学试题 山西省长治市第二中学2021-2022学年高三上学期第三次练考化学试题黑龙江省哈尔滨市尚志中学2022-2023学年高三上学期期中考试化学试题广东省梅州市蕉岭县蕉岭中学2022-2023学年高三上学期高二第二次质检化学试题(已下线)化学(重庆A卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)易错点4化学反应速率、平衡图像分析错误(已下线)题型24 化学反应平衡常数、平衡转化率图像福建师范大学附属中学2023-2024学年高二上学期期中考试化学试题
名校
3 . 700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O(g),发生如下反应:CO(g)+H2O(g) CO2+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法不正确的是
CO2+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法不正确的是
 CO2+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法不正确的是
CO2+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法不正确的是| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.80 | 0.90 |
| t1 | 1.20 | |
| t2 | 0.30 |
| A.t2后若压缩容器体积至原来一半,再次平衡则c(H2O)=0.30mol/L |
| B.若初始量CO:3.6mol,H2O:1.8mol,则平衡时n(H2O)=0.60mol |
| C.t2后若增加0.9 mol H2O,则再次平衡时,H2的体积分数为25% |
| D.若为绝热容器(容器初始温度仍为700℃),其他条件不变,则平衡时n(H2)>0.60mol |
您最近一年使用:0次
2021-11-15更新
|
201次组卷
|
4卷引用:安徽省A10联盟2021-2022学年高二上学期期中联考化学试题
名校
4 . 某温度下,在恒容密闭容器中SO2、O2、SO3三种气态物质建立化学平衡:2SO2(g)+O2(g) 2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是
2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是
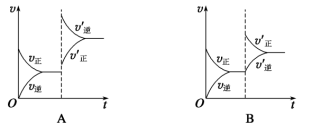
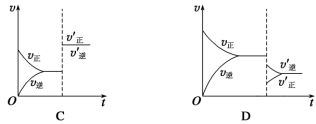
 2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是
2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是

| A.压缩容器体积 | B.通入O2 |
| C.通入稀有气体He | D.减低温度 |
您最近一年使用:0次
2021-11-15更新
|
201次组卷
|
2卷引用:安徽省A10联盟2021-2022学年高二上学期期中联考化学试题
名校
5 . 根据化学反应速率或平衡理论,联系生产实际,下列说法错误的是
| A.供热公司为了节能减排,将煤块粉碎,让煤充分燃烧 |
| B.啤酒瓶开启后,马上泛起大量泡沫,可用勒夏特列原理解释 |
| C.使用高效催化剂是大大提高原料平衡转化率的有效方法 |
| D.将一氧化碳中毒者放入高压氧舱,增大氧气浓度,利用平衡移动原理缓解病情 |
您最近一年使用:0次
2020-12-06更新
|
266次组卷
|
7卷引用:安徽省马鞍山市第二中学2021-2022学年高二上学期期中考试化学试题
6 . 体积不变的密闭容器中发生反应: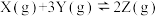
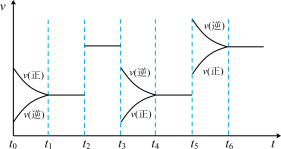
 ,下图表示该反应的速率(v)随时间(t)变化的关系,
,下图表示该反应的速率(v)随时间(t)变化的关系, 、
、 、
、 时刻外界条件有所改变。下列说法中正确的是
时刻外界条件有所改变。下列说法中正确的是
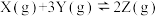
 ,下图表示该反应的速率(v)随时间(t)变化的关系,
,下图表示该反应的速率(v)随时间(t)变化的关系, 、
、 、
、 时刻外界条件有所改变。下列说法中正确的是
时刻外界条件有所改变。下列说法中正确的是
A. 时间内平衡转化率最低 时间内平衡转化率最低 | B. 时降低了温度 时降低了温度 |
C. 时只增加了气体物质Z 时只增加了气体物质Z | D. 时加入了催化剂 时加入了催化剂 |
您最近一年使用:0次
名校
7 . 25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表,说法错误的是
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
| A.反应达到平衡时,X的转化率为50% |
| B.方程式为X+3Y⇌2Z,平衡常数为1600 |
| C.增大压强使平衡正向方向移动,平衡常数增大 |
| D.改变温度可以改变此反应的平衡常数 |
您最近一年使用:0次
2021-12-29更新
|
222次组卷
|
11卷引用:安徽省六安市新安中学2021-2022学年高二上学期期中考试化学试题
安徽省六安市新安中学2021-2022学年高二上学期期中考试化学试题安徽省六安市新安中学2021-2022学年高二上学期12月月考化学试题河南省济源市第五中学2020-2021学年高二下学期6月月考化学试题(已下线)第二章 第三节化学平衡(第3课时 化学平衡常数)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)内蒙古霍林郭勒市第一中学2021-2022学年高二上学期期中考试化学试题河南省范县第一中学等学校2021-2022学年高二上学期联考检测化学试题 广西玉林市市直六所普通高中2021-2022学年高二上学期期中考试理科综合化学试题河南省安阳市滑县实验学校2020-2021学年高二上学期期中考试化学试题(普通班)内蒙古集宁新世纪中学2020-2021学年高二上学期期中考试化学试题(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)四川省泸县第四中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
8 . 某密闭容器中,按物质的量之比1:1充入X、Y两种气体,发生反应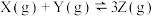
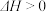 ,达到平衡后,下列有关说法正确的是
,达到平衡后,下列有关说法正确的是
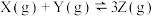
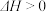 ,达到平衡后,下列有关说法正确的是
,达到平衡后,下列有关说法正确的是| A.继续通入少量物质的量之比为1:1的X、Y气体,保持容器容积不变,达到新平衡时,Z的体积分数增大 |
| B.其他条件不变,升高温度,正逆反应速率都增大,平衡时Z的体积分数比原平衡的体积分数大,平衡常数增大 |
| C.其他条件不变,将容积压缩至原来的一半,平衡逆向移动,平衡时X的体积分数比原平衡的体积分数大,平衡常数减小 |
| D.保持容器容积不变,增加Z的量,平衡逆向移动,平衡时Z的浓度比原平衡的小,体积分数比原平衡的体积分数小 |
您最近一年使用:0次
2020-12-30更新
|
391次组卷
|
6卷引用:安徽省蚌埠第三中学2020-2021学年高二上学期1月教学质量检测化学试题
安徽省蚌埠第三中学2020-2021学年高二上学期1月教学质量检测化学试题安徽省六安市舒城中学2020-2021学年高二上学期期末考试化学试题陕西省商洛市2020-2021学年高二上学期期末教学质量检测化学试题河南省名校联盟2020-2021学年高二上学期12月联合考试化学试题(已下线)练习8 化学平衡的移动-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)(已下线)专题10 化学反应速率与平衡-2023年高考化学一轮复习小题多维练(全国通用)
名校
9 . 在密闭容器中发生反应2SO2(g)+O2(g) 2SO3(g) ΔH<0,下列说法不正确的是( )
2SO3(g) ΔH<0,下列说法不正确的是( )
 2SO3(g) ΔH<0,下列说法不正确的是( )
2SO3(g) ΔH<0,下列说法不正确的是( )| A.升温,正、逆反应速率均加快 | B.压缩容器增大压强,化学平衡正向移动 |
| C.充入O2,可提高SO2的转化率 | D.当气体总质量不变时,反应达平衡状态 |
您最近一年使用:0次
2019-11-28更新
|
109次组卷
|
3卷引用:安徽省滁州市定远县育才学校2021-2022学年高二上学期期中考试(实验班)化学试题
名校
10 . 反应2NO2(g)  N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
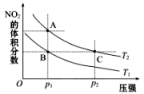
 N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
| A.A、C两点气体的颜色:A深,C浅 |
| B.A、C两点的反应速率:A>C |
| C.A、C两点气体的平均相对分子质量:A>C |
| D.由状态A到状态B,可以采用降温的方法 |
您最近一年使用:0次
2018-12-19更新
|
103次组卷
|
2卷引用:安徽省淮北市树人高级中学2020-2021学年高二上学期第一次联考化学试题



