名校
1 . 用下列实验装置进行相应实验,能达到实验目的的是
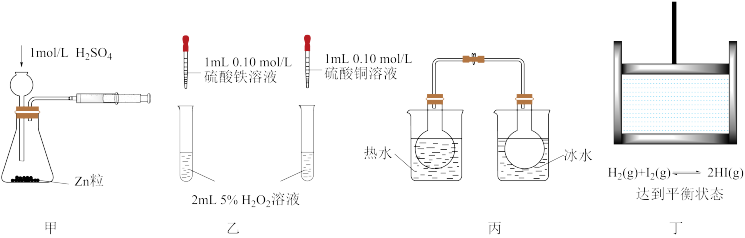

| A.利用装置甲测定化学反应速率 |
| B.利用装置乙证明对H2O2分解反应Fe3+催化效果好于Cu2+ |
| C.利用装置丙探究温度对平衡2NO2(g)⇌N2O4(g)的影响 |
| D.利用装置丁探究压强对平衡H2(g)+I2(g)⇌2HI(g)的影响 |
您最近一年使用:0次
2022-09-19更新
|
465次组卷
|
3卷引用:山东省济南市莱芜凤城高级中学2021-2022学年高二上学期期中考试化学试题
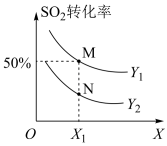
2 . 在体积可变的密闭容器中投入0.5 molO2和1 mol SO2,不同条件下发生反应:O2(g)+2SO2(g) 2SO3(g)ΔH。实验测得平衡时SO2的转化率[α(SO2 )]随温度、压强的变化如图所示。下列说法错误的是
2SO3(g)ΔH。实验测得平衡时SO2的转化率[α(SO2 )]随温度、压强的变化如图所示。下列说法错误的是
 2SO3(g)ΔH。实验测得平衡时SO2的转化率[α(SO2 )]随温度、压强的变化如图所示。下列说法错误的是
2SO3(g)ΔH。实验测得平衡时SO2的转化率[α(SO2 )]随温度、压强的变化如图所示。下列说法错误的是
| A.Y代表压强,且Y1> Y2;X代表温度,且ΔH <0 |
| B.M点反应物转化率之比α(O2) :α (SO2)=1:1,N点该比例减小 |
| C.若M、N两点对应的容器体积均为5 L,则N点的平衡常数K= 20 |
| D.M、N两点对应的平均摩尔质量:M(M)<M(N) |
您最近一年使用:0次
2021-12-03更新
|
229次组卷
|
2卷引用:山东省2021-2022学年高三上学期11月(第三次)联考化学试题
3 . 工业制硫酸的一步重要反应是SO2在400~600℃下的催化氧化:2SO2(g)+ O2(g)⇌2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法正确的是
| A.使用催化剂可加快反应速率,提高SO3产率 |
| B.其它条件保持不变,温度越高,速率越快,生产效益越好 |
| C.实际生产中选定400~600℃作为操作温度,其原因是在此温度下催化剂的活性最高 |
| D.增大压强可以提高SO3产率,但高压对动力和设备要求太高,会增加生产成本 |
您最近一年使用:0次
名校
解题方法
4 . 在容积恒为1 L的密闭容器中通入一定量N2O4,发生反应 △H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
△H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
 △H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
△H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是| t/s | 0 | 20 | 40 | 60 | 80 |
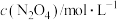 | 0.100 | 0.062 | 0.048 | 0.040 | 0.040 |
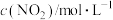 | 0 | 0.076 | 0.104 | 0.120 | 0.120 |
A.0~40 s,N2O4的平均反应速率为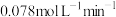 |
| B.80 s时,再充入N2O4、NO2各0.12 mol,平衡移动 |
| C.升高温度,反应的化学平衡常数值增大 |
| D.若压缩容器,达新平衡后,混合气颜色比原平衡时深 |
您最近一年使用:0次
2021-09-12更新
|
402次组卷
|
2卷引用:山东省济南市历城第二中学2021-2022学年(2022届)高三上学期开学考试(B)化学试题
5 . 某温度下,在甲、乙、丙三个恒容密闭容器中进行反应CO2(g)+H2(g) CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4.
CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4.
下列有关说法正确的是
 CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4.
CO(g)+H2O(g),起始时投料如下表,达到平衡状态时K=4. 起始浓度(mol·L-1) | 甲 | 乙 | 丙 |
c(CO2) | 0.01 | 0.02 | 0.02 |
c(H2) | 0.01 | 0.01 | 0.02 |
A.反应CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为0.25 CO2(g)+H2(g)的平衡常数为0.25 |
| B.平衡的时间:t丙>t乙>t甲 |
| C.平衡时,CO2的转化率:乙<甲<丙 |
| D.平衡时,H2的转化率:甲=丙<乙 |
您最近一年使用:0次
2021-05-13更新
|
186次组卷
|
2卷引用:山东省淄博市沂源县第二中学2020-2021学年高二下学期期中考试化学试题
2021·河北邯郸·二模
名校
6 . 常温下,溴水与 溶液发生反应:
溶液发生反应: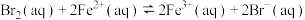 ,若开始时
,若开始时 和
和 的浓度均为
的浓度均为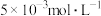 ,达到平衡时
,达到平衡时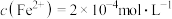 。假设溶液的体积无变化,下列有关说法错误的是
。假设溶液的体积无变化,下列有关说法错误的是
 溶液发生反应:
溶液发生反应: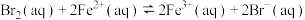 ,若开始时
,若开始时 和
和 的浓度均为
的浓度均为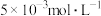 ,达到平衡时
,达到平衡时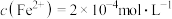 。假设溶液的体积无变化,下列有关说法错误的是
。假设溶液的体积无变化,下列有关说法错误的是A.加入 固体,平衡逆向移动 固体,平衡逆向移动 |
B.加入 振荡,平衡逆向移动,水层颜色变浅 振荡,平衡逆向移动,水层颜色变浅 |
| C.常温下,该反应的平衡常数K的值约为5.1 |
D.向经苯萃取后的水层溶液中滴加酸性 溶液,可验证该反应为可逆反应 溶液,可验证该反应为可逆反应 |
您最近一年使用:0次
2021-04-25更新
|
355次组卷
|
4卷引用:押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)
(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)河北省邯郸市2021届高三第二次模拟考试化学试题广东省深圳外国语学校2022-2023学年高二上学期期末考试化学试题湖南省泸溪县第一中学等多校联考2023-2024学年高二上学期8月月考化学试题
7 . 恒容密闭容器中充入3 mol CH4和6 mol H2S,发生反应:CH4(g)+2H2S(g) CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如图所示。下列说法错误的是
CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如图所示。下列说法错误的是

 CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如图所示。下列说法错误的是
CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如图所示。下列说法错误的是
| A.当满足v逆(H2S)=2v正(H2)时,反应达到平衡状态 |
| B.高温、低压条件有利于提高CH4的平衡转化率 |
| C.M点时,保持温度不变,继续充入3 mol CH4和6 mol H2S,达到新平衡时,CH4的物质的量分数小于H2 |
D.图中N点对应温度下,以物质的量分数表示的化学平衡常数Kx= |
您最近一年使用:0次
名校
8 . 向甲、乙两个容积均为 的恒容密闭容器中分别充入
的恒容密闭容器中分别充入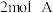 、
、 和
和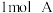 、
、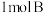 。相同条件下,发生反应
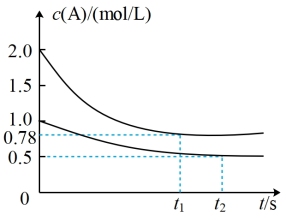
。相同条件下,发生反应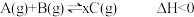 。测得两容器中
。测得两容器中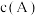 随时间t的变化关系如图所示。下列说法不正确的是
随时间t的变化关系如图所示。下列说法不正确的是
 的恒容密闭容器中分别充入
的恒容密闭容器中分别充入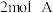 、
、 和
和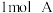 、
、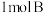 。相同条件下,发生反应
。相同条件下,发生反应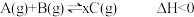 。测得两容器中
。测得两容器中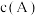 随时间t的变化关系如图所示。下列说法不正确的是
随时间t的变化关系如图所示。下列说法不正确的是
| A.x等于3 |
| B.向平衡后的乙容器中充入氦气,平衡不移动 |
C.向平衡后的乙容器中再加入 ,达到平衡后各物质的体积分数与甲容器中的相同 ,达到平衡后各物质的体积分数与甲容器中的相同 |
D.若向甲容器中再充入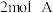 、 、 ,则达到化学平衡时甲容器中 ,则达到化学平衡时甲容器中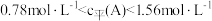 |
您最近一年使用:0次
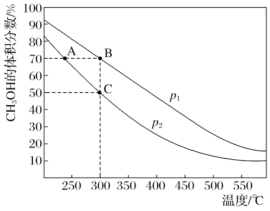
9 . CH3OH是重要的化工原料,工业上用CO与H2在催化剂作用下合成CH3OH,其反应为CO(g)+2H2(g)  CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
 CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
| A.p1<p2 |
| B.该反应的ΔH < 0 |
| C.在C点时,CO转化率为75% |
| D.平衡常数:K(A)=K(B) |
您最近一年使用:0次
名校
10 . 回收利用CO是工业生产的一项新课题,新技术研究成果甲醇与CO反应可制备乙酸,其反应为CH3OH(g)+CO(g) CH3COOH(l),测得甲醇的转化率随温度变化如图所示
CH3COOH(l),测得甲醇的转化率随温度变化如图所示
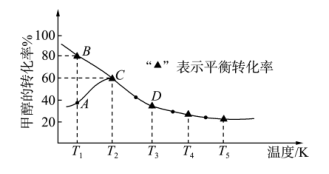
下列有关说法正确的是
 CH3COOH(l),测得甲醇的转化率随温度变化如图所示
CH3COOH(l),测得甲醇的转化率随温度变化如图所示
下列有关说法正确的是
| A.温度升高,平衡常数K增大 |
| B.温度为T1时,该反应的正反应速率:B点>A点 |
| C.缩小容器容积,既能加快反应速率,又能提高甲醇的转化率 |
| D.选择合适的催化剂可以降低反应活化能并提高平衡产率 |
您最近一年使用:0次
2021-12-03更新
|
338次组卷
|
3卷引用:山东省2021-2022学年高三上学期11月(第三次)联考化学试题



