解题方法
1 . 汽车尾气是大气中氮氧化物的主要来源。在汽车内燃机工作时,空气中的部分成分会直接生成少许 ,
, 再被氧化为
再被氧化为 。
。
(1)对内燃机中生成 的反应,下列分析正确的是_______。
的反应,下列分析正确的是_______。
(2)酸雨中的 ,可由大气中的
,可由大气中的 和
和 反应生成,对
反应生成,对 和
和 的反应,下列分析正确的是_______。
的反应,下列分析正确的是_______。
 ,
, 再被氧化为
再被氧化为 。
。(1)对内燃机中生成
 的反应,下列分析正确的是_______。
的反应,下列分析正确的是_______。| A.不属于“氮的固定” | B.涉及共价键的断裂与生成 |
| C.活化能很小 | D.在自然界中无法发生 |
 ,可由大气中的
,可由大气中的 和
和 反应生成,对
反应生成,对 和
和 的反应,下列分析正确的是_______。
的反应,下列分析正确的是_______。A. | B. 表现出了酸性氧化物的性质 表现出了酸性氧化物的性质 |
| C.需要在“放电”条件下发生 | D.氧化剂与还原剂物质的量比为1:2 |
您最近一年使用:0次
2 . 利用甲烷除去 的反应为:
的反应为: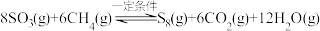 ,下列说法正确的是
,下列说法正确的是
 的反应为:
的反应为: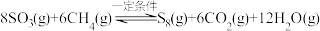 ,下列说法正确的是
,下列说法正确的是A.反应的 |
B.上述反应平衡常数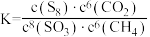 |
| C.使用高效催化剂能降低反应的焓变 |
D.其他条件不变,增大 , , 的转化率升高 的转化率升高 |
您最近一年使用:0次
3 . 神舟航天员在中国空间站进行太空实验——过饱和醋酸钠溶液结晶形成温热的“冰球”。下列说法正确的是
| A.醋酸钠是非电解质 | B.过饱和醋酸钠溶液结晶过程中 |
C.过饱和醋酸钠溶液结晶过程中 | D.向水中加入醋酸钠,水的电离被抑制 |
您最近一年使用:0次
4 . 化学与生活密切相关,下列说法正确的是
| A.用稀醋酸除去水垢中的少量硫酸钙 |
| B.加热后的纯碱溶液去除油污效果更好 |
| C.黄铜(铜锌合金)制作的铜锣易产生铜绿 |
| D.冰在室温下自动熔化成水,这是熵减的过程 |
您最近一年使用:0次
名校
5 . 治理NO的一种方法是先将NO氧化成 后,再将
后,再将 通入还原性碱溶液中电解转化成
通入还原性碱溶液中电解转化成 ,其中氧化的反应原理为
,其中氧化的反应原理为
 。下列说法正确的是
。下列说法正确的是
 后,再将
后,再将 通入还原性碱溶液中电解转化成
通入还原性碱溶液中电解转化成 ,其中氧化的反应原理为
,其中氧化的反应原理为
 。下列说法正确的是
。下列说法正确的是A.已知该反应在较低温度下能自发进行,说明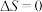 |
| B.加入催化剂,可降低反应的活化能和焓变,从而加快反应的速率 |
| C.有效碰撞理论中,活化能指活化分子平均能量与非活化分子平均能量的差值 |
D.在一定温度下,向恒容密闭容器中充入物质的量之比为 的NO和 的NO和 ,达到平衡时NO转化率为a,再充入一定量物质的量之比为 ,达到平衡时NO转化率为a,再充入一定量物质的量之比为 的NO和 的NO和 ,NO转化率不变 ,NO转化率不变 |
您最近一年使用:0次
6 . 化学与生活、生产、社会密切相关。下列说法错误的是
| A.加热食品时加热剂(生石灰和水)发生了能量变化,也伴随有物质变化 |
| B.水凝结成冰的过程中,△H<0,△S>0 |
| C.古人使用草木灰浸取液洗衣服与盐类水解原理有关 |
| D.航母上的钛合金铆钉可抗海水腐蚀 |
您最近一年使用:0次
7 . 丙烯是重要的有机化工原料,丙烷脱氢制丙烯具有显著的经济价值和社会意义。回答下列问题:
(1)已知:Ⅰ.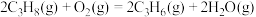
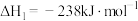
Ⅱ.
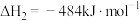
则丙烷脱氢制丙烯反应 的
的
____ ,
____ (填“>“<”或“=”)0。
(2)一定温度下,向 的密闭容器中充入
的密闭容器中充入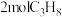 发生脱氢反应,经过
发生脱氢反应,经过 达到平衡状态,测得平衡时气体压强是开始的1.4倍。则
达到平衡状态,测得平衡时气体压强是开始的1.4倍。则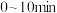 内氢气的生成速率
内氢气的生成速率
_____ , 的平衡转化率为
的平衡转化率为____ 。
(3)脱氢反应在压强分别为 和
和 时发生,丙烷及丙烯的平衡物质的量分数随温度变化如图所示。
时发生,丙烷及丙烯的平衡物质的量分数随温度变化如图所示。
_____ (填“>”或“<”) 。
。
②为了同时提高反应速率和反应物的平衡转化率,可采取的措施是______ 。
(1)已知:Ⅰ.
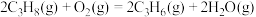
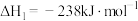
Ⅱ.

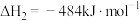
则丙烷脱氢制丙烯反应
 的
的

(2)一定温度下,向
 的密闭容器中充入
的密闭容器中充入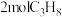 发生脱氢反应,经过
发生脱氢反应,经过 达到平衡状态,测得平衡时气体压强是开始的1.4倍。则
达到平衡状态,测得平衡时气体压强是开始的1.4倍。则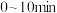 内氢气的生成速率
内氢气的生成速率
 的平衡转化率为
的平衡转化率为(3)脱氢反应在压强分别为
 和
和 时发生,丙烷及丙烯的平衡物质的量分数随温度变化如图所示。
时发生,丙烷及丙烯的平衡物质的量分数随温度变化如图所示。

 。
。②为了同时提高反应速率和反应物的平衡转化率,可采取的措施是
您最近一年使用:0次
名校
解题方法
8 . 以水为原料,通过铁氧化物进行循环制氢,示意图如图。_______ 。若反应Ⅰ生成了标准状况下 的
的 ,则反应中转移的电子数目为
,则反应中转移的电子数目为_______ mol。
2.科学家用钴氧化物进行循环制氢,制氢过程中涉及 的化学反应,该反应的
的化学反应,该反应的 值与温度(K)的关系如图所示。下列判断正确的是_______。
值与温度(K)的关系如图所示。下列判断正确的是_______。

 的
的 ,则反应中转移的电子数目为
,则反应中转移的电子数目为2.科学家用钴氧化物进行循环制氢,制氢过程中涉及
 的化学反应,该反应的
的化学反应,该反应的 值与温度(K)的关系如图所示。下列判断正确的是_______。
值与温度(K)的关系如图所示。下列判断正确的是_______。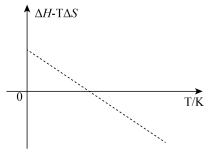
A. , , | B. , , |
C. , , | D. , , |
您最近一年使用:0次
解题方法
9 . CO2的综合利用与工业合成氨:综合利用CO2、CO对实现“零排放”有重要意义。CH4-CO2催化重整是CO2利用的研究热点之一、其主要反应原理为: 。
。
已知:①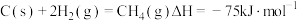 。
。
②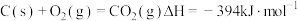 。
。
③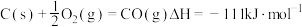 。
。
(1)固态CO2属于_______晶体,当它升华时,其中_______作用力发生了变化_______ 。
A.分子 共价键 B.分子 范德华力 C.共价 共价键
(2)根据盖斯定律,该催化重整反应的
_______  。写出该催化重整反应的平衡常数表达式
。写出该催化重整反应的平衡常数表达式
_______ 。
A.+247 B.-247 C.+358 D.-358
(3)请判断反应②常温下是否可自发进行?_______ (填可或不可)自发进行,并写出判断依据:_______ 。
(4)某温度下,在体积为2L的容器中加入1molCH4、2molCO2以及催化剂进行重整反应,10min时测得生成的CO是0.5mol。则0~10min内的平均反应速率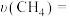
_______ 。
(5)若要加快CO的生成速率同时有利于提高CH4平衡转化率的条件是_______。
 。
。已知:①
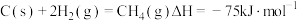 。
。②
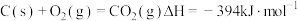 。
。③
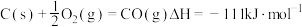 。
。(1)固态CO2属于_______晶体,当它升华时,其中_______作用力发生了变化
A.分子 共价键 B.分子 范德华力 C.共价 共价键
(2)根据盖斯定律,该催化重整反应的

 。写出该催化重整反应的平衡常数表达式
。写出该催化重整反应的平衡常数表达式
A.+247 B.-247 C.+358 D.-358
(3)请判断反应②常温下是否可自发进行?
(4)某温度下,在体积为2L的容器中加入1molCH4、2molCO2以及催化剂进行重整反应,10min时测得生成的CO是0.5mol。则0~10min内的平均反应速率
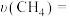
(5)若要加快CO的生成速率同时有利于提高CH4平衡转化率的条件是_______。
| A.高温 | B.高压 | C.使用催化剂 | D.增大 浓度 浓度 |
您最近一年使用:0次
10 . 五氧化二碘( )是一种重要的工业试剂,常温下为白色针状晶体,可作氧化剂除去气体中的一氧化碳。
)是一种重要的工业试剂,常温下为白色针状晶体,可作氧化剂除去气体中的一氧化碳。
已知:
反应I: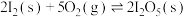


反应II: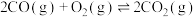


反应III: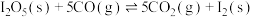


回答下列问题:
(1)对于反应I、II、III;
①
___________ (用含 、
、 的代数式表示),
的代数式表示),
___________ (用含 、
、 的代数式表示)。
的代数式表示)。
②查阅资料可知,对于反应I, ,在
,在___________ (填“低温”“高温”或“任意温度”)下有利于该反应自发进行,判断的理由为___________ 。
(2) ℃时向盛有足量
℃时向盛有足量 (s)的VL恒容密闭容器中通入1.6molCO,此时压强为p,仅发生反应Ⅲ(该反应为放热反应)。
(s)的VL恒容密闭容器中通入1.6molCO,此时压强为p,仅发生反应Ⅲ(该反应为放热反应)。
①下列关于反应III的说法错误的是___________ (填标号)。
A.加入合适的催化剂,可实现CO的完全转化
B.该反应的反应物的能量总和大于生成物的能量总和
C.保持其他条件不变,仅适当降低温度,该反应的平衡常数增大
D.保持其他条件不变,仅适当增大压强, 的大小不发生改变
的大小不发生改变
② ℃时,若反应达到平衡后固体质量减小19.2g,该反应的平衡常数
℃时,若反应达到平衡后固体质量减小19.2g,该反应的平衡常数
___________ (分压=总压×物质的量分数);CO的平衡转化率随 的移出率[
的移出率[ 的移出率=
的移出率=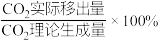 ]变化关系如,则a=
]变化关系如,则a=___________ ,b=___________ (保留3位有效数字)。
 )是一种重要的工业试剂,常温下为白色针状晶体,可作氧化剂除去气体中的一氧化碳。
)是一种重要的工业试剂,常温下为白色针状晶体,可作氧化剂除去气体中的一氧化碳。已知:
反应I:
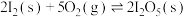


反应II:
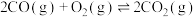


反应III:
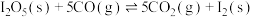


回答下列问题:
(1)对于反应I、II、III;
①

 、
、 的代数式表示),
的代数式表示),
 、
、 的代数式表示)。
的代数式表示)。②查阅资料可知,对于反应I,
 ,在
,在(2)
 ℃时向盛有足量
℃时向盛有足量 (s)的VL恒容密闭容器中通入1.6molCO,此时压强为p,仅发生反应Ⅲ(该反应为放热反应)。
(s)的VL恒容密闭容器中通入1.6molCO,此时压强为p,仅发生反应Ⅲ(该反应为放热反应)。①下列关于反应III的说法错误的是
A.加入合适的催化剂,可实现CO的完全转化
B.该反应的反应物的能量总和大于生成物的能量总和
C.保持其他条件不变,仅适当降低温度,该反应的平衡常数增大
D.保持其他条件不变,仅适当增大压强,
 的大小不发生改变
的大小不发生改变②
 ℃时,若反应达到平衡后固体质量减小19.2g,该反应的平衡常数
℃时,若反应达到平衡后固体质量减小19.2g,该反应的平衡常数
 的移出率[
的移出率[ 的移出率=
的移出率=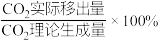 ]变化关系如,则a=
]变化关系如,则a=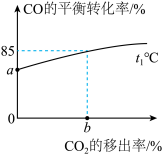
您最近一年使用:0次



