名校
解题方法
1 . 下列说法正确的是
| A.在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 |
| B.NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57 kJ•mol-1,能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
您最近一年使用:0次
2 . 关节炎是因为在关节滑液中形成了尿酸钠晶体,尤其是在寒冷季节易诱发关节疼痛。其化学机理如下:①Hur(尿酸) H++Ur-(尿酸根离子),②Ur-(aq)+Na+(aq)
H++Ur-(尿酸根离子),②Ur-(aq)+Na+(aq) NaUr(s)。下列对反应②的叙述正确的是
NaUr(s)。下列对反应②的叙述正确的是
 H++Ur-(尿酸根离子),②Ur-(aq)+Na+(aq)
H++Ur-(尿酸根离子),②Ur-(aq)+Na+(aq) NaUr(s)。下列对反应②的叙述正确的是
NaUr(s)。下列对反应②的叙述正确的是| A.该反应为熵增的反应 | B.升高温度,平衡向正反应方向移动 |
| C.正反应为放热反应 | D.降低温度,正反应速率减小,逆反应速率增大 |
您最近一年使用:0次
解题方法
3 . 工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为: 。
。
回答下列问题:
(1)合成氨反应在常温下___________ (填“能”或“不能”)自发。
(2)___________ 温(填“高”或“低”,下同)有利于提高反应速率,___________ 温有利于提高平衡转化率,综合考虑催化剂(铁触媒)活性等因素,工业常采用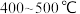 。
。
(3)传统催化剂用的是铁触媒,合成氨反应在 催化剂上可能通过以下机理进行(*表示催化剂表面吸附位,
催化剂上可能通过以下机理进行(*表示催化剂表面吸附位,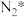 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
)判断上述反应机理中,速率控制步骤(即速率最慢步骤)为___________ (填步骤前的标号),理由是___________ 。
(i)
(ii)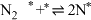
(iii)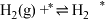
(iv)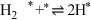
(v)
……
(…)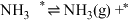
(4)针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
方案一:双温-双控-双催化剂。使用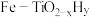 双催化剂,通过光辐射产生温差(如体系温度为
双催化剂,通过光辐射产生温差(如体系温度为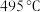 时,
时, 的温度为
的温度为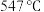 ,而
,而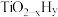 的温度为
的温度为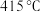 )。
)。

下列说法正确的是___________ 。
a.氨气在“冷 ”表面生成,有利于提高氨的平衡产率
”表面生成,有利于提高氨的平衡产率
b. 在“热
在“热 ”表面断裂,有利于提高合成氨反应速率
”表面断裂,有利于提高合成氨反应速率
c.“热 ”高于体系温度,有利于提高氨的平衡产率
”高于体系温度,有利于提高氨的平衡产率
d.“冷 ”低于体系温度,有利于提高合成氨反应速率
”低于体系温度,有利于提高合成氨反应速率
(5)方案二: 复合催化剂。
复合催化剂。
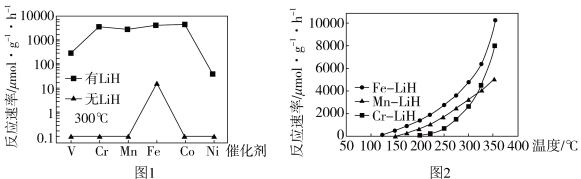
下列说法正确的是___________ 。
a. 时,复合催化剂比单一催化剂效率更高
时,复合催化剂比单一催化剂效率更高
b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高
(6)某合成氨速率方程为: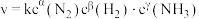 ,根据表中数据,
,根据表中数据,
___________ ;
在合成氨过程中,需要不断分离出氨的原因为___________ 。
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
 。
。回答下列问题:
(1)合成氨反应在常温下
(2)
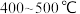 。
。(3)传统催化剂用的是铁触媒,合成氨反应在
 催化剂上可能通过以下机理进行(*表示催化剂表面吸附位,
催化剂上可能通过以下机理进行(*表示催化剂表面吸附位,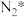 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
)判断上述反应机理中,速率控制步骤(即速率最慢步骤)为(i)

(ii)
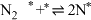
(iii)
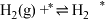
(iv)
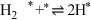
(v)

……
(…)
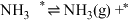
(4)针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
方案一:双温-双控-双催化剂。使用
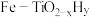 双催化剂,通过光辐射产生温差(如体系温度为
双催化剂,通过光辐射产生温差(如体系温度为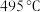 时,
时, 的温度为
的温度为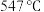 ,而
,而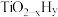 的温度为
的温度为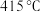 )。
)。
下列说法正确的是
a.氨气在“冷
 ”表面生成,有利于提高氨的平衡产率
”表面生成,有利于提高氨的平衡产率b.
 在“热
在“热 ”表面断裂,有利于提高合成氨反应速率
”表面断裂,有利于提高合成氨反应速率c.“热
 ”高于体系温度,有利于提高氨的平衡产率
”高于体系温度,有利于提高氨的平衡产率d.“冷
 ”低于体系温度,有利于提高合成氨反应速率
”低于体系温度,有利于提高合成氨反应速率(5)方案二:
 复合催化剂。
复合催化剂。
下列说法正确的是
a.
 时,复合催化剂比单一催化剂效率更高
时,复合催化剂比单一催化剂效率更高b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高
(6)某合成氨速率方程为:
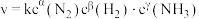 ,根据表中数据,
,根据表中数据,
| 实验 | 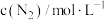 | 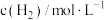 | 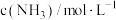 |  |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 2.828q |
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
您最近一年使用:0次
解题方法
4 . 氯及其化合物在工业生产中具有很重要的作用。
(1)舍勒制氯气的方法至今仍是实验室制氯气的常用方法,其离子方程式为:_______ 。制得的 中有大量的
中有大量的 气体,通入饱和食盐水可除去
气体,通入饱和食盐水可除去 ,且溶液中有白色固体产生,这个固体是
,且溶液中有白色固体产生,这个固体是_______ (填化学式)。
(2) 可用于生产一种化工产品
可用于生产一种化工产品 。已知有关反应如下:
。已知有关反应如下:
①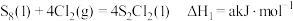
②
③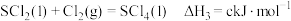
④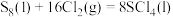
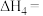
_______  (用含
(用含 和
和 的式子表示)。已知
的式子表示)。已知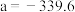 ,则反应①
,则反应①_______ (填字母)
A.一定自发 B.一定不自发 C.高温自发 D.低温自发
(3) 还可在工业上用于生产亚硝酰氯:
还可在工业上用于生产亚硝酰氯: 。
。 时,在
时,在 密闭容器中充入
密闭容器中充入
 与
与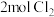 ,一段时间后反应达到平衡。
,一段时间后反应达到平衡。
①该反应达到化学平衡的标志有_______ (填字母)。
A.单位时间内消耗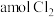 的同时,生成
的同时,生成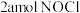
B.容器内总压强不再变化
C.混合气体的密度保持不变
D.混合气体的平均相对分子质量保持不变
E.NO与NOCl的体积分数相等
②已知上述反应中正、逆反应速率的表达式为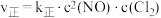 、
、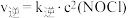 ,
, 、
、 变化如图所示,则该反应
变化如图所示,则该反应
_______ 0(填“>”、“<”)。 时,
时, 平衡转化率为
平衡转化率为 ,则
,则 与
与 的比值为
的比值为_______ 。
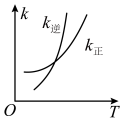
③若在温度为 ,容积为
,容积为 的容器中,充入
的容器中,充入 、
、 、
、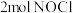 ,则
,则
_______  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
(4)氯气—铝电池是一种新型的燃料电池,若电解质溶液为 溶液,电极分别用铝条和碳棒,负极反应为
溶液,电极分别用铝条和碳棒,负极反应为_______ 。
(1)舍勒制氯气的方法至今仍是实验室制氯气的常用方法,其离子方程式为:
 中有大量的
中有大量的 气体,通入饱和食盐水可除去
气体,通入饱和食盐水可除去 ,且溶液中有白色固体产生,这个固体是
,且溶液中有白色固体产生,这个固体是(2)
 可用于生产一种化工产品
可用于生产一种化工产品 。已知有关反应如下:
。已知有关反应如下:①
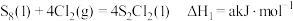
②

③
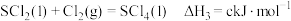
④
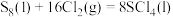
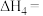
 (用含
(用含 和
和 的式子表示)。已知
的式子表示)。已知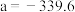 ,则反应①
,则反应①A.一定自发 B.一定不自发 C.高温自发 D.低温自发
(3)
 还可在工业上用于生产亚硝酰氯:
还可在工业上用于生产亚硝酰氯: 。
。 时,在
时,在 密闭容器中充入
密闭容器中充入
 与
与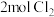 ,一段时间后反应达到平衡。
,一段时间后反应达到平衡。①该反应达到化学平衡的标志有
A.单位时间内消耗
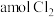 的同时,生成
的同时,生成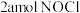
B.容器内总压强不再变化
C.混合气体的密度保持不变
D.混合气体的平均相对分子质量保持不变
E.NO与NOCl的体积分数相等
②已知上述反应中正、逆反应速率的表达式为
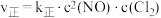 、
、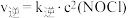 ,
, 、
、 变化如图所示,则该反应
变化如图所示,则该反应
 时,
时, 平衡转化率为
平衡转化率为 ,则
,则 与
与 的比值为
的比值为
③若在温度为
 ,容积为
,容积为 的容器中,充入
的容器中,充入 、
、 、
、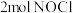 ,则
,则
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。(4)氯气—铝电池是一种新型的燃料电池,若电解质溶液为
 溶液,电极分别用铝条和碳棒,负极反应为
溶液,电极分别用铝条和碳棒,负极反应为
您最近一年使用:0次
5 . 关于反应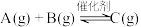
 ,下列说法正确的是
,下列说法正确的是
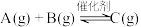
 ,下列说法正确的是
,下列说法正确的是| A.一定是自发反应 |
| B.温度升高,逆反应速率减慢 |
| C.反应物浓度增大,平衡向正反应方向进行 |
| D.催化剂不参与化学反应 |
您最近一年使用:0次
名校
6 . 2023年9月23日,杭州亚运会主火炬塔使用了燃烧高效、排放清洁、可再生、运输便捷的甲醇燃料,这是人类历史上第一次废碳再生利用,有利于推进“碳达峰”和“碳中和”。工业上用 来生产燃料甲醇的反应为
来生产燃料甲醇的反应为
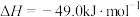 ,现将
,现将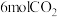 和
和 充入
充入 的恒温刚性密闭容器中,测得的氢气物质的量随时间变化如图中实线所示:
的恒温刚性密闭容器中,测得的氢气物质的量随时间变化如图中实线所示:
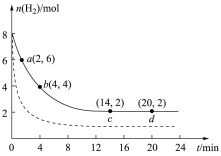
回答下列问题:
(1)该反应在
(2)下列说法不能表明该反应已经达到平衡状态的是_______(填选项字母)。
| A.压强保持不变 |
| B.混合气体的平均相对分子质量不变 |
C.混合气体中 的百分含量保持不变 的百分含量保持不变 |
D. |
(3)
 点正反应速率
点正反应速率 点逆反应速率,前
点逆反应速率,前 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为(4)平衡时
 的转化率为
的转化率为
 。
。(5)仅改变某一实验条件再进行实验,测得
 的物质的量随时间变化如图中虚线所示,对应的实验条件改变的是
的物质的量随时间变化如图中虚线所示,对应的实验条件改变的是(6)如果要加快反应速率并且提高
 平衡转化率,可以采取的措施有
平衡转化率,可以采取的措施有(7)一定条件下,单位时间内不同温度下测定的
 转化率如图所示。温度高于
转化率如图所示。温度高于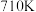 时,随温度的升高
时,随温度的升高 转化率降低的原因可能是
转化率降低的原因可能是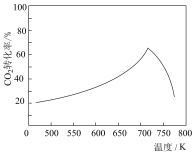
您最近一年使用:0次
7 . 究二氧化碳的回收对我国2060年实现碳中和具有现实意义:
(1)已知:①CO(g)+H2O(g) CO2(g)+H2(g) △H=-41kJ•mol-1
CO2(g)+H2(g) △H=-41kJ•mol-1
②C(s)+2H2(g) CH4(g) △H=-73kJ•mol-1
CH4(g) △H=-73kJ•mol-1
③2CO(g) CO2(g)+C(s) △H=-171kJ•mol-1
CO2(g)+C(s) △H=-171kJ•mol-1
写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:______ 。
(2)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) △H。
C2H5OH(g)+3H2O(g) △H。
①通过表格中的数值可以推断:其正反应在_____ (填“高温”、“低温”或“任何温度”)下能自发进行。
②CO2的平衡转化率与压强、温度及氢碳比m[m= ]的关系分别如图a和图b所示。
]的关系分别如图a和图b所示。
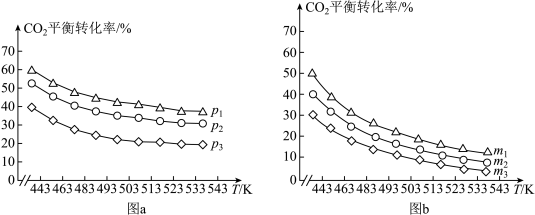
图a中压强从大到小的顺序为_____ ,图b中氢碳比m从大到小的顺序为_____ 。
(3)工业上也可以利用CO2和H2合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)某1L恒温恒容密闭容器中充入1molCO2和3molH2发生反应,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示:
CH3OH(g)+H2O(g)某1L恒温恒容密闭容器中充入1molCO2和3molH2发生反应,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示:
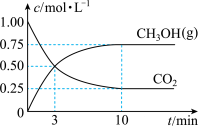
①0~3min内,H2的平均反应速率为_____ mol•L-1•min-1,该温度下的平衡常数为K=_____ (单位可忽略)。若达平衡时,保持温度不变,向容器中再充入CO2、H2、CH3OH和H2O各0.25mol,则此时v正_____ v逆(填“>”、“<”、或“=”)。
②下列说法能说明反应达到化学平衡状态的是_____ 。
A.H2的消耗速率与CH3OH的消耗速率之比为3∶1 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.c(CO2)和c(H2O)的浓度相等时
(4)盖斯定律认为:不管化学过程是一步完成或分几步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①已知:H2O(g)=H2O(l) △H1=-Q1kJ/mol
C2H5OH(g)=C2H5OH(l) △H2=-Q2kJ/mol
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3kJ/mol
若使46g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为______ kJ。
②碳(s)在氧气供应不充足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应:C(s)+ O2(g)=CO(g)的△H。但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有
O2(g)=CO(g)的△H。但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有______ 。
(1)已知:①CO(g)+H2O(g)
 CO2(g)+H2(g) △H=-41kJ•mol-1
CO2(g)+H2(g) △H=-41kJ•mol-1②C(s)+2H2(g)
 CH4(g) △H=-73kJ•mol-1
CH4(g) △H=-73kJ•mol-1③2CO(g)
 CO2(g)+C(s) △H=-171kJ•mol-1
CO2(g)+C(s) △H=-171kJ•mol-1写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:
(2)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g) △H。
C2H5OH(g)+3H2O(g) △H。| 温度/ | 400 | 500 |
| 平衡常数K | 9 | 5.3 |
②CO2的平衡转化率与压强、温度及氢碳比m[m=
 ]的关系分别如图a和图b所示。
]的关系分别如图a和图b所示。
图a中压强从大到小的顺序为
(3)工业上也可以利用CO2和H2合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)某1L恒温恒容密闭容器中充入1molCO2和3molH2发生反应,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示:
CH3OH(g)+H2O(g)某1L恒温恒容密闭容器中充入1molCO2和3molH2发生反应,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示:
①0~3min内,H2的平均反应速率为
②下列说法能说明反应达到化学平衡状态的是
A.H2的消耗速率与CH3OH的消耗速率之比为3∶1 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.c(CO2)和c(H2O)的浓度相等时
(4)盖斯定律认为:不管化学过程是一步完成或分几步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①已知:H2O(g)=H2O(l) △H1=-Q1kJ/mol
C2H5OH(g)=C2H5OH(l) △H2=-Q2kJ/mol
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3kJ/mol
若使46g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为
②碳(s)在氧气供应不充足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应:C(s)+
 O2(g)=CO(g)的△H。但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有
O2(g)=CO(g)的△H。但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有
您最近一年使用:0次
8 . 已知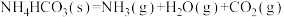
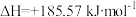 ,下列说法中正确的是
,下列说法中正确的是
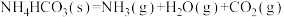
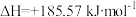 ,下列说法中正确的是
,下列说法中正确的是| A.该反应任何温度下都不能自发进行 |
| B.该反应能自发进行,由于该反应是一个熵增加的反应 |
| C.其他条件不变,使用催化剂可以改变化学反应进行的方向 |
| D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
您最近一年使用:0次
名校
解题方法
9 . 杭州亚运会主火炬的燃料首次使用废碳再生的绿色甲醇,甲醇火炬被称为“零碳”火炬。目前,我国在相关设备及技术方面全球领先。请回答:
(1)二氧化碳催化加氢制甲醇的反应可表示为: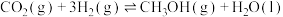 。
。
①已知: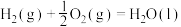
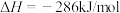


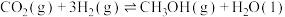
 =
=______ kJ/mol。该反应能自发进行的条件是______ 。
②在恒容条件下能加快二氧化碳催化加氢制甲醇的反应速率,并提高 转化率的措施是
转化率的措施是______ 。
③若二氧化碳催化加氢制甲醇的反应在恒温恒容的密闭容器中进行,能说明反应达到平衡状态的是______ ,(填字母)。
A.容器内压强不随时间变化 B.容器内各物质的浓度相等
C.单位时间消耗1mol ,同时生成3mol
,同时生成3mol D.混合气体的密度不再改变
D.混合气体的密度不再改变
(2)电催化法是制备甲醇的途径之一,原理如图所示。

①室温下, 溶液
溶液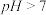 ,
, 水解的离子方程式为
水解的离子方程式为______ 。
② 电极的电极反应式为
电极的电极反应式为______ 。
③与其他有机合成相比,电有机合成的优点是______ 。
(1)二氧化碳催化加氢制甲醇的反应可表示为:
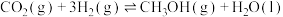 。
。①已知:
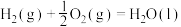
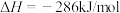


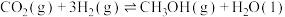
 =
=②在恒容条件下能加快二氧化碳催化加氢制甲醇的反应速率,并提高
 转化率的措施是
转化率的措施是③若二氧化碳催化加氢制甲醇的反应在恒温恒容的密闭容器中进行,能说明反应达到平衡状态的是
A.容器内压强不随时间变化 B.容器内各物质的浓度相等
C.单位时间消耗1mol
 ,同时生成3mol
,同时生成3mol D.混合气体的密度不再改变
D.混合气体的密度不再改变(2)电催化法是制备甲醇的途径之一,原理如图所示。

①室温下,
 溶液
溶液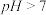 ,
, 水解的离子方程式为
水解的离子方程式为②
 电极的电极反应式为
电极的电极反应式为③与其他有机合成相比,电有机合成的优点是
您最近一年使用:0次
10 . 1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才,现将1molN2和3molH2投入1L的密闭容器,在一定条件下,利用反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H<0. 回答下列问题:
H<0. 回答下列问题:
(1)合成氨反应平衡常数的表达式为_______ 。温度升高,K值_______ (填“增大”“减小”或“不变"):使用催化剂,K值_______ (填“增大“减小”或“不变”)。
(2)反应的 S
S_______ 0(填“>”“<"或“=”)
(3)有利于提高平衡混合物中氨含量的条件有_______ (填序号)。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡_______ 移动(填“正向”“逆向”或“不”);给体系升温,
_______ (填“增大”“减小”或不变”),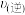
_______ (填“增大”“减小”或“不变”),平衡_______ 移动(填“正向”“逆向”或“不”)。
 2NH3(g)
2NH3(g)  H<0. 回答下列问题:
H<0. 回答下列问题:(1)合成氨反应平衡常数的表达式为
(2)反应的
 S
S(3)有利于提高平衡混合物中氨含量的条件有
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡

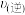
您最近一年使用:0次



