名校
1 . 哈伯法合成氨技术是德国诺贝尔化学奖获得者哈伯发明的。其合成原理为:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H<0,
H<0, S<0。下列有关工业合成氨的说法正确的是
S<0。下列有关工业合成氨的说法正确的是
 2NH3(g)
2NH3(g)  H<0,
H<0, S<0。下列有关工业合成氨的说法正确的是
S<0。下列有关工业合成氨的说法正确的是A.因为 H<0,所以该反应一定能自发进行 H<0,所以该反应一定能自发进行 |
B.因为 S<0,所以该反应一定不能自发进行 S<0,所以该反应一定不能自发进行 |
| C.在低温下进行是为了提高反应物的转化率 |
| D.使用催化剂加快反应速率是因为催化剂降低了反应的活化能 |
您最近一年使用:0次
名校
2 . 工业上以CO2和NH3为原料合成尿素,在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1
H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1
反应Ⅱ:H2NCOONH4(s) CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;
CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ∆H3
CO(NH2)2(s)+H2O(g) ∆H3
(1)反应Ⅰ的熵变ΔS___________  填“
填“ ”“
”“ ”或“
”或“ ”
” 。反应Ⅲ的
。反应Ⅲ的 H3=
H3=___________ ,反应Ⅲ自发进行的条件是___________ (填“低温”、“高温”、“任何温度”)。
(2)下列关于尿素合成的说法正确的是___________。
(3)1mol CO(NH2)2(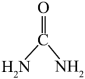 )中含有
)中含有___________ molπ键。NH 离子的VSEPR模型是
离子的VSEPR模型是___________ ,空间构型是___________ 。
(4)对于尿素分子中N、O两种基态原子,下列说法正确的是___________。
反应Ⅰ:2NH3(g)+CO2(g)
 H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1
H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1反应Ⅱ:H2NCOONH4(s)
 CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;
CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;总反应Ⅲ:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ∆H3
CO(NH2)2(s)+H2O(g) ∆H3(1)反应Ⅰ的熵变ΔS
 填“
填“ ”“
”“ ”或“
”或“ ”
” 。反应Ⅲ的
。反应Ⅲ的 H3=
H3=(2)下列关于尿素合成的说法正确的是___________。
| A.及时分离出尿素可促使反应Ⅱ向正反应方向移动 |
| B.从合成塔出来的混合气体分离出水蒸气后其余气体可以循环使用 |
| C.保持容积不变,充入惰性气体增大压强,可提高总反应Ⅲ的反应速率 |
| D.保持压强不变,降低氨碳比[n(NH3)/n(CO2)]可提高反应Ⅰ中NH3的平衡转化率 |
 )中含有
)中含有 离子的VSEPR模型是
离子的VSEPR模型是(4)对于尿素分子中N、O两种基态原子,下列说法正确的是___________。
| A.N的半径较小 | B.N的未成对电子数较多 |
| C.N的电负性较大 | D.N的第一电离能较高 |
您最近一年使用:0次
名校
解题方法
3 . 灰锡结构松散,不能用于制造器皿。现把白锡制造的器皿在0℃、100kPa环境下存放,它会不会变成灰锡而不能继续使用呢?(已知在0℃、100kPa条件下白锡转化为灰锡的反应的焓变和熵变分别为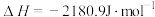 ,
, ,当
,当 时能自发反应)
时能自发反应)
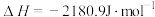 ,
, ,当
,当 时能自发反应)
时能自发反应)| A.会变 | B.不会变 | C.不能确定 | D.升高温度才会变 |
您最近一年使用:0次
解题方法
4 . 下列内容与结论相对应的是
| 选项 | 内容 | 结论 |
| A |  | 该过程的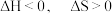 |
| B | 常温下,硝酸铵固体溶于水可自发进行 | 该过程的 |
| C | 一个反应的 | 反应一定不能自发进行 |
| D |  能自发进行 能自发进行 | 则该反应的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 光催化是新发展的一个催化技术,TiO2是目前研究成功的应用广泛的光催化剂,它是由金红石矿(主要成分为TiO2)先制备为TiCl4,再转化为纯TiO2。
请根据表中数据作答:
(1)计算反应:TiO2(s) + 2Cl2(g)= TiCl4(g) + O2(g) 298K的ΔrΗΘm和ΔrSΘm,该反应能否正向进行___________ ?
(2)计算反应2C(s) + O2(g) = 2CO(g) 298K的ΔrΗΘm和ΔrSΘm,并判据反应在298K进行的方向___________ 。
(3)为得到纯的TiCl4,有人设计如下方案:TiO2(s) + 2Cl2(g) + 2C(s) = TiCl4(g ) + 2CO(g)。计算该反应298K的ΔrΗΘm和ΔrSΘm,并判据反应进行的方向___________ 。
| 物种 | TiO2(s) | TiCl4(g) | Cl2(g) | O2(g) | C(s) | CO(g) |
| ΔrΗΘm /kJ∙molˉ1 | –944.7 | –763.2 | 0 | 0 | 0 | –110.5 |
| SΘm/J∙molˉ1∙Kˉ1 | 55.02 | 354.9 | 223.1 | 205.1 | 5.74 | 197.7 |
(1)计算反应:TiO2(s) + 2Cl2(g)= TiCl4(g) + O2(g) 298K的ΔrΗΘm和ΔrSΘm,该反应能否正向进行
(2)计算反应2C(s) + O2(g) = 2CO(g) 298K的ΔrΗΘm和ΔrSΘm,并判据反应在298K进行的方向
(3)为得到纯的TiCl4,有人设计如下方案:TiO2(s) + 2Cl2(g) + 2C(s) = TiCl4(g ) + 2CO(g)。计算该反应298K的ΔrΗΘm和ΔrSΘm,并判据反应进行的方向
您最近一年使用:0次
名校
6 . 可以利用 反应制备H2和CO,下列说法正确的是
反应制备H2和CO,下列说法正确的是
 反应制备H2和CO,下列说法正确的是
反应制备H2和CO,下列说法正确的是| A.该反应△S>0 |
B.反应的平衡常数表达式为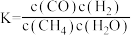 |
| C.上述反应中消耗1molCH4,转移电子的数目约为2×6.02×1023 |
| D.其他条件相同时,增大压强,可以提高CH4的平衡转化率 |
您最近一年使用:0次
名校
7 . 下列说法正确的是
A.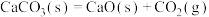 室温下不能自发进行,说明该反应的 室温下不能自发进行,说明该反应的 |
B.10mL浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的 固体,能减小反应速率但又不影响氢气产量 固体,能减小反应速率但又不影响氢气产量 |
C.500°C、30MPa下,0.5mol  (g)和1.5mol (g)和1.5mol  (g)反应生成 (g)反应生成 (g)放热Q kJ,其热化学方程式为 (g)放热Q kJ,其热化学方程式为  |
| D.增大压强(对于气体反应),活化分子百分数增大,故反应速率增大 |
您最近一年使用:0次
名校
8 . 金属硫化物(MxSy)催化反应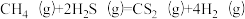 ,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
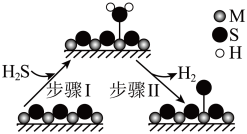
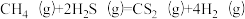 ,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
A.该反应的 S<0 S<0 |
B.该反应的平衡常数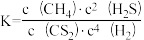 |
| C.其他条件相同,增大体系压强,能提高H2S的平衡转化率 |
| D.题图所示的反应机理中,步骤I可理解为H2S中带部分负电荷的S与催化剂中的M之间发生作用 |
您最近一年使用:0次
名校
解题方法
9 . 下列说法正确的是
A.25℃时,0.1 的醋酸溶液加水稀释,所有离子的浓度均减小 的醋酸溶液加水稀释,所有离子的浓度均减小 |
B.保持温度不变,向稀氨水中缓慢通入 ,溶液中 ,溶液中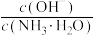 的值减少 的值减少 |
C.反应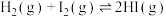 达平衡时,将容积缩小一半,混合气体颜色不变 达平衡时,将容积缩小一半,混合气体颜色不变 |
D.反应 在一定条件下能自发进行,该反应一定为放热反应 在一定条件下能自发进行,该反应一定为放热反应 |
您最近一年使用:0次
名校
10 . 由铁及其化合物可制得FeSO4·7H2O、FeCl3、K2FeO4等化工产品,它们在生产、生活中具有 广泛应用。高炉炼铁的反应为 Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1,对于该反应下列有关说法正确的是
2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1,对于该反应下列有关说法正确的是
 2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1,对于该反应下列有关说法正确的是
2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1,对于该反应下列有关说法正确的是| A.若该反应一定能自发进行,则该反应的ΔS>0 |
| B.升高温度使反应物活化分子数增多,能提高反应速率和CO平衡转化率 |
| C.增加炼铁炉高度,延长CO和铁矿石接触时间,能降低平衡时尾气中CO的体积分数 |
| D.制备的生铁中含少量FexC,相同条件下与酸反应放出氢气的速率比纯铁快 |
您最近一年使用:0次



