名校
1 . 丙烯是三大合成材料的基本原料之一,大量用于生产聚丙烯等。丙烷脱氢制丙烯包含的反应如下:
主反应a.C3H8(g) C3H6(g)+H2(g) △H1=+124.3kJ·mol-1
C3H6(g)+H2(g) △H1=+124.3kJ·mol-1
副反应b.C3H8(g) CH4(g)+C2H4(g) △H2=+98.9kJ·mol-1
CH4(g)+C2H4(g) △H2=+98.9kJ·mol-1
c.C3H8(g)+H2(g) C2H6(g)+CH4(g) △H3=-37.7kJ·mol-1
C2H6(g)+CH4(g) △H3=-37.7kJ·mol-1
d.C2H4(g)+H2(g) C2H6(g) △H4
C2H6(g) △H4
回答下列问题:
(1)△H4=____ kJ·mol-1。
(2)向密闭容器中充入1molC3H8,反应a~d的△G(体系自由能变,△G=△H-T△S,△G<0时反应自发进行)和压强为1atm时LnKp[Kp是以分压表示的平衡常数,分压=总压(1atm)×物质的量分数]与温度的关系分别如图1、2所示:
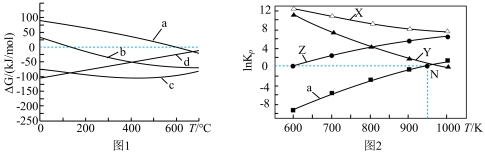
①结合图1,500℃时不能自发进行的反应是____ (填标号);随温度升高,反应b、d的自由能变在相同温度下,400℃前△G2>△G4,400℃后△G2<△G4,导致该变化的原因是△H2>△H4,和____ 。
②图2中X表示的反应是____ (填标号);若不考虑副反应的影响,反应a在N点时C3H8的平衡转化率为____  (结果保留小数点后一位)。
(结果保留小数点后一位)。
(3)目前工业生产中通常采用高温低压并充入CO2的方法制丙烯,采用高温低压的原因是____ 。
主反应a.C3H8(g)
 C3H6(g)+H2(g) △H1=+124.3kJ·mol-1
C3H6(g)+H2(g) △H1=+124.3kJ·mol-1副反应b.C3H8(g)
 CH4(g)+C2H4(g) △H2=+98.9kJ·mol-1
CH4(g)+C2H4(g) △H2=+98.9kJ·mol-1c.C3H8(g)+H2(g)
 C2H6(g)+CH4(g) △H3=-37.7kJ·mol-1
C2H6(g)+CH4(g) △H3=-37.7kJ·mol-1d.C2H4(g)+H2(g)
 C2H6(g) △H4
C2H6(g) △H4回答下列问题:
(1)△H4=
(2)向密闭容器中充入1molC3H8,反应a~d的△G(体系自由能变,△G=△H-T△S,△G<0时反应自发进行)和压强为1atm时LnKp[Kp是以分压表示的平衡常数,分压=总压(1atm)×物质的量分数]与温度的关系分别如图1、2所示:

①结合图1,500℃时不能自发进行的反应是
②图2中X表示的反应是
 (结果保留小数点后一位)。
(结果保留小数点后一位)。(3)目前工业生产中通常采用高温低压并充入CO2的方法制丙烯,采用高温低压的原因是
您最近一年使用:0次
2022-06-18更新
|
121次组卷
|
2卷引用:河南省安阳市2021-2022学年高二下学期阶段性测试(五)化学试题
2 . 钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 ,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
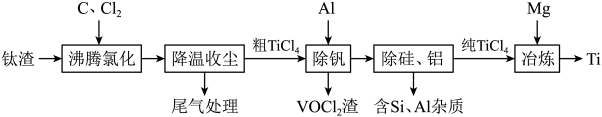
已知“降温收尘”后,粗 中含有的几种物质的沸点:
中含有的几种物质的沸点:
回答下列问题:
(1)已知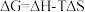 ,
, 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略 、
、 随温度的变化。若
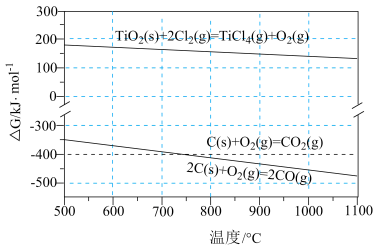
随温度的变化。若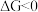 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
时,下列反应不能自发进行的是_______。
(2) 与C、
与C、 ,在
,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
①该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为_______ ;
②随着温度升高,尾气中 的含量升高,原因是
的含量升高,原因是_______ 。
(3)“除钒”过程中的化学方程式为_______ ;“除硅、铝”过程中,分离 中含
中含 、
、 杂质的方法是
杂质的方法是_______ 。
(4)“除钒”和“除硅、铝”的顺序_______ (填“能”或“不能”)交换,理由是_______ 。
(5)下列金属冶炼方法与本工艺流程中加入 冶炼
冶炼 的方法相似的是_______。
的方法相似的是_______。
 ,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗
 中含有的几种物质的沸点:
中含有的几种物质的沸点:| 物质 |  |  |  |  |
沸点/ | 136 | 127 | 57 | 180 |
(1)已知
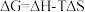 ,
, 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略 、
、 随温度的变化。若
随温度的变化。若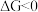 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
时,下列反应不能自发进行的是_______。
A. | B. |
C. | D. |
 与C、
与C、 ,在
,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:| 物质 |  |  |  |  |
分压 | 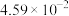 | 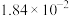 |  |  |
 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为②随着温度升高,尾气中
 的含量升高,原因是
的含量升高,原因是(3)“除钒”过程中的化学方程式为
 中含
中含 、
、 杂质的方法是
杂质的方法是(4)“除钒”和“除硅、铝”的顺序
(5)下列金属冶炼方法与本工艺流程中加入
 冶炼
冶炼 的方法相似的是_______。
的方法相似的是_______。| A.高炉炼铁 | B.电解熔融氯化钠制钠 | C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
2022-06-10更新
|
11482次组卷
|
19卷引用:云南省开远市第一中学校2022-2023学年高二下学期5月月考化学试题
云南省开远市第一中学校2022-2023学年高二下学期5月月考化学试题福建省厦门第一中学2023-2024学年高二上学期期中考试化学试题河南省周口恒大中学2023-2024学年高二上学期12月月考化学试题2022年新高考湖南化学高考真题(已下线)2022年湖南卷高考真题变式题(15-19)(已下线)专题14 化学反应原理综合题-2022年高考真题模拟题分项汇编(已下线)专题16 工艺流程题-三年(2020-2022)高考真题分项汇编(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)2022年湖北省高考真题变式题16-19(已下线)2022年海南省高考真题变式题15-19(已下线)易错点08 金属材料-备战2023年高考化学考试易错题(已下线)专题29 无机化工流程综合分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 大题突破3 无机化工流程题题型研究(已下线)题型38 基于金属元素的工艺流程题(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
解题方法
3 . 在密闭容器中投入一定量的CaCO3发生分解反应: CaCO3(s)  CaO(s)+CO2(g) ΔH>0,某温度下,达到平衡时,测得体系中气体的压强为P。当其他条件不变,仅改变影响平衡的一个条件,下列说法正确的是
CaO(s)+CO2(g) ΔH>0,某温度下,达到平衡时,测得体系中气体的压强为P。当其他条件不变,仅改变影响平衡的一个条件,下列说法正确的是
 CaO(s)+CO2(g) ΔH>0,某温度下,达到平衡时,测得体系中气体的压强为P。当其他条件不变,仅改变影响平衡的一个条件,下列说法正确的是
CaO(s)+CO2(g) ΔH>0,某温度下,达到平衡时,测得体系中气体的压强为P。当其他条件不变,仅改变影响平衡的一个条件,下列说法正确的是| A.当CaO的质量不再变化时,表明该反应重新达到了化学平衡状态 |
| B.升高温度,正反应速率增大,逆反应速率减小 |
| C.扩大容器体积,重新达到平衡时CO2的压强一定小于P |
| D.常温常压下CaCO3的分解反应一定自发 |
您最近一年使用:0次
2022-05-26更新
|
1065次组卷
|
4卷引用:上海市行知中学2022-2023学年高二上学期期中考试化学(加试)试题
上海市行知中学2022-2023学年高二上学期期中考试化学(加试)试题辽宁省鞍山市第一中学2022届高三下学期六模化学试题河北省邯郸市大名县第一中学2022-2023学年高三上学期第一次月考化学试题(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题6-10)
2022·河北·模拟预测
名校
解题方法
4 . 一定条件下HCOOH在Pd催化剂表面脱氢的反应机理、反应历程与能量的关系如图所示:
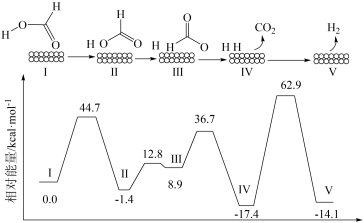
下列说法错误的是

下列说法错误的是
| A.HCOOH催化脱氢反应在该温度下能自发进行 |
| B.在历程Ⅰ~Ⅴ中,由Ⅳ到Ⅴ的反应为决速步骤 |
| C.由反应历程可得出HCOOH中第1个H原子更易脱去 |
| D.在该反应历程中,HCOOH所有的化学键均发生断裂 |
您最近一年使用:0次
5 . 氮氧化物的有效去除和资源的充分利用是当今社会的重要研究课题。
(1)已知:4NH3(g)+5O2(g)=4NO(g) +6H2O(g) ΔH1 = -907.0 kJ•mol-1
4NH3(g) +3O2(g)=2N2(g)+6H2O(g) ΔH2= -1269.0 kJ•mol-1
若4NH3(g) +6NO(g) 5N2(g) +6H2O(g)的逆反应活化能为 E逆 kJ•mol-1,则其正反应活化能为
5N2(g) +6H2O(g)的逆反应活化能为 E逆 kJ•mol-1,则其正反应活化能为_______ kJ•mol-1 (用含E逆的代数式表示)。
(2)已知:①2NO(g)+2ICl(g) 2NOCl (g)+I2(g)
2NOCl (g)+I2(g)
②2NOCl(g) 2NO(g)+Cl2(g)
2NO(g)+Cl2(g)
③I2(g)+Cl2(g) 2ICl(g)
2ICl(g)
若向VL恒容密闭容器中加 2mol NO和 2mol ICl发生上述反应,达到平衡时,容器中 NOCl (g)为amol,Cl2(g)为b mol,此时 I2(g)的浓度为_______ mol•L-1(用含 a、b、V 的代数式表示,下同),反应③的平衡常数为_______ 。
(3)某化工厂排出的尾气(含 CO、N2O)治理的方法为在密闭容器中发生如下反应:CO(g)+N2O(g) CO2(g)+N2(g),CO、N2O在Pt2O+表面进行反应转化为无毒气体,其相对能量与反应历程的关系如下图所示:
CO2(g)+N2(g),CO、N2O在Pt2O+表面进行反应转化为无毒气体,其相对能量与反应历程的关系如下图所示:_______ 。
(4)已知4CO(g) +2NO2(g) 4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在_______ (填“高温”、“低温”或“任何温度”)下能自发进行,为探究温度及不同催化剂对该反应的影响,保持其它初始条件不变重复实验,在相同时间内测得 N2产率与温度的关系如图所示。在催化剂乙作用下,图中 M 点对应的速率(对应温度400℃)v正_______ (填“>”、“<” 或“=”) v逆,温度高于400℃,N2产率降低的原因可能是_______ 。
(1)已知:4NH3(g)+5O2(g)=4NO(g) +6H2O(g) ΔH1 = -907.0 kJ•mol-1
4NH3(g) +3O2(g)=2N2(g)+6H2O(g) ΔH2= -1269.0 kJ•mol-1
若4NH3(g) +6NO(g)
 5N2(g) +6H2O(g)的逆反应活化能为 E逆 kJ•mol-1,则其正反应活化能为
5N2(g) +6H2O(g)的逆反应活化能为 E逆 kJ•mol-1,则其正反应活化能为(2)已知:①2NO(g)+2ICl(g)
 2NOCl (g)+I2(g)
2NOCl (g)+I2(g) ②2NOCl(g)
 2NO(g)+Cl2(g)
2NO(g)+Cl2(g)③I2(g)+Cl2(g)
 2ICl(g)
2ICl(g)若向VL恒容密闭容器中加 2mol NO和 2mol ICl发生上述反应,达到平衡时,容器中 NOCl (g)为amol,Cl2(g)为b mol,此时 I2(g)的浓度为
(3)某化工厂排出的尾气(含 CO、N2O)治理的方法为在密闭容器中发生如下反应:CO(g)+N2O(g)
 CO2(g)+N2(g),CO、N2O在Pt2O+表面进行反应转化为无毒气体,其相对能量与反应历程的关系如下图所示:
CO2(g)+N2(g),CO、N2O在Pt2O+表面进行反应转化为无毒气体,其相对能量与反应历程的关系如下图所示:
(4)已知4CO(g) +2NO2(g)
 4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
您最近一年使用:0次
2022-05-12更新
|
857次组卷
|
5卷引用:湖南省祁东县育贤中学2022-2023学年高二上学期第一次月考化学试题
湖南省祁东县育贤中学2022-2023学年高二上学期第一次月考化学试题(已下线)专题06 化学反应的方向及调控【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)天津市和平区2022届高三第二次质量调查化学试题湖南省邵东市第三中学2021-2022学年高三下学期5月月考化学试题2024届广西桂林市高三下学期4月月考化学试卷
名校
6 . 图表示生成几种氯化物反应的自由能变化 随温度变化情况。若在图示温度范围内焓变
随温度变化情况。若在图示温度范围内焓变 和熵变
和熵变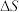 不变,且
不变,且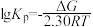 ,其中R为常数,T为温度。下列说法错误的是
,其中R为常数,T为温度。下列说法错误的是
 随温度变化情况。若在图示温度范围内焓变
随温度变化情况。若在图示温度范围内焓变 和熵变
和熵变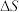 不变,且
不变,且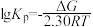 ,其中R为常数,T为温度。下列说法错误的是
,其中R为常数,T为温度。下列说法错误的是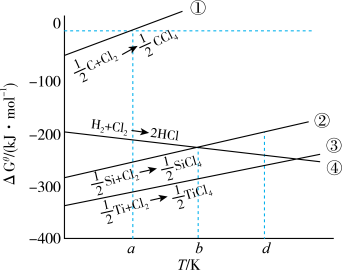
A.反应①在温度a时的平衡常数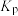 为1 为1 | B.反应②的平衡常数随温度升高而减小 |
| C.图示温度范围内,③是自发进行的 | D.任何温度下均可用 还原 还原 制备 制备 |
您最近一年使用:0次
2022-05-02更新
|
1283次组卷
|
7卷引用:山东省青岛第二中学2022-2023学年高二上学期期中考试化学试题
山东省青岛第二中学2022-2023学年高二上学期期中考试化学试题湖南省岳阳市第一中学2022-2023高二上学期期末考试化学试题(已下线)【2022】【高二上】【期中考】【高中化学】60(已下线)【2022】【高二化学】【期中考】-179河北省2022届高三下学期4月全过程纵向评价化学试题山东省东营市胜利第一中学2022届高三仿真演练押题化学试题(已下线)第22讲 化学平衡常数及转化率的计算(讲)-2023年高考化学一轮复习讲练测(全国通用)
名校
解题方法
7 . “氯碱工业”以电解饱和食盐水为基础制取氯气等产品,氯气是实验室和工业上的常用气体。
(1)离子交换膜法电解饱和食盐水示意图如下,回答下列问题:
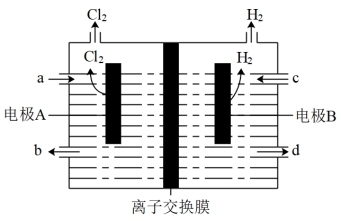
①电解饱和食盐水制取氯气的化学方程式是_______ 。
②下列说法不正确 的是_______ 。
A.电极A为阳极,发生氧化反应生成氯气
B.离子交换膜为阳离子交换膜
C.饱和NaCl溶液从a处进,NaOH溶液从d处出
D.OH—迁移的数量等于导线上通过电子的数量
③电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用_______ 。
(2)25℃时,氯气溶于水的过程及其平衡常数为:
Cl2(g) Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2
Cl2(aq)+H2O HClO+H++Cl— K2=10-3.4
HClO+H++Cl— K2=10-3.4
HClO H++ClO— K3
H++ClO— K3
其中Cl2(aq)、HClO和ClO-分别在三者中占分数(α)随pH变化的关系如下图所示:
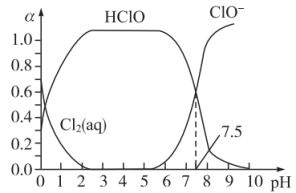
①Cl2(g) Cl2(aq)的焓变△H1
Cl2(aq)的焓变△H1_______ 0(填“>”、“=”或“<”)。
②已知25℃时:Cl2(g)+H2O 2H++ClO—+Cl—K4,则K4=
2H++ClO—+Cl—K4,则K4=_______ 。
(1)离子交换膜法电解饱和食盐水示意图如下,回答下列问题:

①电解饱和食盐水制取氯气的化学方程式是
②下列说法
A.电极A为阳极,发生氧化反应生成氯气
B.离子交换膜为阳离子交换膜
C.饱和NaCl溶液从a处进,NaOH溶液从d处出
D.OH—迁移的数量等于导线上通过电子的数量
③电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用
(2)25℃时,氯气溶于水的过程及其平衡常数为:
Cl2(g)
 Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2Cl2(aq)+H2O
 HClO+H++Cl— K2=10-3.4
HClO+H++Cl— K2=10-3.4HClO
 H++ClO— K3
H++ClO— K3其中Cl2(aq)、HClO和ClO-分别在三者中占分数(α)随pH变化的关系如下图所示:

①Cl2(g)
 Cl2(aq)的焓变△H1
Cl2(aq)的焓变△H1②已知25℃时:Cl2(g)+H2O
 2H++ClO—+Cl—K4,则K4=
2H++ClO—+Cl—K4,则K4=
您最近一年使用:0次
名校
解题方法
8 . 一定条件下HCOOH在Pd催化剂表面脱氢的反应机理、反应历程与能量的关系如图所示:
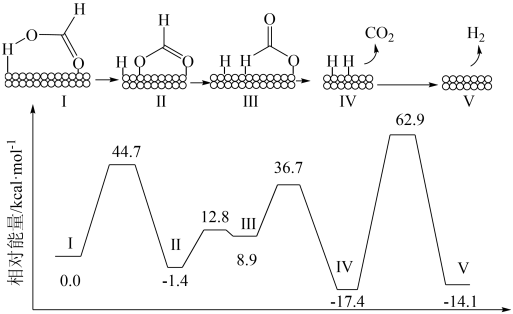
下列说法错误的是

下列说法错误的是
| A.HCOOH催化脱氢反应在该温度下能自发进行 |
| B.在历程Ⅰ~Ⅴ中,由Ⅳ到Ⅴ的反应为决速步骤 |
| C.由反应历程可得出HCOOH中第2个H原子更易脱去 |
| D.在该反应历程中,HCOOH所有的化学键均发生断裂 |
您最近一年使用:0次
2022-04-16更新
|
1057次组卷
|
6卷引用:山东省青岛莱西市2022-2023学年高二上学期期中考试化学试题
山东省青岛莱西市2022-2023学年高二上学期期中考试化学试题山东省枣庄市2022届高三第二次模拟化学试题山东省枣庄市2022届高三下学期4月模拟考试化学试题(已下线)专项10 化学反应与能量-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)山东省潍坊市2022届高三下学期5月模拟考试(二)化学试题湖南省长沙市望城区第一中学2022届高三下学期期中考试化学试题
名校
解题方法
9 . Ⅰ.从氯二氟甲烷(CHClF2)中获得四氟乙烯(C2F4):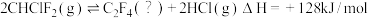 。
。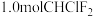 样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有
样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有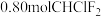 。
。
(1)写出四氟乙烯形成的高分子化合物聚四氟乙烯的结构简式_______ 。
(2)如图是一定条件下,反应物平衡时物质的量分数与压强的关系曲线。据此判断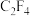 的状态是
的状态是 _______ (填“气体”、“液体”或“固体”)。
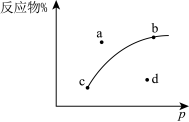
(3)该反应在_______ (填“高温”、“低温”或“任意温度”)的自发性更大;
(4)如图的a~d四点中,表示Q>K的点有_______ ;
(5)以平衡时气态物质的量分数表示平衡常数 ,其计算表达式为
,其计算表达式为 _______ 。
Ⅱ. 研究 氧化
氧化 制
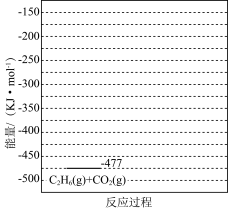
制 对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):
对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):
Ⅰ.C2H6(g) C2H4(g)+H2(g) △H1=136kJ·mol-1
C2H4(g)+H2(g) △H1=136kJ·mol-1
Ⅱ.C2H6(g)+CO2(g) C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1
C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1
Ⅲ.C2H6(g)+2CO2(g) 4CO(g)+3H2(g) △H3
4CO(g)+3H2(g) △H3
Ⅳ.CO2(g)+H2(g) CO(g)+H2O(g) △H4=41kJ·mol-1
CO(g)+H2O(g) △H4=41kJ·mol-1

(6)有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下:[C2H6(g)+CO2(g)]→[C2H4(g)+H2(g)+CO2(g)]→[C2H4(g)+CO(g)+H2O(g)],且第二步速率较慢(反应活化能为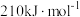 )。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量
)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量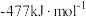 开始(如图)。
开始(如图)。_______
(7)① 和
和 按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“
按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“ 氧化
氧化 制
制 ”的影响,所得实验数据如下表:
”的影响,所得实验数据如下表:
结合具体反应分析,在催化剂X作用下, 氧化
氧化 的主要产物是
的主要产物是_______ ,判断依据是_______ 。
②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高 的选择性(生成
的选择性(生成 的物质的量与消耗
的物质的量与消耗 的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是
的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是_______ 。
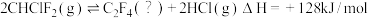 。
。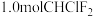 样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有
样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有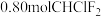 。
。(1)写出四氟乙烯形成的高分子化合物聚四氟乙烯的结构简式
(2)如图是一定条件下,反应物平衡时物质的量分数与压强的关系曲线。据此判断
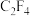 的状态是
的状态是 
(3)该反应在
(4)如图的a~d四点中,表示Q>K的点有
(5)以平衡时气态物质的量分数表示平衡常数
 ,其计算表达式为
,其计算表达式为 Ⅱ. 研究
 氧化
氧化 制
制 对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):
对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):Ⅰ.C2H6(g)
 C2H4(g)+H2(g) △H1=136kJ·mol-1
C2H4(g)+H2(g) △H1=136kJ·mol-1Ⅱ.C2H6(g)+CO2(g)
 C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1
C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1Ⅲ.C2H6(g)+2CO2(g)
 4CO(g)+3H2(g) △H3
4CO(g)+3H2(g) △H3Ⅳ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H4=41kJ·mol-1
CO(g)+H2O(g) △H4=41kJ·mol-1
(6)有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下:[C2H6(g)+CO2(g)]→[C2H4(g)+H2(g)+CO2(g)]→[C2H4(g)+CO(g)+H2O(g)],且第二步速率较慢(反应活化能为
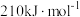 )。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量
)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量 开始(如图)。
开始(如图)。
(7)①
 和
和 按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“
按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“ 氧化
氧化 制
制 ”的影响,所得实验数据如下表:
”的影响,所得实验数据如下表:| 催化剂 | 转化率C2H6/% | 转化率CO2/% | 产率C2H4/% |
| 催化剂X | 19.0 | 37.6 | 3.3 |
 氧化
氧化 的主要产物是
的主要产物是②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高
 的选择性(生成
的选择性(生成 的物质的量与消耗
的物质的量与消耗 的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是
的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是
您最近一年使用:0次
名校
10 . 利用CO2催化加氢可制乙烯,反应为2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g) △H,在两个容积均为1L恒容密闭容器中,分别加入2molCO2、4molH2,分别选用两种催化剂,反应进行相同时间,测得CO2转化率随反应温度的变化如下图所示。下列说法正确的是
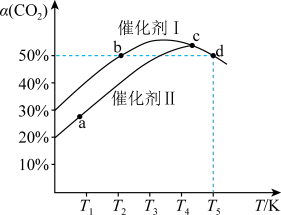

| A.使用催化剂I时反应的活化能低于催化剂II |
| B.△H>0 |
| C.b、d两状态下,化学反应速率相等 |
| D.d状态下,保持其他条件不变,向容器中再加入1molCO2与0.5molC2H4,v(正)<v(逆) |
您最近一年使用:0次
2022-03-30更新
|
1508次组卷
|
12卷引用:江西省宜春市宜丰中学2023-2024学年高二上学期9月月考化学试题
江西省宜春市宜丰中学2023-2024学年高二上学期9月月考化学试题河北省保定市六校联考2023-2024学年高二上学期11月期中考试化学试题江苏省徐州市新沂市第一中学2021-2022学年高三下学期3月月考化学试题(已下线)卷06 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)湖北省襄阳市第五中学2022届高三下学期适应性考试(二模)化学试题(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)河南省南阳市2022-2023学年高三上学期期中质量评估化学试题学科特色4 化学反应速率、平衡图像(已下线)题型23 平衡常数、平衡转化率图象河南省南阳市2022-2023学年高三上学期11月期中考试化学试题(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型04 化学反应速率与平衡图像分析-2024年高考化学答题技巧与模板构建



