名校
解题方法
1 . 研究化学反应的方向、速率、限度具有重要意义,下列说法正确的是
| A.ΔH<0、ΔS>0的反应在温度低时不能自发进行 |
B.一定温度下反应CaCO3(s) CaO(s)+CO2(g)达平衡,增加CaCO3的量,平衡正向移动 CaO(s)+CO2(g)达平衡,增加CaCO3的量,平衡正向移动 |
| C.升高温度可增大反应物分子的活化分子百分数从而提高化学反应速率 |
| D.在其他外界条件不变的情况下,汽车排气管中使用催化剂,可以改变产生尾气的反应方向 |
您最近一年使用:0次
2024-02-26更新
|
214次组卷
|
2卷引用:辽宁省沈阳市重点高中联合体2023-2024学年高二上学期期末考试化学试题
名校
2 . 硫酰氯(SO2Cl2)在有机合成中有广泛应用。实验室制备原理是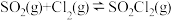
 。在密闭反应器中充入1molSO2和2.6molCl2合成SO2Cl2,测得体系内SO2平衡转化率与温度、压强关系如图所示。下列叙述正确的是
。在密闭反应器中充入1molSO2和2.6molCl2合成SO2Cl2,测得体系内SO2平衡转化率与温度、压强关系如图所示。下列叙述正确的是
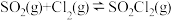
 。在密闭反应器中充入1molSO2和2.6molCl2合成SO2Cl2,测得体系内SO2平衡转化率与温度、压强关系如图所示。下列叙述正确的是
。在密闭反应器中充入1molSO2和2.6molCl2合成SO2Cl2,测得体系内SO2平衡转化率与温度、压强关系如图所示。下列叙述正确的是
| A.该可逆反应的正反应在较高温度下能自发进行 |
B.M点 分压为6.0kPa 分压为6.0kPa |
C.正反应速率: |
| D.在a、b、c、d和P点中,a和P点的平衡常数相等 |
您最近一年使用:0次
2024-02-23更新
|
69次组卷
|
2卷引用:江西省宜春市上高二中2023-2024学年高二下学期3月月考化学试题
名校
3 . 在恒容、密闭的容器中放置一定量的NO和足量的C,发生反应: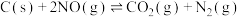 ,NO的平衡浓度与温度的关系如图所示。下列说法正确的是
,NO的平衡浓度与温度的关系如图所示。下列说法正确的是
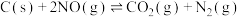 ,NO的平衡浓度与温度的关系如图所示。下列说法正确的是
,NO的平衡浓度与温度的关系如图所示。下列说法正确的是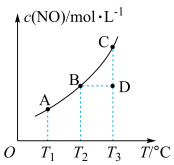
| A.增大压强或升高温度,NO的转化率均增大 |
B.在 时,若反应体系处于状态D,则 时,若反应体系处于状态D,则 |
C.状态A、B、C、D的平衡常数: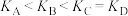 |
D.若该反应在任意温度下均能自发进行,则 |
您最近一年使用:0次
2024-02-23更新
|
111次组卷
|
3卷引用:江西省部分学校2023-2024学年高二上学期1月期末化学试题
名校
解题方法
4 . 分析下列反应,在任何温度下均能自发进行的是
A.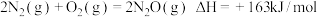 |
B.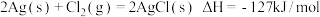 |
C.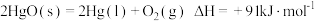 |
D.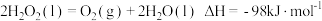 |
您最近一年使用:0次
名校
解题方法
5 . 工业燃烧煤、石油等化石燃料释放出大量氮氧化物、一氧化碳、二氧化碳等气体,严重污染空气。通过对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
(1)甲醇不仅是重要的化工原料,而且还是性能优良的能源和车用燃料。甲醇和水蒸气制取 的反应如下:
的反应如下:
反应Ⅰ: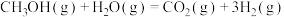
 平衡常数为
平衡常数为
反应Ⅱ:
 平衡常数为
平衡常数为
反应 的
的
______ (用含 的式子表示),平衡常数
的式子表示),平衡常数
______ (用含 的式子表示)。
的式子表示)。
(2)二氧化碳可以合成甲醇,一氧化碳也可以合成甲醇,用CO和 合成
合成 的化学方程式为
的化学方程式为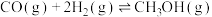
 ,向2L恒容密闭容器中加入2mol CO和4mol
,向2L恒容密闭容器中加入2mol CO和4mol  ,在适当的催化剂作用下,此反应能自发进行。
,在适当的催化剂作用下,此反应能自发进行。
①该反应
______ 0(填“>”、“<”或“=”)
②下列叙述能说明此反应达到平衡状态的是______ 。(填字母)
A.混合气体的平均相对分子质量保持不变 B.CO的转化率和 的转化率相等
的转化率相等
C.1mol CO生成的同时有2mol H-H键断裂 D.混合气体的密度保持不变
③按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,请分析:
温度:
______  ;正反应速率:
;正反应速率: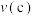
______ 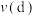 (填“>”、“<”或“=”)
(填“>”、“<”或“=”) kPa的容器中加入2mol CO和4mol
kPa的容器中加入2mol CO和4mol  ,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率
,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率
______ ,反应平衡常数表示为
______ ( 就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含
就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含 的式子表示)
的式子表示)
(1)甲醇不仅是重要的化工原料,而且还是性能优良的能源和车用燃料。甲醇和水蒸气制取
 的反应如下:
的反应如下:反应Ⅰ:
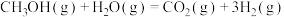
 平衡常数为
平衡常数为
反应Ⅱ:

 平衡常数为
平衡常数为
反应
 的
的
 的式子表示),平衡常数
的式子表示),平衡常数
 的式子表示)。
的式子表示)。(2)二氧化碳可以合成甲醇,一氧化碳也可以合成甲醇,用CO和
 合成
合成 的化学方程式为
的化学方程式为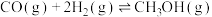
 ,向2L恒容密闭容器中加入2mol CO和4mol
,向2L恒容密闭容器中加入2mol CO和4mol  ,在适当的催化剂作用下,此反应能自发进行。
,在适当的催化剂作用下,此反应能自发进行。①该反应

②下列叙述能说明此反应达到平衡状态的是
A.混合气体的平均相对分子质量保持不变 B.CO的转化率和
 的转化率相等
的转化率相等C.1mol CO生成的同时有2mol H-H键断裂 D.混合气体的密度保持不变
③按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,请分析:
温度:

 ;正反应速率:
;正反应速率: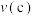
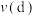 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)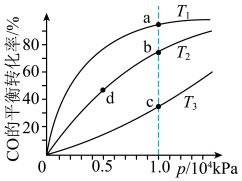
 kPa的容器中加入2mol CO和4mol
kPa的容器中加入2mol CO和4mol  ,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率
,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率

 就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含
就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含 的式子表示)
的式子表示)
您最近一年使用:0次
2024-02-21更新
|
67次组卷
|
2卷引用:浙江省宁波三锋教研联盟2023-2024学年高二上学期期中联考化学试题
名校
6 . I.肼可作氢气“储蓄罐”。Ni-Pt/La2O3是一种高选择性的肼分解制氢催化剂,催化反应机理如图所示,反应如下:

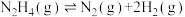
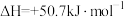
(1)根据上述信息,推测Ni-Pt/La2O3___________。
Ⅱ.肼类燃烧剂曾是火箭的“粮食”,但会造成污染,正逐渐被淘汰。新一代运载火箭采用全新配方——低温液氢液氧推进剂,让火箭飞得更稳健。已知一定条件下:
①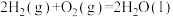
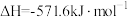 '
'
②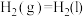

③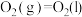
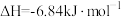
④

(2)请写出相同条件下液氢和液氧生成气态水的热化学方程式:___________ 。
(3)根据上述信息,以下说法正确的是___________。

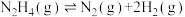
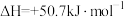
(1)根据上述信息,推测Ni-Pt/La2O3___________。
| A.能够有效降低制氢反应的反应热 |
| B.同时提高制氢正反应和逆反应的速率 |
| C.改变了制氢反应的反应历程 |
| D.不参与化学反应,使用一段时间后无需补加 |
Ⅱ.肼类燃烧剂曾是火箭的“粮食”,但会造成污染,正逐渐被淘汰。新一代运载火箭采用全新配方——低温液氢液氧推进剂,让火箭飞得更稳健。已知一定条件下:
①
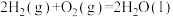
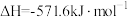 '
'②
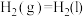

③
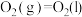
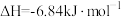
④


(2)请写出相同条件下液氢和液氧生成气态水的热化学方程式:
(3)根据上述信息,以下说法正确的是___________。
| A.变化④为低温自发的过程 |
| B.液氢液氧不点燃观察不到水生成,故该反应无法自发进行 |
| C.0.5mol液态氢气的能量高于0.5mol气态氢气的能量 |
| D.液氢和液氧作为火箭推进剂符合绿色化学理念 |
您最近一年使用:0次
解题方法
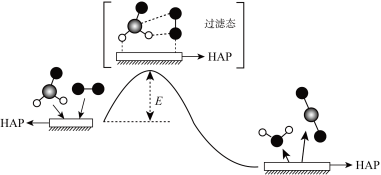
7 .  与
与 在催化剂
在催化剂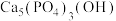 (简写为HAP)表面催化生成
(简写为HAP)表面催化生成 和
和 的历程示意图如图所示。已知该反应
的历程示意图如图所示。已知该反应 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是
 与
与 在催化剂
在催化剂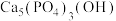 (简写为HAP)表面催化生成
(简写为HAP)表面催化生成 和
和 的历程示意图如图所示。已知该反应
的历程示意图如图所示。已知该反应 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是
| A.该反应发生时,环境温度升高 |
| B.HAP的作用是降低反应的反应热 |
C.任何条件下,HCHO和 的内能大于 的内能大于 和 和 的内能 的内能 |
| D.在高温条件自发进行 |
您最近一年使用:0次
8 .  是重要的化工原料,合成氨反应为
是重要的化工原料,合成氨反应为
 。工业上常用氨氧化法制硝酸(如图):将氨和空气混合后先经过热交换器,再通入灼热催化剂铂铑合金网生成NO,经过反应
。工业上常用氨氧化法制硝酸(如图):将氨和空气混合后先经过热交换器,再通入灼热催化剂铂铑合金网生成NO,经过反应
 ,将
,将 与水反应制得硝酸。
与水反应制得硝酸。
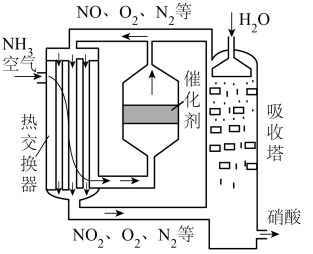
下列有关合成氨反应的说法正确的是
 是重要的化工原料,合成氨反应为
是重要的化工原料,合成氨反应为
 。工业上常用氨氧化法制硝酸(如图):将氨和空气混合后先经过热交换器,再通入灼热催化剂铂铑合金网生成NO,经过反应
。工业上常用氨氧化法制硝酸(如图):将氨和空气混合后先经过热交换器,再通入灼热催化剂铂铑合金网生成NO,经过反应
 ,将
,将 与水反应制得硝酸。
与水反应制得硝酸。
下列有关合成氨反应的说法正确的是
A.反应的 |
B.反应的 (E表示键能) (E表示键能) |
C.反应在高温和催化剂条件下进行可提高 的平衡转化率 的平衡转化率 |
D.反应中每消耗 转移电子的数目约等于 转移电子的数目约等于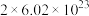 |
您最近一年使用:0次
名校
解题方法
9 . 我国的能源消费结构以燃煤为主,将煤气化可减少环境污染。
(1)将煤与水蒸气在恒容密闭容器中反应,可制合成气。制备过程中的主要反应(a)、(b)的 (
( 为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
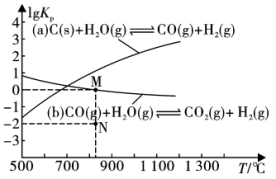
①下列能说明反应(a)
 已达到平衡状态的是
已达到平衡状态的是___________ (填字母)。
A. B.混合气体的总压强不再变化
B.混合气体的总压强不再变化
C. 不再变化 D.混合气体的密度不再变化
不再变化 D.混合气体的密度不再变化
②在容积为1L的密闭容器中充入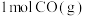 、
、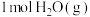 只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
___________  ;已知反应速率
;已知反应速率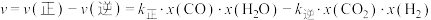 ,
, 、
、 分别为正、逆反应速率常数,x为物质的量分数,N处的
分别为正、逆反应速率常数,x为物质的量分数,N处的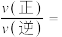
___________ 。
(2)一种新型煤气化燃烧集成制氢发生的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.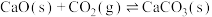

Ⅳ.
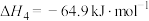
副反应:
Ⅴ.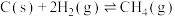
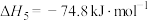
Ⅵ.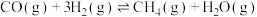
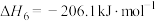
已知反应Ⅰ、Ⅱ的平衡常数 ,
, 随温度的变化如图1、图2所示。
随温度的变化如图1、图2所示。
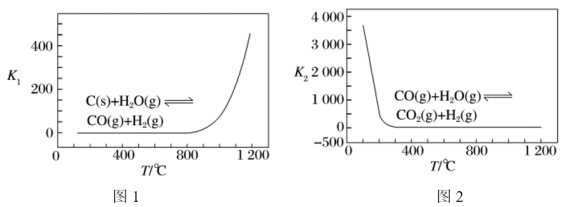
①由反应Ⅴ和反应Ⅵ可知,
___________  ;反应Ⅰ的
;反应Ⅰ的
___________ (填“>”或“<”)0。
②温度小于800℃时, ,原因是
,原因是___________ 。
③为提高反应Ⅱ中CO的转化率,可采取的措施是___________ (写一条)。
④ 时,向密闭容器中充入
时,向密闭容器中充入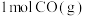 和
和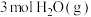 ,只发生反应Ⅱ,此时该反应的平衡常数
,只发生反应Ⅱ,此时该反应的平衡常数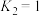 ,CO的平衡转化率为
,CO的平衡转化率为___________ 。
⑤从环境保护角度分析,该制氢工艺中设计反应Ⅲ的优点是___________ 。
(1)将煤与水蒸气在恒容密闭容器中反应,可制合成气。制备过程中的主要反应(a)、(b)的
 (
( 为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
①下列能说明反应(a)

 已达到平衡状态的是
已达到平衡状态的是A.
 B.混合气体的总压强不再变化
B.混合气体的总压强不再变化C.
 不再变化 D.混合气体的密度不再变化
不再变化 D.混合气体的密度不再变化②在容积为1L的密闭容器中充入
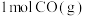 、
、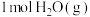 只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
 ;已知反应速率
;已知反应速率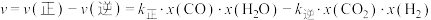 ,
, 、
、 分别为正、逆反应速率常数,x为物质的量分数,N处的
分别为正、逆反应速率常数,x为物质的量分数,N处的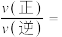
(2)一种新型煤气化燃烧集成制氢发生的主要反应如下:
Ⅰ.


Ⅱ.


Ⅲ.
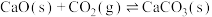

Ⅳ.

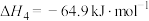
副反应:
Ⅴ.
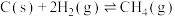
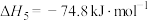
Ⅵ.
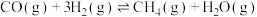
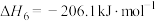
已知反应Ⅰ、Ⅱ的平衡常数
 ,
, 随温度的变化如图1、图2所示。
随温度的变化如图1、图2所示。
①由反应Ⅴ和反应Ⅵ可知,

 ;反应Ⅰ的
;反应Ⅰ的
②温度小于800℃时,
 ,原因是
,原因是③为提高反应Ⅱ中CO的转化率,可采取的措施是
④
 时,向密闭容器中充入
时,向密闭容器中充入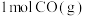 和
和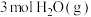 ,只发生反应Ⅱ,此时该反应的平衡常数
,只发生反应Ⅱ,此时该反应的平衡常数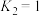 ,CO的平衡转化率为
,CO的平衡转化率为⑤从环境保护角度分析,该制氢工艺中设计反应Ⅲ的优点是
您最近一年使用:0次
10 . 汽车尾气在稀土催化剂作用下通过反应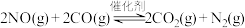 能实现转化。下列说法正确的是
能实现转化。下列说法正确的是
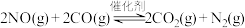 能实现转化。下列说法正确的是
能实现转化。下列说法正确的是A.该反应 |
B.该反应的平衡常数可表示为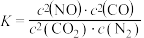 |
C.其它条件相同, 越大,CO的平衡转化率越大 越大,CO的平衡转化率越大 |
| D.若反应在恒温体积固定的条件下进行,平衡后充入氦气,压强增大,平衡正向移动 |
您最近一年使用:0次



