名校
解题方法
1 . 某温度下,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,正确的是
晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,正确的是
 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,正确的是
晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,正确的是| A.该温度低于25℃ |
B.该温度下加入等体积 的NaOH溶液可使该溶液恰好呈中性 的NaOH溶液可使该溶液恰好呈中性 |
C.加入 晶体促进了水的电离 晶体促进了水的电离 |
D.由水电离出来的 的浓度是 的浓度是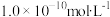 |
您最近一年使用:0次
2023-12-29更新
|
153次组卷
|
2卷引用:福建省泉州市泉港区第一中学2023-2024学年高二上学期12月月考化学试题
名校
2 . 25℃时,用 盐酸滴定
盐酸滴定 氨水的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是
氨水的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是

 盐酸滴定
盐酸滴定 氨水的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是
氨水的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是
A.a点溶液中水电离出的 小于 小于 |
| B.温度升高,c点溶液的pH减小 |
C.滴定过程,溶液中 不变 不变 |
D.25℃时,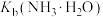 的数量级为 的数量级为 |
您最近一年使用:0次
2023-07-16更新
|
676次组卷
|
3卷引用:福建省宁德市区域性学业质量检测2022-2023学年高二上学期2月期末考试化学试题
名校
3 . 常温下,将0.1 mol∙L−1NaOH溶液滴加到20mL0.1 mol∙L−1二元弱酸H2A溶液中,混合溶液的pH随NaOH溶液滴入量的关系如图所示。下列叙述不正确的是
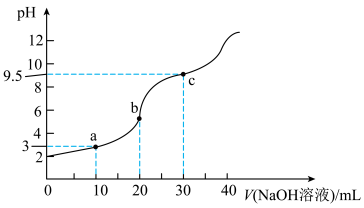

| A.Ka1(H2A)≈10−3 |
| B.b处溶质为NaHA,所以促进水的电离 |
| C.b点时溶液中存在c(Na+)>c(HA﹣)>c(H+)>c(A2﹣)>c(H2A) |
| D.c点时溶液中存在c(Na+)﹣c(HA﹣)−2c(A2﹣)=10−4.5−10﹣9.5 |
您最近一年使用:0次
2023-05-11更新
|
455次组卷
|
4卷引用:福建省福州第三中学2022-2023学年高二下学期期末考试化学试题
名校
4 . 已知草酸( )为二元弱酸,在室温下,向一定浓度的草酸溶液中逐滴加入一定浓度的
)为二元弱酸,在室温下,向一定浓度的草酸溶液中逐滴加入一定浓度的 溶液,溶液中
溶液,溶液中 、
、 、
、 三种微粒分别在三者中所占的物质的量分数
三种微粒分别在三者中所占的物质的量分数 与溶液
与溶液 的关系如图所示。下列说法中正确的是
的关系如图所示。下列说法中正确的是

 )为二元弱酸,在室温下,向一定浓度的草酸溶液中逐滴加入一定浓度的
)为二元弱酸,在室温下,向一定浓度的草酸溶液中逐滴加入一定浓度的 溶液,溶液中
溶液,溶液中 、
、 、
、 三种微粒分别在三者中所占的物质的量分数
三种微粒分别在三者中所占的物质的量分数 与溶液
与溶液 的关系如图所示。下列说法中正确的是
的关系如图所示。下列说法中正确的是
A.室温时, 的水解平衡常数 的水解平衡常数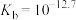 |
B.当溶液 时, 时,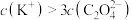 |
C.当溶液 时, 时,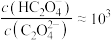 |
| D.A点溶液加水稀释,则水的电离程度减小 |
您最近一年使用:0次
2023-05-11更新
|
404次组卷
|
4卷引用:福建省泉州第五中学2023届高三一模化学试题
名校
5 . 常温下,pH均为2、体积均为V0的HA、 HB、HC三种酸溶液,分别加水稀释至体积为V,溶液pH随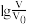 的变化关系如图所示,下列叙述错误的是
的变化关系如图所示,下列叙述错误的是
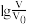 的变化关系如图所示,下列叙述错误的是
的变化关系如图所示,下列叙述错误的是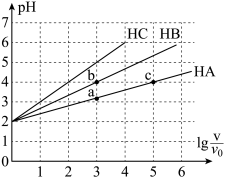
| A.常温下:Ka(HB)> Ka(HA) |
| B.水的电离程度:b点<c点 |
| C.酸的物质的量浓度:b点<a点 |
D.当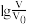 =4时,三种溶液同时升高温度, =4时,三种溶液同时升高温度, 减小 减小 |
您最近一年使用:0次
2022-09-06更新
|
1360次组卷
|
6卷引用:福建省莆田五中2023-2024学年高二上学期第三次月考化学试卷
名校
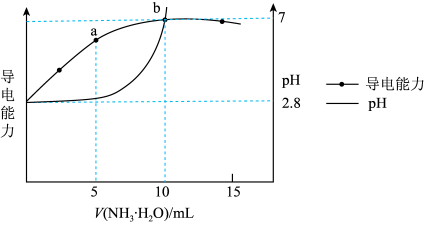
6 . 常温时,向 溶液中逐滴加入
溶液中逐滴加入 的氨水,导电能力、pH与
的氨水,导电能力、pH与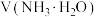 的关系变化如图所示(假设反应过程中温度不变)。下列分析错误的是
的关系变化如图所示(假设反应过程中温度不变)。下列分析错误的是
 溶液中逐滴加入
溶液中逐滴加入 的氨水,导电能力、pH与
的氨水,导电能力、pH与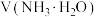 的关系变化如图所示(假设反应过程中温度不变)。下列分析错误的是
的关系变化如图所示(假设反应过程中温度不变)。下列分析错误的是
A.水的电离程度: |
B.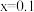 ,该温度下的 ,该温度下的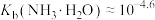 |
C.该温度下反应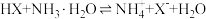 的平衡常数的数量级为 的平衡常数的数量级为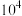 |
D.a点对应的溶液中存在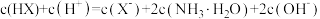 |
您最近一年使用:0次
2022-04-22更新
|
2072次组卷
|
9卷引用:福建省厦门双十中学2022届高三热身考化学试题
福建省厦门双十中学2022届高三热身考化学试题福建省永春第一中学2023届高三下学期适应性考试(五)化学试题云南省2022届高三第二次高中毕业生复习统一检测理科综合能力测试化学试题(已下线)专题10水溶液中的离子平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-2022年高考真题+模拟题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)(已下线)2022年全国乙卷高考变式题(选择题)湖南省株洲市天元区名校2022-2023学年高二上学期12月月考化学试题(已下线)学科特色3 电解质溶液图像
名校
7 . 如图为某实验测得0.10mol·L-1NaHCO3溶液在升温过程中(不考虑水挥发)的pH变化曲线。下列说法正确的是
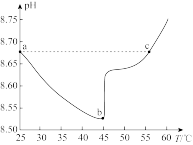

A.ab段,pH减小说明升温促进了HCO 的电离,同时抑制了HCO 的电离,同时抑制了HCO 的水解 的水解 |
| B.b点溶液恰好显中性 |
| C.a点溶液的c(OH-)比c点溶液的小 |
| D.a点时,Kw<Ka1(H2CO3)·Ka2(H2CO3) |
您最近一年使用:0次
2022-04-04更新
|
287次组卷
|
2卷引用:福建省福州第一中学2021-2022学年高二上学期期末考试化学试题
解题方法
8 . 已知水的电离平衡曲线如图所示,下列说法中正确的是
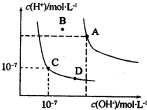

| A.水的离子积常数关系为:KW(B)>KW(A)>KW(C)>KW(D) |
| B.恒温下向水中加入氢氧化钠固体,可从C点到D点 |
| C.B点对应的温度下,pH=4的硫酸与pH=10的氢氧化钠溶液等体积混合后所得溶液的pH=7 |
| D.温度升高可实现由C点到D点 |
您最近一年使用:0次
9 . 室温下,向20.00mL 0.10mol·L﹣1 HX溶液中逐滴滴加0.10mol·L﹣1 NaOH溶液,溶液pH随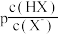 变化关系如图所示,已知
变化关系如图所示,已知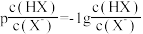 。下列说法错误的是
。下列说法错误的是
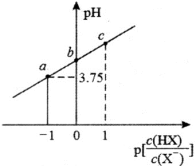
A.HX的电离常数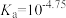 |
B.当 时,加入NaOH溶液的体积小于10.00mL 时,加入NaOH溶液的体积小于10.00mL |
C.当加入10.00mL NaOH溶液时: |
| D.如图所示各点对应溶液中水的电离程度:a>c |
您最近一年使用:0次
名校
解题方法
10 . 25℃时,向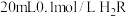 (二元弱酸)溶液中滴加
(二元弱酸)溶液中滴加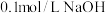 溶液,溶液pH与加入
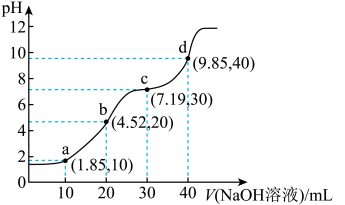
溶液,溶液pH与加入 溶液体积的关系如图所示(忽略溶液体积变化)。下列说法正确的是
溶液体积的关系如图所示(忽略溶液体积变化)。下列说法正确的是
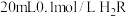 (二元弱酸)溶液中滴加
(二元弱酸)溶液中滴加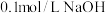 溶液,溶液pH与加入
溶液,溶液pH与加入 溶液体积的关系如图所示(忽略溶液体积变化)。下列说法正确的是
溶液体积的关系如图所示(忽略溶液体积变化)。下列说法正确的是
A.a点对应的溶液中: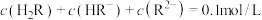 |
| B.b点对应的溶液中:c(Na+)>c(HR-)>c(H2R)>c(R2-) |
| C.溶液的导电性:b>c |
| D.a、b、c、d点中,d点对应的溶液中水的电离程度最大 |
您最近一年使用:0次
2020-09-19更新
|
2042次组卷
|
9卷引用:福建省莆田华侨中学2021-2022学年高二上学期期末考试化学试题



