1 . 为了探究温度对水解平衡的影响,用手持技术测定一定浓度 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是
 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是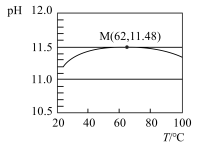
| A.该实验能证明升温促进水解 | B.点M之后 水解放热 水解放热 |
C.点M处溶液中 略大于 略大于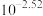 mol/L mol/L | D.点M后pH下降是因为升温对 的影响更大 的影响更大 |
您最近一年使用:0次
名校
解题方法
2 . 雪碧、可乐是深受人们青睐的碳酸型饮料.
Ⅰ.雪琩是一款柠檬味汽水饮料,其中所含酸性物质包括碳酸、柠檬酸、苯甲酸. 时,上述三种酸的电离常数如表所示:
时,上述三种酸的电离常数如表所示:
(1)上述三种酸的酸性由强到弱的顺序为____________ (填字母并用“>”符号连接)。
a.苯甲酸 b.碳酸 c.柠檬酸
(2)水中存在平衡 ,欲使平衡向右移动且溶液显碱性,下列方法可行的是
,欲使平衡向右移动且溶液显碱性,下列方法可行的是____________ (填字母)。
a.通入氨气 b.加入 c.加热至
c.加热至 d.加入
d.加入 固体
固体
(3)室温下,向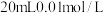 苯甲酸
苯甲酸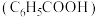 溶液中滴加等物质的量浓度的
溶液中滴加等物质的量浓度的 溶液,溶液的
溶液,溶液的 与加入
与加入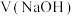 之间的关系如图所示,已知
之间的关系如图所示,已知 。
。

① 点溶液的
点溶液的
____________ (保留小数点后一位)。
②下列说法正确的有____________ 。
a.为准确判断滴定终点,可使用甲基橙做指示剂
b. 点溶液
点溶液 ,且有
,且有
c. 点溶液中一定存在
点溶液中一定存在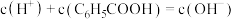
d.D点溶液中有
e.从 点到
点到 点,溶液中水的电离程度最小的是
点,溶液中水的电离程度最小的是 点
点
Ⅱ.可乐中的食品添加剂有白砂糖、二氧化碳、焦糖、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为 )有一定关系,已知磷酸电离常数为:
)有一定关系,已知磷酸电离常数为: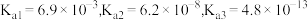
(4)室温下,测得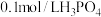 溶液的
溶液的 ,原因是
,原因是____________ (用电离方程式表示)。
(5)向含磷酸的溶液中滴加 溶液,此过程中各含磷微粒在溶液中的物质的量分数与
溶液,此过程中各含磷微粒在溶液中的物质的量分数与 的关系如图所示:
的关系如图所示:
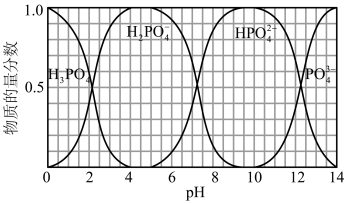
①溶液 由11增大到14的过程中,发生反应的离子方程式为
由11增大到14的过程中,发生反应的离子方程式为____________ 。
②若已知碳酸的电离常数,将磷酸滴入碳酸钠溶液中,发生反应的离子方程式错误的为____________ 。
A.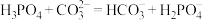 B.
B.
C.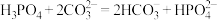 D.
D.
Ⅰ.雪琩是一款柠檬味汽水饮料,其中所含酸性物质包括碳酸、柠檬酸、苯甲酸.
 时,上述三种酸的电离常数如表所示:
时,上述三种酸的电离常数如表所示:| 物质 | 苯甲酸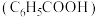 | 碳酸 | 柠檬酸 |
| 电离常数 |  |  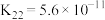 | 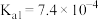 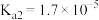  |
(1)上述三种酸的酸性由强到弱的顺序为
a.苯甲酸 b.碳酸 c.柠檬酸
(2)水中存在平衡
 ,欲使平衡向右移动且溶液显碱性,下列方法可行的是
,欲使平衡向右移动且溶液显碱性,下列方法可行的是a.通入氨气 b.加入
 c.加热至
c.加热至 d.加入
d.加入 固体
固体(3)室温下,向
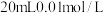 苯甲酸
苯甲酸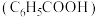 溶液中滴加等物质的量浓度的
溶液中滴加等物质的量浓度的 溶液,溶液的
溶液,溶液的 与加入
与加入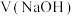 之间的关系如图所示,已知
之间的关系如图所示,已知 。
。
①
 点溶液的
点溶液的
②下列说法正确的有
a.为准确判断滴定终点,可使用甲基橙做指示剂
b.
 点溶液
点溶液 ,且有
,且有
c.
 点溶液中一定存在
点溶液中一定存在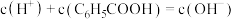
d.D点溶液中有

e.从
 点到
点到 点,溶液中水的电离程度最小的是
点,溶液中水的电离程度最小的是 点
点Ⅱ.可乐中的食品添加剂有白砂糖、二氧化碳、焦糖、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为
 )有一定关系,已知磷酸电离常数为:
)有一定关系,已知磷酸电离常数为: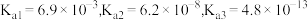
(4)室温下,测得
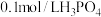 溶液的
溶液的 ,原因是
,原因是(5)向含磷酸的溶液中滴加
 溶液,此过程中各含磷微粒在溶液中的物质的量分数与
溶液,此过程中各含磷微粒在溶液中的物质的量分数与 的关系如图所示:
的关系如图所示:
①溶液
 由11增大到14的过程中,发生反应的离子方程式为
由11增大到14的过程中,发生反应的离子方程式为②若已知碳酸的电离常数,将磷酸滴入碳酸钠溶液中,发生反应的离子方程式错误的为
A.
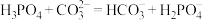 B.
B.
C.
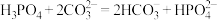 D.
D.
您最近一年使用:0次
解题方法
3 . 常温下,实验室用 的NaOH溶液滴定
的NaOH溶液滴定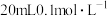 的HA溶液。溶液中,含A微粒a、b的分布系数δ、NaOH溶液的体积V与pH的关系如图所示。已知:HA的分布系数
的HA溶液。溶液中,含A微粒a、b的分布系数δ、NaOH溶液的体积V与pH的关系如图所示。已知:HA的分布系数 。下列叙述错误的是
。下列叙述错误的是

 的NaOH溶液滴定
的NaOH溶液滴定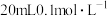 的HA溶液。溶液中,含A微粒a、b的分布系数δ、NaOH溶液的体积V与pH的关系如图所示。已知:HA的分布系数
的HA溶液。溶液中,含A微粒a、b的分布系数δ、NaOH溶液的体积V与pH的关系如图所示。已知:HA的分布系数 。下列叙述错误的是
。下列叙述错误的是
| A.x点对应溶液的pH约为5 |
B.p点对应的溶液中存在: |
| C.p→q对应的溶液中,水的电离程度一直增大 |
D.n点对应的溶液中存在: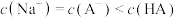 |
您最近一年使用:0次
2023-12-29更新
|
504次组卷
|
3卷引用:四川省雅安市2023-2024学年高三上学期12月联考理综试题
4 . 常温时,浓度均为0.1mol·L-1的两种一元酸次磷酸 H3PO2溶液(曲线a)和氟硼酸 溶液(曲线b),pH随加水稀释体积变化曲线如图所示。V0为起始体积,稀释后溶液的体积均为 V。下列说法符合曲线表达的是
溶液(曲线b),pH随加水稀释体积变化曲线如图所示。V0为起始体积,稀释后溶液的体积均为 V。下列说法符合曲线表达的是

 溶液(曲线b),pH随加水稀释体积变化曲线如图所示。V0为起始体积,稀释后溶液的体积均为 V。下列说法符合曲线表达的是
溶液(曲线b),pH随加水稀释体积变化曲线如图所示。V0为起始体积,稀释后溶液的体积均为 V。下列说法符合曲线表达的是
A.氟硼酸的电离方程式为:HBF4⇌H++BF |
| B.用NaOH溶液中和等体积A、B两点溶液,耗用V(NaOH):B>A |
| C.B、D两点溶液,c(H+)B<100c(H+)D |
| D.图中A、B、C、D点溶液中水的电离程度由大到小的顺序是:D>C>B>A |
您最近一年使用:0次
名校
5 . 人体血液存在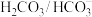 和
和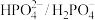 等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值
等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值 [x表示
[x表示 或
或 ]与pH的关系如图所示。已知
]与pH的关系如图所示。已知 ,
,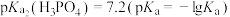 。下列说法正确的是
。下列说法正确的是

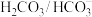 和
和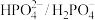 等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值
等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值 [x表示
[x表示 或
或 ]与pH的关系如图所示。已知
]与pH的关系如图所示。已知 ,
,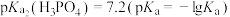 。下列说法正确的是
。下列说法正确的是
A.曲线I表示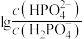 与pH的变化关系 与pH的变化关系 |
| B.a点→b点的过程中,水的电离程度逐渐减小 |
C.当pH增大时, 逐渐减小 逐渐减小 |
D.当 时, 时, |
您最近一年使用:0次
2023-10-10更新
|
851次组卷
|
5卷引用: 四川省成都市石室天府中学2023-2024学年高三上学期入学考试化学试题
名校
解题方法
6 . 常温下,某实验人员在两个相同的容器中分别加入 溶液和
溶液和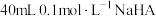 溶液,再分别用
溶液,再分别用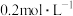 盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。(
盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。( 溶液达到某浓度后,会放出一定量气体)下列说法错误的是
溶液达到某浓度后,会放出一定量气体)下列说法错误的是

 溶液和
溶液和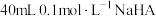 溶液,再分别用
溶液,再分别用 盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。(
盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。( 溶液达到某浓度后,会放出一定量气体)下列说法错误的是
溶液达到某浓度后,会放出一定量气体)下列说法错误的是
A.图中曲线甲和丁代表向 溶液中滴加盐酸 溶液中滴加盐酸 |
B.a点溶液中满足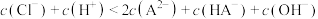 |
C.c点溶液的pH约为8,由此可知, |
| D.水的电离程度:b点>d点 |
您最近一年使用:0次
名校
7 . 室温下,用0.1mol/LNaOH溶液滴定0.02mol/LFeCl3溶液的pH-t曲线如图所示。下列说法正确的是

已知:①室温时Ksp[Fe(OH)3]=4×10-38
②lg2=0.3
③溶液中离子浓度小于或等于10-5mol/L,可认为离子沉淀完全

已知:①室温时Ksp[Fe(OH)3]=4×10-38
②lg2=0.3
③溶液中离子浓度小于或等于10-5mol/L,可认为离子沉淀完全
| A.滴定开始,a点的pH值近似为2.1 |
| B.若b点x=3.2,则溶液中Fe3+未沉淀完全 |
| C.c点存在的浓度关系:3c(Fe3+)+c(H+)=c(OH-)+c(Cl-) |
| D.从a到c点,水的电离程度一直增大 |
您最近一年使用:0次
名校
8 . 25℃时,用 盐酸滴定
盐酸滴定 氨水的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是
氨水的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是

 盐酸滴定
盐酸滴定 氨水的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是
氨水的滴定曲线如图所示(已知:滴定剂与被滴定组分的物质的量之比为滴定分数)。下列说法错误的是
A.a点溶液中水电离出的 小于 小于 |
| B.温度升高,c点溶液的pH减小 |
C.滴定过程,溶液中 不变 不变 |
D.25℃时,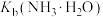 的数量级为 的数量级为 |
您最近一年使用:0次
2023-07-16更新
|
676次组卷
|
3卷引用:四川省成都外国语学校2023-2024学年高二上学期11月期中考试化学试题
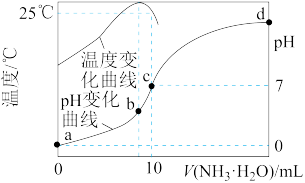
9 . 在某温度时,将nmol·L-1氨水滴入10mL1.0mol·L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是

A.a点: |
B.b点溶液中离子浓度大小关系为c(OH-)<c(H+)><c(Cl-)<c( ) ) |
| C.氨水的浓度应该大于1.0mol·L-1 |
| D.a、b、c三点水的电离程度大小关系是c>b>a |
您最近一年使用:0次
名校
10 . 下列说法正确的是
| A.常温下,pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7 |
B.常温下,水电离出的c(H+)=10-13mol/L的溶液可能与含Fe3+、NH 的溶液不共存 的溶液不共存 |
C.加入铝粉能产生H2的溶液中,可能存在大量的 Na+、Ba2+、Fe2+、AlO 、NO 、NO |
| D.pH=4的醋酸溶液,稀释至10倍后pH=5 |
您最近一年使用:0次



