21-22高二下·江苏南通·开学考试
名校
解题方法
1 . 下列图示与对应的叙述相符的是


A.图I表示2SO2(g)+O2(g)  2SO3(g) △H <0 的速率时间图象,t1时刻改变的条件是升高温度 2SO3(g) △H <0 的速率时间图象,t1时刻改变的条件是升高温度 |
| B.图II表示常温下盐酸滴定20.00 mL NaOH溶液得到的滴定曲线,由图可知盐酸的物质的量浓度为0.1 mol·L-1 |
C.图III表示反应2NO2(g)  N2O4(g) △H中NO2平衡转化率与温度、 压强的变化关系,由图可知:△H<0、P1<P2 N2O4(g) △H中NO2平衡转化率与温度、 压强的变化关系,由图可知:△H<0、P1<P2 |
| D.图IV表示pH相同的NaOH溶液与氨水稀释过程的pH变化,由图可知a对应氨水 |
您最近一年使用:0次
2022-09-14更新
|
475次组卷
|
4卷引用:云南省临沧市第一中学2022-2023学年高二上学期期中考试化学试题
云南省临沧市第一中学2022-2023学年高二上学期期中考试化学试题四川省德阳市第五中学校2022-2023学年高二上学期期中考试化学试题(已下线)江苏省如皋市2021-2022学年高二下学期期初调研化学试题河南省鹤壁市高中2022-2023学年高二上学期10月居家测试化学(平行班)试题
名校
解题方法
2 . 常温下,以酚酞作指示剂,用0.1mol/L的NaOH溶液滴定20.00mL0.1mol/L的二元酸H2A溶液。溶液中pH、分布系数δ随滴加NaOH溶液体积V(NaOH)的变化关系如图所示。[A2−的分布系数为 ],下列说法正确的是
],下列说法正确的是
 ],下列说法正确的是
],下列说法正确的是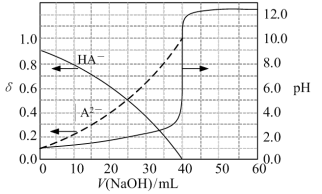
| A.当V(NaOH)=0mL时,c(HA-)+c(A2-)=0.1mol/L |
| B.当V(NaOH)=20.00mL时,c(Na+)>c(HA-)+2c(A2-) |
| C.常温下,A2-的水解常数值为1.0×10-11 |
| D.当V(NaOH)=30.00mL时,c(HA-)+c(H+)=c(A2-)+c(OH-) |
您最近一年使用:0次
2022-04-26更新
|
845次组卷
|
7卷引用:云南省昆明市禄劝彝族苗族自治县第一中学2022-2023学年高二下学期半期考试 化学试题
(已下线)云南省昆明市禄劝彝族苗族自治县第一中学2022-2023学年高二下学期半期考试 化学试题江西省安义中学2022-2023学年高三上学期中考试化学试题辽宁省阜新市阜新蒙古族自治县高级中学2022届高三下学期模拟考试化学试题(已下线)【直抵名校】03-备战2022年高考化学名校进阶模拟卷(通用版)辽宁省朝阳市建平县实验中学高三化学021-2022学年度高三第五次模拟考试化学试题(已下线)第22练 新高考模式综合练(辽宁卷)-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)第25讲 盐类水解(讲)-2023年高考化学一轮复习讲练测(全国通用)
名校
3 . 室温下,向20.00mL0.1000mol/L盐酸中逐滴滴加0.1000mol/L的NaOH溶液,pH变化如图所示。已知lg5=0.7,下列说法错误的是
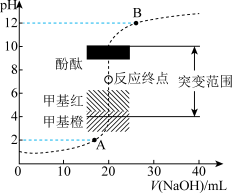

| A.溶液中水的电离程度:B=A |
| B.滴定开始时溶液的pH=1,滴定终点时溶液的pH=7 |
| C.当V(NaOH)=30.00mL时,溶液的pH=12.3 |
| D.酚酞、甲基橙和甲基红均可以作为滴定指示剂 |
您最近一年使用:0次
2022-01-20更新
|
302次组卷
|
3卷引用:云南省昆明市第一中学2023-2024学年高二上学期期中化学试题
名校
4 . 室温下,向20.00mL0.1000mol•L-1的某一元碱MOH溶液中滴加未知浓度的稀硫酸溶液,混合溶液的温度与pH随加如稀硫酸体积的变化如图所示。下列说法正确的是
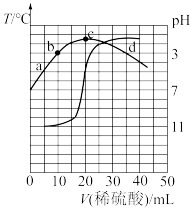

| A.稀硫酸的浓度为0.1000mol•L-1 |
| B.室温下MOH的电离平衡常数Kb=1.0×10-6 |
| C.b点对应的溶液中:2c(OH-)+c(MOH)=c(M+)+2c(H+) |
D.当pH=7时,溶液中存在c(H+)=c(OH-)<c(M+)<c(SO ) ) |
您最近一年使用:0次
2021-12-16更新
|
574次组卷
|
4卷引用:云南省曲靖市富源县第一中学2021-2022学年高二下学期期中考试化学试题
5 . 某烧碱样品含少量不与酸作用的杂质,为了测定其纯度,进行以下滴定操作:
A.在250 mL的容量瓶中定容配成250 mL烧碱溶液
B.用移液管移取25 mL烧碱溶液于锥形瓶中并滴几滴酚酞指示剂
C.在天平上准确称取烧碱样品W g,在烧杯中用蒸馏水溶解
D.将物质的量浓度为c mol·L-1的标准硫酸溶液装入酸式滴定管,调节液面,记下开始读数为V1
E.在锥形瓶下垫一张白纸,滴定至终点,记下读数V2
回答下列各问题:
(1)正确操作步骤的顺序是___ →___ →__ →D→__ (均用字母填写)。
(2)滴定管的读数应注意_____ 。
(3)E中在锥形瓶下垫一张白纸的作用是_____ 。
(4)D步骤中液面应调节到___ ,尖嘴部分应___ 。
(5)滴定终点时锥形瓶内溶液变化现象是____ 。
(6)若酸式滴定管不用标准硫酸润洗,在其他操作均正确的前提下,会对测定结果(指烧碱的纯度)有何影响?___ (填“偏高”、“偏低”或“不变”)。
(7)该烧碱样品纯度的计算式为____ 。
A.在250 mL的容量瓶中定容配成250 mL烧碱溶液
B.用移液管移取25 mL烧碱溶液于锥形瓶中并滴几滴酚酞指示剂
C.在天平上准确称取烧碱样品W g,在烧杯中用蒸馏水溶解
D.将物质的量浓度为c mol·L-1的标准硫酸溶液装入酸式滴定管,调节液面,记下开始读数为V1
E.在锥形瓶下垫一张白纸,滴定至终点,记下读数V2
回答下列各问题:
(1)正确操作步骤的顺序是
(2)滴定管的读数应注意
(3)E中在锥形瓶下垫一张白纸的作用是
(4)D步骤中液面应调节到
(5)滴定终点时锥形瓶内溶液变化现象是
(6)若酸式滴定管不用标准硫酸润洗,在其他操作均正确的前提下,会对测定结果(指烧碱的纯度)有何影响?
(7)该烧碱样品纯度的计算式为
您最近一年使用:0次
6 . I.无水MgBr2可用作催化剂,实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图所示(夹持装置省略)。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性
②MgBr2+3C2H5OC2H5 MgBr2·3C2H5OC2H5。
MgBr2·3C2H5OC2H5。
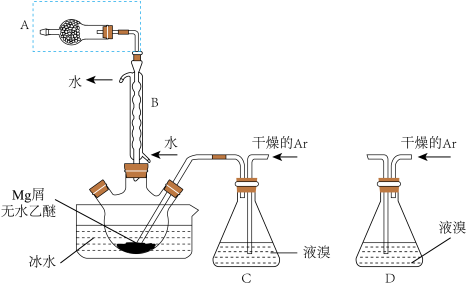
主要步骤如下:
步骤1:三颈烧瓶中装入10g镁屑和150mL无水乙醚;装置C中加入15mL液溴;
步骤2:缓慢通入干燥的氩气,直至溴完全导入三颈烧瓶中;
步骤3:反应完毕后恢复至室温,过滤除去镁,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品;
步骤4:常温下用CCl4溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
请回答下列问题
⑴仪器A的名称是___________ 。B的作用为___________ 。
⑵下列有关步骤4的说法正确的是___________ (填选项字母)
A.可用75%的乙醇代替CCl4溶解粗品
B.加热至160℃的主要目的是除去CCl4
C.洗涤晶体可选用0℃的CCl4
D.该步骤只除去了可能残留的溴
⑶若将装置C改为装置D,可能会导致的后果是___________ 。
⑷为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,以铬黑T(简写为In)为指示剂。已知Mg2+与铬黑T和EDTA均能形成配合物,且EDTA与Mg2+配合更稳定:
反应的离子方程式为Mg2++Y4-=MgY2-
①滴定终点的现象为______________________ 。
②测定前,先称取0.2500g无水MgBr2产品,溶解后,加入2滴铬黑T试液作指示剂,用0.0500mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50mL,则测得无水MgBr2产品的纯度是_______________ (用质量分数表示)。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性
②MgBr2+3C2H5OC2H5
 MgBr2·3C2H5OC2H5。
MgBr2·3C2H5OC2H5。
主要步骤如下:
步骤1:三颈烧瓶中装入10g镁屑和150mL无水乙醚;装置C中加入15mL液溴;
步骤2:缓慢通入干燥的氩气,直至溴完全导入三颈烧瓶中;
步骤3:反应完毕后恢复至室温,过滤除去镁,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品;
步骤4:常温下用CCl4溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
请回答下列问题
⑴仪器A的名称是
⑵下列有关步骤4的说法正确的是
A.可用75%的乙醇代替CCl4溶解粗品
B.加热至160℃的主要目的是除去CCl4
C.洗涤晶体可选用0℃的CCl4
D.该步骤只除去了可能残留的溴
⑶若将装置C改为装置D,可能会导致的后果是
⑷为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,以铬黑T(简写为In)为指示剂。已知Mg2+与铬黑T和EDTA均能形成配合物,且EDTA与Mg2+配合更稳定:
| 物质 | 颜色 | 物质 | 颜色 |
| Y4- | 无色 | MgY2- | 无色 |
| In | 纯蓝色 | MgIn- | 酒红色 |
①滴定终点的现象为
②测定前,先称取0.2500g无水MgBr2产品,溶解后,加入2滴铬黑T试液作指示剂,用0.0500mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50mL,则测得无水MgBr2产品的纯度是
您最近一年使用:0次
名校
解题方法
7 . Ⅰ.下列有关实验操作中,合理的是_________ (选填字母)。
A.用托盘天平称取11.70g食盐
B.用量筒量取12.36ml盐酸
C.用酸式滴定管量取21.20ml0.10mol·L-1H2SO4溶液
D.用200ml容量瓶配制100ml0.1mol·L-1NaCl溶液
Ⅱ.现用物质的量浓度为amol·L-1的标准盐酸去测定VmLNaOH溶液的物质的量浓度,请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,还应该进行的操作是_________ 。
(2)如图是酸式滴定管中液面在滴定前后的读数:
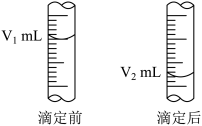
c(NaOH)=_________ mol/L。
(3)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度_________ 。(选填“偏大”、“偏小”、“无影响”)
III.t℃时,某稀硫酸溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知:a+b=12。
(4)该温度下水的离子积常数KW的数值为_________ 。
(5)该温度下(t℃),将100mL0.1mol·L-1的稀H2SO4与100mL0.4mol·L-1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=_________ 。
A.用托盘天平称取11.70g食盐
B.用量筒量取12.36ml盐酸
C.用酸式滴定管量取21.20ml0.10mol·L-1H2SO4溶液
D.用200ml容量瓶配制100ml0.1mol·L-1NaCl溶液
Ⅱ.现用物质的量浓度为amol·L-1的标准盐酸去测定VmLNaOH溶液的物质的量浓度,请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,还应该进行的操作是
(2)如图是酸式滴定管中液面在滴定前后的读数:

c(NaOH)=
(3)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度
III.t℃时,某稀硫酸溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知:a+b=12。
(4)该温度下水的离子积常数KW的数值为
(5)该温度下(t℃),将100mL0.1mol·L-1的稀H2SO4与100mL0.4mol·L-1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=
您最近一年使用:0次
9-10高一下·江西·期末
名校
解题方法
8 . 将V1 mL1.00mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL,下列叙述正确的是( )


| A.做该实验时环境温度为22℃ |
| B.该实验表明化学能可能转化为热能 |
| C.NaOH溶液的浓度约为1.00mol·L-1 |
| D.该实验表明有水生成的反应都是放热反应 |
您最近一年使用:0次
2020-03-19更新
|
1954次组卷
|
75卷引用:2015-2016学年云南省昆明三中高二下期中化学试卷
2015-2016学年云南省昆明三中高二下期中化学试卷(已下线)2010年云南省玉溪一中高二下学期期末考试化学试题(已下线)2010年黑龙江牡丹江一中高二上学期期中考试化学试卷(已下线)2011-2012年广东东莞南城中学高二上学期期中考试化学试卷(已下线)2011-2012学年浙江省杭州地区七校高二下学期期中联考化学试卷(已下线)2012-2013学年黑龙江省庆安三中高二上学期期中考试化学试卷(已下线)2012-2013学年重庆市第七中学高二上学期期中考试化学试卷2015-2016学年浙江省安吉县上墅私立高中高一下期中化学试卷西藏日喀则市第二高级中学2017-2018学年高二上学期期中考试化学试题安徽省淮北市第一中学2017-2018学年高一下学期期中考试化学试题浙江省浙东北联盟(ZDB)2019-2020学年高二上学期期中考试化学试题安徽省安庆市怀宁县怀宁中学2019-2020学年高一下学期期中考试化学试题陕西省西安市第八十九中学2018-2019学年高二上学期期中考试化学试题湖南大学附属中学2021-2022学年高二上学期期中考试化学试题云南省丽江市第一高级中学2021-2022学年高二上学期元月考化学试题天津市天津中学2022-2023学年高二上学期期中测试化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期中考试化学(选考)试题陕西省西安中学2023-2024学年高二上学期11月期中考试化学试题(已下线)09~10年江西白鹭洲中学高一下学期期末试题化学卷(已下线)2011-2012学年吉林省长春市十一高中高一下学期期初考试化学试卷(已下线)2012年苏教版高中化学选修6 6.1食醋总酸含量的测定练习卷(已下线)2014年高二化学人教版选修四 2中和反应反应热的测定练习卷(已下线)2015安徽望江中学同步课时练(人教选修4)1.1中和反应反应热的测定(已下线)2014-2015学年河南省南阳市新野三中上学期10月月考高二化学试卷2015-2016学年山西省右玉一中高二上学期第一次月考化学试卷2015-2016学年福建省师大附中高二上期末理化学试卷2015-2016学年山东省泰安市高一下学期期末考试化学试卷2017届河北省邯郸一中等五校高三上学期第一次模拟化学试卷2016-2017学年河北省辛集中学高一下学期第二次月考化学试卷湖北省沙市中学2017-2018学年高二上学期第二次双周考化学试题山西省实验中学2017-2018学年高二上学期10月月考化学试题江西省九江市2017-2018学年高二上学期第一次阶段联考化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题A内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题B广东省中山市2017-2018学年高二上学期期末考试化学试题山西省忻州第一中学2018-2019学年高二上学期第一次月考化学试题【全国百强校】广东省汕头市金山中学2018-2019学年高二上学期10月月考化学试题湖南省娄底市第四中学2018-2019学年高二上学期10月月考化学试题【全国百强校】山西省忻州市第一中学2018-2019学年高二上学期第一次月考化学试题湖北省荆州中学2018-2019学年高一下学期5月月考化学试题湖南省永州市东安县第一中学2019-2020学年高二上学期第一次月考化学试题甘肃省张掖市临泽县第一中学2019-2020学年高二上学期9月月考化学试题贵州省思南中学2019-2020学年高二9月月考化学试题人教版高中化学必修二第二单元《化学反应与能量》测试卷甘肃省酒泉市敦煌中学2020届高三上学期第二次调研考试化学试题2020届高三化学知识点强化训练—中和热四川省南充市阆中中学2020届高三化学选择题专项训练(22)山西省太原市山西省实验中学2019-2020学年高二上学期10月月考化学试题(已下线)1.1.1 化学反应的反应热 内能变化 练习——【高中新教材同步备课】鲁科版高中化学选择性必修1山东省滕州市第一中学2020-2021学年高二9月开学收心考试化学试题(已下线)1.1.2+热化学方程式-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)高一必修第二册(人教2019版)第六章 第一节 化学反应与能量变化 课时1 化学反应与能量变化鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第1节 化学反应的热效应 课时1 化学反应的反应热、内能变化与焓变人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 第一节 反应热 课时1 反应热 焓变(已下线)小题必刷31 酸碱中和滴定及拓展应用——2021年高考化学一轮复习小题必刷(通用版本)河北省衡水市第十四中学2020-2021学年高二上学期期末考试化学试题宁夏大学附属中学2020-2021学年高二下学期第一次月考化学试题选择性必修1(SJ)专题1第一单元课时3 反应热的测定(已下线)1.1.2 反应热的测量与计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)辽宁省大连市第一中学2021-2022学年高二上学期学情反馈(一)化学试题浙江省金华市第八中学2021-2022学年高二上学期9月月考化学试题浙江省磐安县第二中学2021-2022学年高二10月份竞赛化学试题黑龙江省哈尔滨市依兰县高级中学2021-2022学年高二上学期第一次月考化学试题安徽省南陵中学2021-2022学年高二上学期9月月考化学试题(已下线)1.2.1 反应热的测量和热化学方程式-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第15讲 化学反应的热效应 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)1.1.2 反应热(二)-同步学习必备知识河北省唐山市迁西县职业技术教育中心2021-2022学年高二(普职融通部)上学期9月月考化学试题安徽省庐江县2021-2022学年高二上学期期末考试化学试题四川省宜宾市叙州区第一中学校2022-2023学年高二下学期开学考试化学试题安徽省安庆市怀宁县第二中学2022-2023学年高二上学期期末考试化学试题5.3.1 化学变化中的能量变化(第1课时)-【帮课堂】高一化学同步精品讲义(沪科版2020必修第二册)宁夏六盘山高级中学2023-2024学年高二上学期第一次月考化学试题陕西省西安市 周至县第四中学2023-2024学年高二上学期10月份月考化学试题浙江省杭州市源清中学2023-2024学年高二上学期期末考试化学试题
9 . NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的Ka1=1.1×10−3 ,Ka2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是
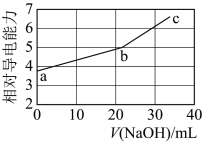

| A.混合溶液的导电能力与离子浓度和种类有关 |
| B.Na+与A2−的导电能力之和大于HA−的 |
| C.b点的混合溶液pH=7 |
| D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−) |
您最近一年使用:0次
2019-06-09更新
|
21039次组卷
|
67卷引用:云南师范大学附属中学2019-2020学年高二上学期期中考试化学试题
云南师范大学附属中学2019-2020学年高二上学期期中考试化学试题湖南省永州市宁远县第一中学2022-2023学年高二上学期期中考试化学试题广东省汕头市金山中学2022-2023学年高二下学期期中考试化学试题2019年全国统一考试化学试题(新课标Ⅰ)(已下线)专题10 水溶液中的离子平衡——2019年高考真题和模拟题化学分项汇编安徽省阜阳市颍上二中等三校2020届高三上学期入学考试化学试题(已下线)专题8.1 弱电解质的电离平衡(讲)-《2020年高考一轮复习讲练测》2020届高考化学小题狂练(全国通用版)专练15 弱电解质的电离平衡和溶液酸碱性湖南省株洲市茶陵二中2020届高三上学期第二次月考化学试题江苏省海安高级中学2019-2020学年高二12月月考化学试题福建省莆田第二十五中学2020届高三上学期期末考试化学试题专题2.3 水溶液中的离子平衡(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升湖南省长沙市天心区雅礼中学2018-2019学年高二下学期期末考试化学试题湖南省长沙市雅礼中学2019-2020学年高二上学期期末考试化学试题天津市海河中学2020届高三第二学期化学测试(二)试卷(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训辽宁省本溪市2019-2020学年高二下学期寒假验收考试化学试题江苏省南通市2020届高三第二次模拟考试(5月) 化学 试题黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题北京市海淀区育英学校2020届高三三模化学试题天津市第一中学2020届高三下学期第五次月考化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3章 综合检测高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三章素养检测(已下线)3.3.2+影响盐类水解的主要因素和盐类水解的应用-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 高考帮(已下线)第03章 水溶液中的离子反应与平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过高考 3年真题强化闯关第25讲 弱电解质的电离平衡(精讲)-2021年高考化学一轮复习讲练测(已下线)【浙江新东方】【2020】【高三上】【一模】【HD-LP416】【化学】(已下线)【浙江新东方】112(已下线)小题必刷31 酸碱中和滴定及拓展应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷30 水的电离与溶液的酸碱性——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷29 弱电解质的电离平衡——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷33 粒子浓度大小比较——2021年高考化学一轮复习小题必刷(通用版本)福建省连城县第一中学2021届高三上学期第二次月考化学试题(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题重庆市育才中学2021届高三下学期入学考试化学试题(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)专题07 电解质溶液——备战2021年高考化学纠错笔记(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)天津市南开中学2021届高三上学期第五次月考化学试卷(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)选择性必修1(SJ)专题3专题培优专练(已下线)考点23 弱电解质的电离-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时39 弱电解质的电离平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第21讲 电离平衡(讲)-2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第6讲 离子平衡坐标图像-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)重庆育才中学2021-2022学年高二上学期第四次定时练习化学试题山西省太原市第五中学2021-2022学年高二上学期12月月考化学试题(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习湖北省沙市中学2021-2022学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第4节 离子反应(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)浙江省绍兴市柯桥区2022届高考及选考科目5月适应性考试化学试题(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)河北省秦皇岛市第一中学2021-2022学年高二下学期期末考试化学试题天津市咸水沽第一中学2023届高三上学期第一次模拟考试化学试题(已下线)第21讲 电离平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题06 水溶液中的离子平衡(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)第八章 水溶液中的离子反应与平衡 第46讲 弱电解质的电离平衡(已下线)题型134 导电能力与酸碱中和滴定图像(已下线)专题16 水溶液中的离子平衡(已下线)T11-电解质溶液(已下线)第31讲盐类的水解2018-2019学年度耀华实验学校第二学期高二实验化学期末试卷
真题
名校
10 . 室温下,用0.l00mol/L NaOH溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是
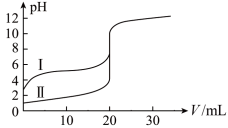

| A.II表示的是滴定醋酸的曲线 |
| B.pH=7时,滴定醋酸消耗的V(NaOH)小于20 mL |
| C.V(NaOH)=" 20.00" mL时,两份溶液中c(Cl-)= C(CH3COO-) |
| D.V(NaOH) ="10.00" mL时,醋酸溶液中c(Na+)> C(CH3COO-)> c(H+)> c(OH-) |
您最近一年使用:0次
2019-01-30更新
|
4228次组卷
|
50卷引用:云南省昆明市东川区明月中学2018-2019学年高二下学期期中考试化学试题
云南省昆明市东川区明月中学2018-2019学年高二下学期期中考试化学试题(已下线)2014-2015学年吉林省延边二中高二上学期期中理科化学卷2015-2016学年甘肃省天水一中高二上学期第一次段中考试化学试卷浙江省温州中学2017-2018学年高二上学期期中考试化学试题内蒙古自治区翁牛特旗乌丹第一中学2018-2019学年高二上学期期中考试化学试题湖北省恩施利川市第五中学2019-2020学年高二上学期期中考试化学试题黑龙江省鹤岗市第一中学2021-2022学年高二上学期期中考试化学试题北京市日坛中学2021-2022学年高二上学期期中考试化学试题北京市日坛中学2022-2023学年高二上学期期中考试化学试题北京市第二中学2023-2024学年高二上学期第二学段 段考化学试题2014年全国普通高等学校招生统一考试理科综合能力测试化学(海南卷)2015届安徽省芜湖一中高三上学期期末理综化学试卷2014-2015学年河北省正定中学高二下第三次月考化学试卷2015-2016学年山西省怀仁一中高二上11月月考化学试卷2015-2016学年山西省曲沃中学高二上学期12月月考化学试卷2015-2016学年重庆市杨家坪中学高二上学期第三次月考化学试卷2015-2016学年四川省广安市邻水等高二下学期期末联考化学试卷2017届江西省赣中南五校高三上学期第一次模拟考试化学试卷2016-2017学年安徽省六安一中高二上阶段测二化学卷2017届四川省眉山中学高三2月月考理科综合化学试卷安徽省黄山市2016-2017学年高二上学期期末质量检测化学试题湖北省武昌区2017届高三5月调研考试理综化学试题安徽省淮南市第二中学2017-2018学年高二上学期第二次月考化学试题陕西省西安市长安区第一中学2018届高三上学期第五次质量检测化学试题吉林省辽源市田家炳高级中学等五校2018届高三上学期期末联考化学试题广西陆川中学2017-2018学年高三化学上学期期末考试题江西省抚州市临川区第一中学2018届高三上学期期末考试理综-化学试题福建省莆田第一中学2017-2018学年高二下学期期初考试化学试题【全国百强校】陕西省西安市长安区第一中学2018-2019学年高二(理)上学期期末考试化学试题【全国百强校】福建省仙游第一中学2018-2019学年高二下学期第一次月考化学试题【区级联考】湖北省武汉市武昌区2019届高三下学期五月调研考试理科综合化学试题(已下线)专题10 水溶液中的离子平衡——2019年高考真题和模拟题化学分项汇编广西桂林十八中2020届高三上学期8月第一次月考化学试题河南省鹤壁市浚县二中2019-2020学年高二上学期第二次月考化学试题苏教版选修四化学反应原理专题3第三单元 盐类的水解 同步检测试卷【全国百强校】广西壮族自治区玉林高级中学2020届高三上学期第一次月考(8月)理综化学试题山西运城市运康中学校2019-2020学年高三12月月考化学试题广东省广州市天河中学2019-2020学年高二上学期能力性考试(11月月考)化学试题2020年春季人教版高中化学选修4第三章《水溶液中的离子平衡》测试卷2020届高三化学二轮冲刺新题专练—混合溶液中微粒浓度大小的比较夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——酸碱中和滴定专题2.3 水溶液中的离子平衡(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升四川省凉山州2018-2019学年高二下学期期期末考试化学试题陕西省延安市吴起高级中学2020-2021学年高二上学期第一次月考化学试题安徽省池州市第一中学2020-2021学年高二12月月考化学试题宁夏海原县第一中学2021届高三上学期期末考试化学试题甘肃省天水市第一中学2020-2021学年高二下学期开学考试化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期第四次教学质量检测化学试题浙江省诸暨市2017-2018学年高一下学期期末考试化学试题 重庆市璧山来凤中学2023-2024学年高二上学期12月月考化学试题



