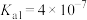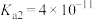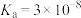1 . 已知: ,
, 。25℃时,向
。25℃时,向 溶液中滴加
溶液中滴加 的NaOH溶液。溶液中
的NaOH溶液。溶液中 与加入NaOH溶液体积的关系如图所示。下列说法
与加入NaOH溶液体积的关系如图所示。下列说法错误 的是
 ,
, 。25℃时,向
。25℃时,向 溶液中滴加
溶液中滴加 的NaOH溶液。溶液中
的NaOH溶液。溶液中 与加入NaOH溶液体积的关系如图所示。下列说法
与加入NaOH溶液体积的关系如图所示。下列说法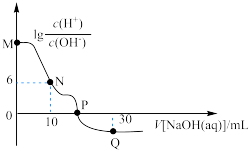
A.M点溶液中存在: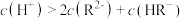 |
B.25℃时. 的水解常数 的水解常数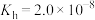 |
| C.P点加入NaOH溶液的体积小于20mL |
D.Q点溶液中存在: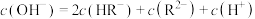 |
您最近一年使用:0次
名校
2 . 向100mL NaOH溶液中通入一定量 充分反应后,向所得溶液中,逐滴滴加1mol/L的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。
充分反应后,向所得溶液中,逐滴滴加1mol/L的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。 充分反应后,所得溶液的溶质为
充分反应后,所得溶液的溶质为___________ (填化学式)。
(2)已知25℃碳酸的 ,
, ,忽略
,忽略 和
和 浓度的变化,在滴加盐酸前,此时溶液pH=
浓度的变化,在滴加盐酸前,此时溶液pH=___________ 。
(3)关于该溶液的表达式正确的是___________。
 充分反应后,向所得溶液中,逐滴滴加1mol/L的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。
充分反应后,向所得溶液中,逐滴滴加1mol/L的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。
 充分反应后,所得溶液的溶质为
充分反应后,所得溶液的溶质为(2)已知25℃碳酸的
 ,
, ,忽略
,忽略 和
和 浓度的变化,在滴加盐酸前,此时溶液pH=
浓度的变化,在滴加盐酸前,此时溶液pH=(3)关于该溶液的表达式正确的是___________。
A. |
B. |
C. |
D. |
您最近一年使用:0次
名校
3 . 已知:25℃时, 的电离平衡常数
的电离平衡常数 、
、 。某小组同学用
。某小组同学用 溶液吸收
溶液吸收 得到吸收液w。
得到吸收液w。
1.请根据上述数据判断 溶液呈
溶液呈___________ (填“酸性”、“碱性”、“中性”),理由是:___________ 。
2.当吸收液w呈中性时,溶液中
___________  。
。
A. B.
B. C.
C.
 的电离平衡常数
的电离平衡常数 、
、 。某小组同学用
。某小组同学用 溶液吸收
溶液吸收 得到吸收液w。
得到吸收液w。1.请根据上述数据判断
 溶液呈
溶液呈2.当吸收液w呈中性时,溶液中

 。
。A.
 B.
B. C.
C.
您最近一年使用:0次
4 . 完成下列问题。
(1) 水溶液呈酸性的原因是(用离子方程式表示):
水溶液呈酸性的原因是(用离子方程式表示):________ 。
(2)室温时, 的
的 溶液中由水电离出的
溶液中由水电离出的
______  。
。
(3)室温时, 的Ba(OH)2溶液,
的Ba(OH)2溶液,
________ 。
(4)室温下pH=3的 水溶液水电离的c(H+)
水溶液水电离的c(H+)______  。
。
(5)常温下pH=13的 溶液与pH=11
溶液与pH=11 溶液等体积混合,混合溶液pH=
溶液等体积混合,混合溶液pH=______ 。
(6)常温下0.1 的NH3·H2O,pH=11,则Kb=
的NH3·H2O,pH=11,则Kb=_______ ,常温下0.1 的CH3COOH溶液pH=3 ,则Ka=
的CH3COOH溶液pH=3 ,则Ka=_______ 。
(1)
 水溶液呈酸性的原因是(用离子方程式表示):
水溶液呈酸性的原因是(用离子方程式表示):(2)室温时,
 的
的 溶液中由水电离出的
溶液中由水电离出的
 。
。(3)室温时,
 的Ba(OH)2溶液,
的Ba(OH)2溶液,
(4)室温下pH=3的
 水溶液水电离的c(H+)
水溶液水电离的c(H+) 。
。(5)常温下pH=13的
 溶液与pH=11
溶液与pH=11 溶液等体积混合,混合溶液pH=
溶液等体积混合,混合溶液pH=(6)常温下0.1
 的NH3·H2O,pH=11,则Kb=
的NH3·H2O,pH=11,则Kb= 的CH3COOH溶液pH=3 ,则Ka=
的CH3COOH溶液pH=3 ,则Ka=
您最近一年使用:0次
名校
5 . 已知常温下部分弱电解质的电离平衡常数如下表所示:
(1)25℃时,pH=10的NaClO溶液中各离子浓度的大小关系为_______ (离子浓度如Na+的浓度以c(Na+)表示,下同)。向NaClO溶液中通入少量CO2,反应的离子方程式为_______ 。
(2)NH4Cl溶液中的电荷守恒关系式为_______ 。
(3)NH4F溶液显_______ (填酸性、碱性或中性)。
(4)物质的量浓度相同的NaNO2、NaClO两种溶液,pH较大的是_______ 。
(5)泡沫灭火器利用了硫酸铝溶液和碳酸氢钠溶液的反应,用离子方程式表示原理_______ 。
(6)常温下,向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中 和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。_______ (填“A”或“B”)。
②当加入盐酸体积为50mL时,溶液中c( )∶c(NH3·H2O)=
)∶c(NH3·H2O)=_______ 。
| 化学式 | HF | HClO | H2CO3 | NH3·H2O | HNO2 |
| 电离常数 | 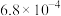 | 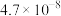 |  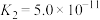 |  |  |
(1)25℃时,pH=10的NaClO溶液中各离子浓度的大小关系为
(2)NH4Cl溶液中的电荷守恒关系式为
(3)NH4F溶液显
(4)物质的量浓度相同的NaNO2、NaClO两种溶液,pH较大的是
(5)泡沫灭火器利用了硫酸铝溶液和碳酸氢钠溶液的反应,用离子方程式表示原理
(6)常温下,向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中
 和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。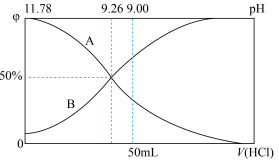
②当加入盐酸体积为50mL时,溶液中c(
 )∶c(NH3·H2O)=
)∶c(NH3·H2O)=
您最近一年使用:0次
6 . 回答下列问题
(1)现有a. b.HCl两种溶液,请回答下列问题(填“>”、“<”或“=”)。
b.HCl两种溶液,请回答下列问题(填“>”、“<”或“=”)。
①相同物质的量浓度的两种酸溶液中,水的电离程度的大小关系为a_________ b。
②pH相同、体积相同的两种酸溶液中分别加入足量锌,相同状况下产生气体体积大小关系为a_________ b。
将体积相同、pH=2的醋酸和pH=2的盐酸分别与pH=12的氢氧化钠溶液等体积混合,反应后溶液的pH的大小关系为a_________ b。
(2)常温下,根据表中的几种物质的电离平衡常数回答下列问题:
①下列反应不能发生的是_________ (填序号)。
a.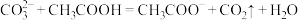
b.
c.
d.
②反应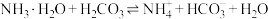 的平衡常数K=
的平衡常数K=_________ 。
(3)常温下,浓度均为0.1 的下列五种钠盐溶液的pH如下表:
的下列五种钠盐溶液的pH如下表:
①上述盐溶液中的阴离子,结合 能力最强的是
能力最强的是 _________ 。
②根据表中数据,浓度均为0.01 的下列四种酸的溶液分别稀释100倍,pH变化最大的是
的下列四种酸的溶液分别稀释100倍,pH变化最大的是_________ (填编号)。
A.HCN B.HClO C. D.
D.
(4)①已知t℃时,0.01 NaOH溶液的pH=11,0.1
NaOH溶液的pH=11,0.1 的HA溶液中
的HA溶液中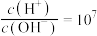 。该温度下,0.1
。该温度下,0.1 HA溶液中水电离出的
HA溶液中水电离出的
_________ 。
②25℃时,将体积 、pH=a的某一元强碱与体积为
、pH=a的某一元强碱与体积为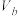 、pH=b的某二元强酸混合。若所得溶液的pH=11,且a=13,b=2,则
、pH=b的某二元强酸混合。若所得溶液的pH=11,且a=13,b=2,则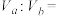
_________ 。
③25℃时,pH=5的醋酸和pH=5的 溶液中由水电离出的
溶液中由水电离出的 浓度之比为
浓度之比为_________ 。
(1)现有a.
 b.HCl两种溶液,请回答下列问题(填“>”、“<”或“=”)。
b.HCl两种溶液,请回答下列问题(填“>”、“<”或“=”)。①相同物质的量浓度的两种酸溶液中,水的电离程度的大小关系为a
②pH相同、体积相同的两种酸溶液中分别加入足量锌,相同状况下产生气体体积大小关系为a
将体积相同、pH=2的醋酸和pH=2的盐酸分别与pH=12的氢氧化钠溶液等体积混合,反应后溶液的pH的大小关系为a
(2)常温下,根据表中的几种物质的电离平衡常数回答下列问题:
弱酸 |
|
|
| HClO |
电离平衡常数 |
|
|
|
|
a.
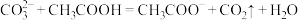
b.

c.

d.

②反应
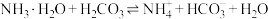 的平衡常数K=
的平衡常数K=(3)常温下,浓度均为0.1
 的下列五种钠盐溶液的pH如下表:
的下列五种钠盐溶液的pH如下表:溶质 |
|
|
| NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
 能力最强的是
能力最强的是 ②根据表中数据,浓度均为0.01
 的下列四种酸的溶液分别稀释100倍,pH变化最大的是
的下列四种酸的溶液分别稀释100倍,pH变化最大的是A.HCN B.HClO C.
 D.
D.
(4)①已知t℃时,0.01
 NaOH溶液的pH=11,0.1
NaOH溶液的pH=11,0.1 的HA溶液中
的HA溶液中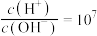 。该温度下,0.1
。该温度下,0.1 HA溶液中水电离出的
HA溶液中水电离出的
②25℃时,将体积
 、pH=a的某一元强碱与体积为
、pH=a的某一元强碱与体积为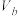 、pH=b的某二元强酸混合。若所得溶液的pH=11,且a=13,b=2,则
、pH=b的某二元强酸混合。若所得溶液的pH=11,且a=13,b=2,则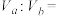
③25℃时,pH=5的醋酸和pH=5的
 溶液中由水电离出的
溶液中由水电离出的 浓度之比为
浓度之比为
您最近一年使用:0次
名校
解题方法
7 . 已知如下四种物质① ②
② ③NaOH④
③NaOH④
1.写出①的电离方程式_____ 。
2.向②的溶液中滴加几滴浓盐酸,平衡_____ 移动(填“正向”、“逆向”或“不移动”),平衡时溶液中
_____ (填“增大”、“减小”或者“不变”),
_____ (填“增大”、“减小”或者“不变”)。
3.将 的①溶液和
的①溶液和 的③溶液等体积混合后得到的溶液中主要溶质是
的③溶液等体积混合后得到的溶液中主要溶质是_____ (填化学式),该溶液显酸性,原因是_____ (请用文字结合该溶液中两个相关平衡方程式加以说明)。
4.将标准状况下2.24L④缓慢通入 的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为
的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为_____ ,该溶液中各离子浓度大小关系_____ 。
5.将足量④缓慢通入 的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度_____ 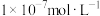 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH_____ (填“增大”、“减小”、或“不变”)。
 ②
② ③NaOH④
③NaOH④
1.写出①的电离方程式
2.向②的溶液中滴加几滴浓盐酸,平衡


3.将
 的①溶液和
的①溶液和 的③溶液等体积混合后得到的溶液中主要溶质是
的③溶液等体积混合后得到的溶液中主要溶质是4.将标准状况下2.24L④缓慢通入
 的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为
的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为5.将足量④缓慢通入
 的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度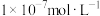 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH
您最近一年使用:0次
名校
8 . 25℃时部分弱酸的电离平衡常数如下表:
1.室温下① ②
② ③
③ ④
④ ,溶液的pH由大到小的关系为(填序号)
,溶液的pH由大到小的关系为(填序号)_____ 。
2.下列离子方程式书写正确的是
| 弱酸 |  |  |  |  |
| 电离平衡常数 |  |  |   |   |
 ②
② ③
③ ④
④ ,溶液的pH由大到小的关系为(填序号)
,溶液的pH由大到小的关系为(填序号)2.下列离子方程式书写正确的是
A.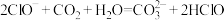 |
B. |
C. |
D. |
您最近一年使用:0次
名校
9 . 烟气脱硫可有效减少 引起的大气污染,同时还可得到有用产品。传统湿法脱硫多以碱性物质作吸收剂,新型脱硫方法选用离子液体(指在室温或接近室温时呈液态的盐类物质,由正、负离子组成)作吸收剂,通过物理和化学吸收实现脱硫。
引起的大气污染,同时还可得到有用产品。传统湿法脱硫多以碱性物质作吸收剂,新型脱硫方法选用离子液体(指在室温或接近室温时呈液态的盐类物质,由正、负离子组成)作吸收剂,通过物理和化学吸收实现脱硫。
已知25℃时,几种酸的电离常数:
(1)下列物质不属于电解质的是________。
(2)传统湿法脱硫涉及的下列离子方程式中,正确的是________。
(3)请运用相关化学用语解释 溶液呈现碱性的原因:
溶液呈现碱性的原因:___________________________ 。
研究发现:乳酸和乙醇胺( 作用得到的离子液体—乙醇胺乳酸盐(),既可脱硫,也可吸收
作用得到的离子液体—乙醇胺乳酸盐(),既可脱硫,也可吸收 。
。
(4)液态时的导电性: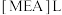
________ 乳酸(填“>”、“<”或“=”"),原因是________________ *。
(5)常温下,水电离的 相同的三种溶液:①
相同的三种溶液:① ②
② ③
③ ,其浓度由大到小的顺序是
,其浓度由大到小的顺序是________ (填序号)。
(6) 溶液加水稀释过程中,下列数据变大的是________。
溶液加水稀释过程中,下列数据变大的是________。
(7)向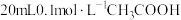 中逐滴加入
中逐滴加入 过程中,
过程中, 变化如图所示。下列说法不正确的是________。
变化如图所示。下列说法不正确的是________。

(8)在进行胃部透视时,为取得良好的检查效果,需在检查前服用“钡餐”,“钡餐”的主要成分是硫酸钡。在25℃时,硫酸钡的溶度积常数为 。钡离子是有毒的重金属离子,当体内钡离子浓度达到
。钡离子是有毒的重金属离子,当体内钡离子浓度达到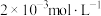 时,就会对健康产生危害。请计算并从沉淀溶解平衡的角度说明使用硫酸钡而不使用碳酸钡作为“钡餐”的主要成分的原因:
时,就会对健康产生危害。请计算并从沉淀溶解平衡的角度说明使用硫酸钡而不使用碳酸钡作为“钡餐”的主要成分的原因:________________________________ 。
 引起的大气污染,同时还可得到有用产品。传统湿法脱硫多以碱性物质作吸收剂,新型脱硫方法选用离子液体(指在室温或接近室温时呈液态的盐类物质,由正、负离子组成)作吸收剂,通过物理和化学吸收实现脱硫。
引起的大气污染,同时还可得到有用产品。传统湿法脱硫多以碱性物质作吸收剂,新型脱硫方法选用离子液体(指在室温或接近室温时呈液态的盐类物质,由正、负离子组成)作吸收剂,通过物理和化学吸收实现脱硫。已知25℃时,几种酸的电离常数:
| 酸 |  |  |  (乳酸) | HCN |  |
| 电离常数 | 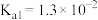 | 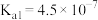 | 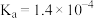 | 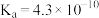 |  |
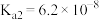 | 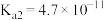 |
A. | B. | C. | D. |
A.烟气与氧化镁浆液的反应: |
B.烟气与石灰石浆液反应得到石膏: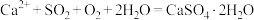 |
C.烟气与氨水反应得到硫酸铵: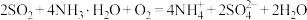 |
D.烟气与海水中 的反应: 的反应: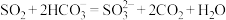 |
 溶液呈现碱性的原因:
溶液呈现碱性的原因:研究发现:乳酸和乙醇胺(
 作用得到的离子液体—乙醇胺乳酸盐(),既可脱硫,也可吸收
作用得到的离子液体—乙醇胺乳酸盐(),既可脱硫,也可吸收 。
。(4)液态时的导电性:
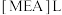
(5)常温下,水电离的
 相同的三种溶液:①
相同的三种溶液:① ②
② ③
③ ,其浓度由大到小的顺序是
,其浓度由大到小的顺序是(6)
 溶液加水稀释过程中,下列数据变大的是________。
溶液加水稀释过程中,下列数据变大的是________。A. | B. | C.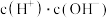 | D. |
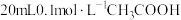 中逐滴加入
中逐滴加入 过程中,
过程中, 变化如图所示。下列说法不正确的是________。
变化如图所示。下列说法不正确的是________。
A.A、C两点水的电离程度: |
B.B点溶液中: |
C.若 点为恰好完全中和的点,则溶液中: 点为恰好完全中和的点,则溶液中: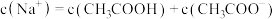 |
D.溶液 时, 时, |
 。钡离子是有毒的重金属离子,当体内钡离子浓度达到
。钡离子是有毒的重金属离子,当体内钡离子浓度达到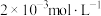 时,就会对健康产生危害。请计算并从沉淀溶解平衡的角度说明使用硫酸钡而不使用碳酸钡作为“钡餐”的主要成分的原因:
时,就会对健康产生危害。请计算并从沉淀溶解平衡的角度说明使用硫酸钡而不使用碳酸钡作为“钡餐”的主要成分的原因:
您最近一年使用:0次
名校
10 . 自然界碳的循环与 、碳酸及碳酸盐有着密切的联系。
、碳酸及碳酸盐有着密切的联系。
(1) 的空间构型为
的空间构型为___________ , 分子中σ键与π键的个数比为
分子中σ键与π键的个数比为___________ 。
(2)常温常压下,空气中 溶于水达到平衡时
溶于水达到平衡时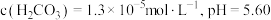 。若忽略水的电离及
。若忽略水的电离及 的第二级电离,则碳酸的一级电离常数
的第二级电离,则碳酸的一级电离常数
___________ (已知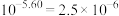 ,结果保留1位小数)。
,结果保留1位小数)。
(3)已知 的二级电离常数
的二级电离常数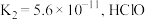 的电离常数
的电离常数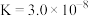 。将少量
。将少量 通入过量的
通入过量的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为___________ 。
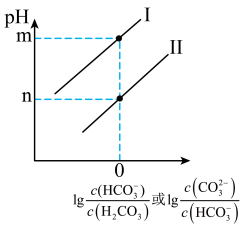
(4)在常温下向 水溶液中滴加
水溶液中滴加 溶液,所得溶液的
溶液,所得溶液的 与粒子浓度的变化关系如图。则下图中
与粒子浓度的变化关系如图。则下图中___________ 线(填“I”或“Ⅱ”)表示 ,碳酸的两级电离常数
,碳酸的两级电离常数 与
与 的关系为
的关系为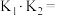
___________ (用含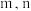 的式子表示)。
的式子表示)。
 、碳酸及碳酸盐有着密切的联系。
、碳酸及碳酸盐有着密切的联系。(1)
 的空间构型为
的空间构型为 分子中σ键与π键的个数比为
分子中σ键与π键的个数比为(2)常温常压下,空气中
 溶于水达到平衡时
溶于水达到平衡时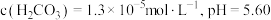 。若忽略水的电离及
。若忽略水的电离及 的第二级电离,则碳酸的一级电离常数
的第二级电离,则碳酸的一级电离常数
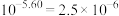 ,结果保留1位小数)。
,结果保留1位小数)。(3)已知
 的二级电离常数
的二级电离常数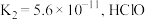 的电离常数
的电离常数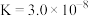 。将少量
。将少量 通入过量的
通入过量的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为(4)在常温下向
 水溶液中滴加
水溶液中滴加 溶液,所得溶液的
溶液,所得溶液的 与粒子浓度的变化关系如图。则下图中
与粒子浓度的变化关系如图。则下图中 ,碳酸的两级电离常数
,碳酸的两级电离常数 与
与 的关系为
的关系为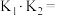
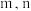 的式子表示)。
的式子表示)。
您最近一年使用:0次
2024-03-16更新
|
157次组卷
|
2卷引用:云南省昆明市云南师范大学实验中学2023-2024学年高二下学期3月月考化学试题