1 . 2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:
(1)在一定温度下,向体积固定的密闭容器中加入足量的 和
和 ,起始压强为
,起始压强为 时,发生下列反应生成水煤气:
时,发生下列反应生成水煤气:
Ⅰ.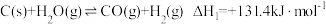
Ⅱ.
①下列说法正确的是_______ ;
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时 的体积分数可能大于
的体积分数可能大于
D.将炭块粉碎,可加快反应速率
②反应平衡时, 的转化率为
的转化率为 ,CO的物质的量为
,CO的物质的量为 。此时,整个体系
。此时,整个体系_______ (填“吸收”或“放出”)热量_______ kJ,反应Ⅰ的平衡常数
_______ (以分压表示,分压=总压×物质的量分数)。
(2)一种脱除和利用水煤气中 方法的示意图如下:
方法的示意图如下:
 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液的
,则该溶液的
_______ (该温度下 的
的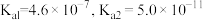 );
);
②再生塔中产生 的离子方程式为
的离子方程式为_______ ;
③利用电化学原理,将 电催化还原为
电催化还原为 ,阴极反应式为
,阴极反应式为_______ 。
(1)在一定温度下,向体积固定的密闭容器中加入足量的
 和
和 ,起始压强为
,起始压强为 时,发生下列反应生成水煤气:
时,发生下列反应生成水煤气:Ⅰ.
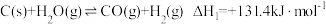
Ⅱ.

①下列说法正确的是
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时
 的体积分数可能大于
的体积分数可能大于
D.将炭块粉碎,可加快反应速率
②反应平衡时,
 的转化率为
的转化率为 ,CO的物质的量为
,CO的物质的量为 。此时,整个体系
。此时,整个体系
(2)一种脱除和利用水煤气中
 方法的示意图如下:
方法的示意图如下: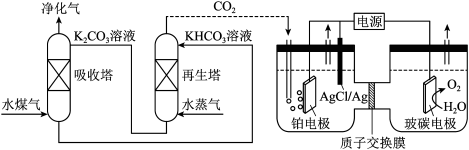
 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液的
,则该溶液的
 的
的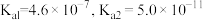 );
);②再生塔中产生
 的离子方程式为
的离子方程式为③利用电化学原理,将
 电催化还原为
电催化还原为 ,阴极反应式为
,阴极反应式为
您最近一年使用:0次
2022-06-10更新
|
11371次组卷
|
21卷引用:模块综合检测卷2
模块综合检测卷22022年新高考湖南化学高考真题(已下线)2022年湖南卷高考真题变式题(15-19)(已下线)专题14 化学反应原理综合题-2022年高考真题模拟题分项汇编(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题18 化学反应原理综合题-备战2023年高考化学母题题源解密(广东卷)广东省汕头市金山中学2022-2023学年高三上学期第二次月考化学试题山东省枣庄市第三中学2022-2023学年高三上学期期中考试化学试题广东省佛山市顺德区第一中学2023届高三上学期12月综合训练化学试题安徽省六安第一中学2022-2023学年高二上学期期末考试化学试题山东省潍坊市昌乐第一中学2022-2023学年高二上学期期末拉练二化学试题(已下线)回归教材重难点08 聚焦热、速率、平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)第20练 化学反应原理综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题14 化学反应原理综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)四川省眉山市彭山区第一中学2023-2024学年高三上学期11月月考理综试题 河南省南阳市第一中学校2024届高三上学期阶段检测化学试题(12月)湖南省浏阳景雅高级中学2024届高三下学期5月全真仿真模拟考试化学试题
名校
解题方法
2 . (1)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
a.当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是_______ (用字母表示,下同)。
b.同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是_______ 。
c.若三者c(H+)相同时,物质的量浓度由大到小的顺序是_______ 。
d.将c(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积大小关系为_______ 。
e.将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是_______ 。
(2)当H2S浓度较低时常用纯碱溶液进行吸收。表为H2S、H2CO3 的电离平衡常数。
纯碱溶液吸收少量H2S的离子方程式为_______ 。
(3)磷酸是三元弱酸,常温下三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13,解答下列问题:
a.常温下同浓度①Na3PO4、②Na2HPO4、③NaH2PO4的pH由小到大的顺序是_______ (填序号)。
b.常温下,NaH2PO4的水溶液pH_______ (填“>”“<”或“=”)7。
c.常温下,Na2HPO4的水溶液呈_______ (填“酸”“碱”或“中”)性
a.当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
b.同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是
c.若三者c(H+)相同时,物质的量浓度由大到小的顺序是
d.将c(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积大小关系为
e.将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是
(2)当H2S浓度较低时常用纯碱溶液进行吸收。表为H2S、H2CO3 的电离平衡常数。
| 电离平衡常数 | Kal | Ka2 |
| H2S | 9.1×10-8 | 1.1×10-12 |
| H2CO3 | 4.3×10-7 | 5.61×10-11 |
纯碱溶液吸收少量H2S的离子方程式为
(3)磷酸是三元弱酸,常温下三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13,解答下列问题:
a.常温下同浓度①Na3PO4、②Na2HPO4、③NaH2PO4的pH由小到大的顺序是
b.常温下,NaH2PO4的水溶液pH
c.常温下,Na2HPO4的水溶液呈
您最近一年使用:0次
3 . 如表所示是几种弱电解质的电离平衡常数和某难溶电解质的溶度积Ksp (25℃)。
回答下列问题:
(1)由上表分析,若①CH3COOH,②HCO ,③C6H5OH,④H2PO
,③C6H5OH,④H2PO 均可看成酸,则它们的酸性由强到弱的顺序为
均可看成酸,则它们的酸性由强到弱的顺序为_________ (填序号)。
(2)25℃时,将等体积、等浓度的CH3COOH溶液和氨水混合,混合液中:c(CH3COO-)
______ (填“>”“=”或“<”)c(NH )
)
(3)25℃时,向10mL 0.01mol•L-1苯酚溶液中滴加VmL 0.01mol•L-1氨水,下列说法正确的是________ (填序号)。
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(NH )>c(C6H5O-)>c(H+)>c(OH-)
)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10液中水的电离程度小于10mL 0.01mol•L-1苯酚溶液中水的电离程度
D. V=5时,2c(NH3•H2O)+2c(NH )=c(C6H5O-)+c(C6H5OH)
)=c(C6H5O-)+c(C6H5OH)
(4)如图所示为某温度时BaSO4的沉淀溶解平衡曲线,下列说法不正确的是______ (填序号)。
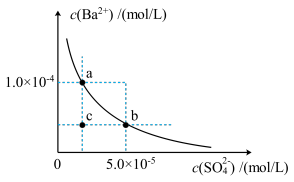
A.加入Na2SO4可使溶液由a点变为b点
B.在曲线上方区域任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由c点变为曲线上a、b之间的某一点(不含a、b)
D.升高温度,可使溶液由b点变为c点
| 电解质 | 平衡方程式 | 平衡常数K | Ksp |
| CH3COOH | CH3COOH CH3COO-+H+ CH3COO-+H+ | 1.8×10-5 | |
| H2CO3 | H2CO3 H++ HCO H++ HCO HCO   H++CO H++CO | Ka1=4.5×10-7 Ka2=4.7×10-11 | |
| C6H5OH | C6H5OH C6H5O-+H+ C6H5O-+H+ | 1.0×10-10 | |
| H3PO4 | H3PO4 H++H2PO H++H2PO H2PO   H++HPO H++HPO HPO   H++PO H++PO | Ka1=6.9×10-3 Ka2=6.2×10-8 Ka3=4.8×10-13 | |
| NH3·H2O | NH3·H2O NH NH +OH- +OH- | 1.8×10-5 | |
| BaSO4 | BaSO4(s) Ba2+(aq)+SO Ba2+(aq)+SO (aq) (aq) | 1.1×10-10 |
(1)由上表分析,若①CH3COOH,②HCO
 ,③C6H5OH,④H2PO
,③C6H5OH,④H2PO 均可看成酸,则它们的酸性由强到弱的顺序为
均可看成酸,则它们的酸性由强到弱的顺序为(2)25℃时,将等体积、等浓度的CH3COOH溶液和氨水混合,混合液中:c(CH3COO-)
 )
)(3)25℃时,向10mL 0.01mol•L-1苯酚溶液中滴加VmL 0.01mol•L-1氨水,下列说法正确的是
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(NH
 )>c(C6H5O-)>c(H+)>c(OH-)
)>c(C6H5O-)>c(H+)>c(OH-)C.V=10液中水的电离程度小于10mL 0.01mol•L-1苯酚溶液中水的电离程度
D. V=5时,2c(NH3•H2O)+2c(NH
 )=c(C6H5O-)+c(C6H5OH)
)=c(C6H5O-)+c(C6H5OH)(4)如图所示为某温度时BaSO4的沉淀溶解平衡曲线,下列说法不正确的是

A.加入Na2SO4可使溶液由a点变为b点
B.在曲线上方区域任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由c点变为曲线上a、b之间的某一点(不含a、b)
D.升高温度,可使溶液由b点变为c点
您最近一年使用:0次
2020-10-13更新
|
235次组卷
|
4卷引用:鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 易错疑难集训(二)
名校
解题方法
4 . 已知K、Ka、Kw、Ksp分别表示化学平衡常数、弱酸的电离平衡常数、水的离子积常数、难溶电解质的溶度积常数。
(1)有关上述常数的说法正确的是_____ 。
a.它们的大小都随温度的升高而增大
b.它们都能反映一定条件下对应可逆过程进行的程度
c.常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
(2)已知25℃时CH3COOH和NH3·H2O电离常数相等,则该温度下CH3COONH4溶液的pH=_______ ,溶液中离子浓度大小关系为_________________________________ 。
(3)硝酸铜溶液蒸干、灼烧后得到的固体物质是___________ 。
(4)明矾净水原理______________________________________ 。(用离子方程式表示)
(5)已知在25℃时Ksp[AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1×10-12。25℃时,向浓度均为0.02mol·L-1的NaCl和Na2CrO4混合溶液中逐滴加入AgNO3溶液,先析出_______ (填化学式)沉淀,当两种沉淀共存时, =
=_________ 。
(1)有关上述常数的说法正确的是
a.它们的大小都随温度的升高而增大
b.它们都能反映一定条件下对应可逆过程进行的程度
c.常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
(2)已知25℃时CH3COOH和NH3·H2O电离常数相等,则该温度下CH3COONH4溶液的pH=
(3)硝酸铜溶液蒸干、灼烧后得到的固体物质是
(4)明矾净水原理
(5)已知在25℃时Ksp[AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1×10-12。25℃时,向浓度均为0.02mol·L-1的NaCl和Na2CrO4混合溶液中逐滴加入AgNO3溶液,先析出
 =
=
您最近一年使用:0次
5 . 实验是化学的灵魂。
(1)中和滴定是重要的定量实验,实验成功的关键是准确读数和终点判断。
①如图I表示10 mL量筒中液面的位置,A与B,B与C刻度间相差1 mL,如果刻度A为5,量筒中液体的体积是______ mL。
②如图 II表示50 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体体积为_____ (填代号)。
A.a mL B.大于a mL C.等于(50-a) mL D.大于(50-a) mL

(2)某研究性学习小组用0.2000 mol·L-1 NaOH标准溶液滴定20.00 mL 醋酸溶液的浓度,实验数据记录如下:
①计算醋酸溶液的浓度______________ 保留四位有效数字 。
②关于该滴定实验,从下列选项中选出最恰当的一项______ 选填字母。
(3)浓度影响弱酸、弱碱的电离程度。用pH计测定时不同浓度的醋酸的pH,结果如表:
①根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是___________ 。
②从表中的数据,还可以得出另一结论:随着醋酸浓度的增大,醋酸的电离程度将_________ 填“增大”“减小”或“不变”。
(4)多元弱酸分步电离,以第一步电离为主,即电离常数Ka1>Ka2。
向0.10 二元弱酸H2A溶液逐滴滴入NaOH溶液,溶液中的H2A、HA-、A2-的物质的量分数
二元弱酸H2A溶液逐滴滴入NaOH溶液,溶液中的H2A、HA-、A2-的物质的量分数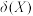 随pH的变化如图所示[已知
随pH的变化如图所示[已知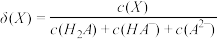 ]。则Ka1: Ka2=
]。则Ka1: Ka2=_______ 。

(5)温度影响弱酸、弱碱的电离。以醋酸为例,设计如下实验方案进行验证:用pH计或精密pH试纸测定相同浓度的醋酸在不同________ 的pH。
(1)中和滴定是重要的定量实验,实验成功的关键是准确读数和终点判断。
①如图I表示10 mL量筒中液面的位置,A与B,B与C刻度间相差1 mL,如果刻度A为5,量筒中液体的体积是
②如图 II表示50 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体体积为
A.a mL B.大于a mL C.等于(50-a) mL D.大于(50-a) mL

(2)某研究性学习小组用0.2000 mol·L-1 NaOH标准溶液滴定20.00 mL 醋酸溶液的浓度,实验数据记录如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积 | 20.07 | 20.02 | 18.80 | 19.97 |
①计算醋酸溶液的浓度
②关于该滴定实验,从下列选项中选出最恰当的一项
| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 石蕊 | 乙 |
| B | 酸 | 碱 | 甲基橙 | 甲 |
| C | 酸 | 碱 | 酚酞 | 乙 |
| D | 碱 | 酸 | 酚酞 | 甲 |
(3)浓度影响弱酸、弱碱的电离程度。用pH计测定时不同浓度的醋酸的pH,结果如表:
| 醋酸浓度 | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
①根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是
②从表中的数据,还可以得出另一结论:随着醋酸浓度的增大,醋酸的电离程度将
(4)多元弱酸分步电离,以第一步电离为主,即电离常数Ka1>Ka2。
向0.10
 二元弱酸H2A溶液逐滴滴入NaOH溶液,溶液中的H2A、HA-、A2-的物质的量分数
二元弱酸H2A溶液逐滴滴入NaOH溶液,溶液中的H2A、HA-、A2-的物质的量分数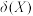 随pH的变化如图所示[已知
随pH的变化如图所示[已知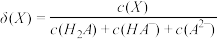 ]。则Ka1: Ka2=
]。则Ka1: Ka2=
(5)温度影响弱酸、弱碱的电离。以醋酸为例,设计如下实验方案进行验证:用pH计或精密pH试纸测定相同浓度的醋酸在不同
您最近一年使用:0次
名校
6 . 电解质的水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。下列方法中,可以使醋酸稀溶液中CH3COOH电离程度增大的是_________ (填字母序号)。
a. 滴加少量浓盐酸 b. 微热溶液 c. 加水稀释 d. 加入少量醋酸钠晶体
(2)白醋是常见的烹调酸味辅料,白醋总酸度测定方法如下。
a.量取20.00 mL白醋样品,用100 mL容量瓶配制成待测液。
b.将滴定管洗净、润洗,装入溶液,赶出尖嘴处气泡,调整液面至0刻度线。
c.取20.00 mL配制的待测液于洁净的锥形瓶中,加3滴酚酞溶液,用0.1000 mol· L-1的NaOH溶液滴定至终点,记录数据。
d.重复滴定实验3次并记录数据。
e.计算白醋样品中醋酸总酸度。回答下列问题:
①实验a中量取20.00 mL白醋所用的仪器名称是_____________________ 。
②若实验b中碱式滴定管未用NaOH标准溶液润洗,会造成测定结果比准确值_____________ (填“偏大”、“偏小”或“不变”)。
③实验C中判断滴定终点的现象是________________________________ 。
④实验数据如下表,则该白醋样品中醋酸总酸度为________________ mol· L-1。
(1)醋酸是常见的弱酸。下列方法中,可以使醋酸稀溶液中CH3COOH电离程度增大的是
a. 滴加少量浓盐酸 b. 微热溶液 c. 加水稀释 d. 加入少量醋酸钠晶体
(2)白醋是常见的烹调酸味辅料,白醋总酸度测定方法如下。
a.量取20.00 mL白醋样品,用100 mL容量瓶配制成待测液。
b.将滴定管洗净、润洗,装入溶液,赶出尖嘴处气泡,调整液面至0刻度线。
c.取20.00 mL配制的待测液于洁净的锥形瓶中,加3滴酚酞溶液,用0.1000 mol· L-1的NaOH溶液滴定至终点,记录数据。
d.重复滴定实验3次并记录数据。
e.计算白醋样品中醋酸总酸度。回答下列问题:
①实验a中量取20.00 mL白醋所用的仪器名称是
②若实验b中碱式滴定管未用NaOH标准溶液润洗,会造成测定结果比准确值
③实验C中判断滴定终点的现象是
④实验数据如下表,则该白醋样品中醋酸总酸度为
待测液体积/mL | 标准NaOH溶液 | ||
滴定前读数/mL | 滴定终点读数/mL | ||
第1次 | 20.00 | 0 | 21.98 |
第2次 | 20.00 | 0 | 22.00 |
第3次 | 20.00 | 0 | 22.02 |
您最近一年使用:0次
2020-01-14更新
|
183次组卷
|
3卷引用:第二节 离子反应(一)-2020-2021学年高一化学必修第一册课时同步练(新人教)
(已下线)第二节 离子反应(一)-2020-2021学年高一化学必修第一册课时同步练(新人教)湖北省宜昌市部分示范高中教学协作体2019-2020学年高二上学期期末联考化学试题四川省泸县第四中学2019-2020学年高二下学期第一次在线月考化学试题
名校
解题方法
7 . 常温下向20.00 mL 0.10 mol/L Na2CO3溶液中逐滴加入0.10 mol/L盐酸40.00 mL,所得溶液的pH与加入盐酸体积的关系如表所示:
回答下列问题:
(1)20.00 mL 0.10 mol/L Na2CO3溶液中所有阳离子和阴离子的浓度有何关系?______ (用等式表示)。
(2)当V(HCl)=20.00 mL时,溶液呈碱性的原因是________ (用离子方程式和必要的文字说明)此时溶液中c(H2CO3)____ (填“>”、“<”或“=”)c(CO32—)。
(3)V(HCl)=40.00 mL时,得到H2CO3饱和溶液,且c(H2CO3)=4.0×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3—+H+的电离常数K1=
HCO3—+H+的电离常数K1=_____ 。此时保持其他条件不变,继续加入0.1 mol/L盐酸10.00 mL,K1将_____ (填“变大”、“变小”或“不变”)。
(4)若向20 mL 0.10 mol/L Na2CO3溶液中加入BaCl2粉末3.94×10-7 g时开始产生沉淀BaCO3,则Ksp(Ba2CO3)= 。
| 溶液的pH | 加入盐酸的总体积 |
| 12 | V(HCl)=0 |
| 8 | V(HCl)=20.00 mL |
| 5 | V(HCl)=40.00 mL |
回答下列问题:
(1)20.00 mL 0.10 mol/L Na2CO3溶液中所有阳离子和阴离子的浓度有何关系?
(2)当V(HCl)=20.00 mL时,溶液呈碱性的原因是
(3)V(HCl)=40.00 mL时,得到H2CO3饱和溶液,且c(H2CO3)=4.0×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3
 HCO3—+H+的电离常数K1=
HCO3—+H+的电离常数K1=(4)若向20 mL 0.10 mol/L Na2CO3溶液中加入BaCl2粉末3.94×10-7 g时开始产生沉淀BaCO3,则Ksp(Ba2CO3)= 。
您最近一年使用:0次
2018-09-08更新
|
1137次组卷
|
6卷引用:人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 章末综合检测卷
8 . 砷(As)是一些工厂和矿山废水中的污染元素,使用吸附剂是去除水中砷的有效措施之一。
(1)将硫酸锰、硝酸钇与氢氧化钠溶液按一定比例混合,搅拌使其充分反应,可获得一种砷的高效吸附剂X,吸附剂X中含有 ,其原因是
,其原因是_______________________________ 。
(2)H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图- 1和图- 2所示。

①以酚酞为指示剂(变色范围pH 8.0 ~ 10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为__________________ 。
②H3AsO4第一步电离方程式H3AsO4⇌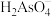 +H+的电离常数为Ka1,则pKa1=
+H+的电离常数为Ka1,则pKa1=______ (p Ka1 = -lg Ka1 )。
(3)溶液的pH对吸附剂X表面所带电荷有影响。pH =7.1时, 吸附剂X表面不带电荷;pH > 7.1时带负电荷,pH越高,表面所带负电荷越多;pH<7.1时带正电荷,pH越低,表面所带正电荷越多。pH不同时吸附剂X对三价砷和五价砷的平衡吸附量(吸附达平衡时单位质量吸附剂X吸附砷的质量)如图-3所示。

①在pH7~9之间,吸附剂X对五价砷的平衡吸附量随pH升高而迅速下降,其原因是______________ 。
②在pH4~7之间,吸附剂X对水中三价砷的去除能力远比五价砷的弱,这是因为___________ 。 提高吸附剂X对三价砷去除效果可采取的措施是_________________________________ 。
(1)将硫酸锰、硝酸钇与氢氧化钠溶液按一定比例混合,搅拌使其充分反应,可获得一种砷的高效吸附剂X,吸附剂X中含有
 ,其原因是
,其原因是(2)H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图- 1和图- 2所示。

①以酚酞为指示剂(变色范围pH 8.0 ~ 10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为
②H3AsO4第一步电离方程式H3AsO4⇌
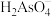 +H+的电离常数为Ka1,则pKa1=
+H+的电离常数为Ka1,则pKa1=(3)溶液的pH对吸附剂X表面所带电荷有影响。pH =7.1时, 吸附剂X表面不带电荷;pH > 7.1时带负电荷,pH越高,表面所带负电荷越多;pH<7.1时带正电荷,pH越低,表面所带正电荷越多。pH不同时吸附剂X对三价砷和五价砷的平衡吸附量(吸附达平衡时单位质量吸附剂X吸附砷的质量)如图-3所示。

①在pH7~9之间,吸附剂X对五价砷的平衡吸附量随pH升高而迅速下降,其原因是
②在pH4~7之间,吸附剂X对水中三价砷的去除能力远比五价砷的弱,这是因为
您最近一年使用:0次
2017-08-08更新
|
4137次组卷
|
11卷引用:鲁科版(2019)选择性必修1 模块复习备考攻略
鲁科版(2019)选择性必修1 模块复习备考攻略人教版(2019)高二选择性必修第一册 模块复习备考攻略2017年全国普通高等学校招生统一考试化学(江苏卷精编版)(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【教学案】辽宁省实验中学2019-2020学年高二上学期期中考试化学试题北京市2019—2020学年高二上学期期中考试化学试题(选修4人教版)2020届高考化学二轮复习题精准训练——化学反应原理大题专练(直击考点:陌生图像分析)2020届四川省成都市第七中学高三二月份网络教学质量监测卷化学试题湖北省武汉市华中师范大学第一附属中学2020届高三下学期四月份网络教学质量监测理科综合化学试题(已下线)第19讲 水的电离和溶液的酸碱性-2021年高考化学一轮复习名师精讲练江苏省镇江市第一中学2020-2021学年高二下学期4月分阶段测化学试题



