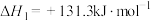名校
解题方法
1 . 水煤气是一种优质燃料和重要的化工原料,其制备方法是将水蒸气与焦炭在高温下混合反应,然后投入固体 进行处理。
进行处理。
I.在温度 下将高温水蒸气通入炽热的焦炭中,其中可能发生的一些反应如下:
下将高温水蒸气通入炽热的焦炭中,其中可能发生的一些反应如下:
(1)已知反应 的焓变
的焓变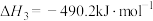 ,近似认为反应焓变不随温度变化,则焦炭的燃烧热
,近似认为反应焓变不随温度变化,则焦炭的燃烧热
______  。
。
(2)在温度 下体系达到化学平衡,将这一时刻记为
下体系达到化学平衡,将这一时刻记为 ,然后将可压缩的恒温反应容器突然压缩至原来体积的一半。将压缩之后这一瞬间的时刻记为
,然后将可压缩的恒温反应容器突然压缩至原来体积的一半。将压缩之后这一瞬间的时刻记为 ,重新达到平衡时的时刻记为
,重新达到平衡时的时刻记为 ,则______(填标号)。
,则______(填标号)。
(3)反应②的平衡常数 很小,若近似忽略生成
很小,若近似忽略生成 的反应,在一个体积固定的恒温容器内投入足量焦炭与一定量的水蒸气,在温度
的反应,在一个体积固定的恒温容器内投入足量焦炭与一定量的水蒸气,在温度 下达到平衡时水蒸气的转化率为
下达到平衡时水蒸气的转化率为 ,下图的三条曲线分别代表了达到平衡时不同的转化率
,下图的三条曲线分别代表了达到平衡时不同的转化率 对应的水蒸气分压、
对应的水蒸气分压、 分压、体系的总压,则代表
分压、体系的总压,则代表 分压的曲线是
分压的曲线是______ (填标号)。欲使平衡转化率为 ,则初始充入水蒸气的压强应为
,则初始充入水蒸气的压强应为______  (结果保留两位有效数字)。
(结果保留两位有效数字)。 ,生成
,生成 。除了以外,钙还有多种氧化物。
。除了以外,钙还有多种氧化物。
(4) 在大约
在大约 的高压条件下还可以进一步与
的高压条件下还可以进一步与 反应得到由
反应得到由 和
和 构成的另一种钙的氧化物
构成的另一种钙的氧化物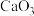 ,预测
,预测 的VSEPR模型名称是
的VSEPR模型名称是______ .
(5)反应生成的 在自然界中会被溶解有
在自然界中会被溶解有 的雨水溶蚀,该过程的离子方程式为
的雨水溶蚀,该过程的离子方程式为______ 。已知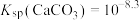 ,碳酸的
,碳酸的 (碳酸浓度以
(碳酸浓度以 形式计算)、
形式计算)、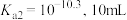 某雨水恰好能够溶解
某雨水恰好能够溶解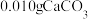 ,此时该雨水中的
,此时该雨水中的 浓度为
浓度为 ,忽略固体溶解产生的体积变化,则此时该雨水的
,忽略固体溶解产生的体积变化,则此时该雨水的 为
为______ 。
 进行处理。
进行处理。I.在温度
 下将高温水蒸气通入炽热的焦炭中,其中可能发生的一些反应如下:
下将高温水蒸气通入炽热的焦炭中,其中可能发生的一些反应如下:反应方程式 | 焓变 | 压强平衡常数 |
① |
|
|
② |
|
|
(1)已知反应
 的焓变
的焓变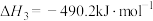 ,近似认为反应焓变不随温度变化,则焦炭的燃烧热
,近似认为反应焓变不随温度变化,则焦炭的燃烧热
 。
。(2)在温度
 下体系达到化学平衡,将这一时刻记为
下体系达到化学平衡,将这一时刻记为 ,然后将可压缩的恒温反应容器突然压缩至原来体积的一半。将压缩之后这一瞬间的时刻记为
,然后将可压缩的恒温反应容器突然压缩至原来体积的一半。将压缩之后这一瞬间的时刻记为 ,重新达到平衡时的时刻记为
,重新达到平衡时的时刻记为 ,则______(填标号)。
,则______(填标号)。A. 时,反应①的正反应速率比 时,反应①的正反应速率比 时增大 时增大 | B. 时,反应②的逆反应速率比 时,反应②的逆反应速率比 时减小 时减小 |
C. 时,反应①的压强平衡常数 时,反应①的压强平衡常数 比 比 时增大 时增大 | D. 时,水蒸气的转化率比 时,水蒸气的转化率比 时减小 时减小 |
(3)反应②的平衡常数
 很小,若近似忽略生成
很小,若近似忽略生成 的反应,在一个体积固定的恒温容器内投入足量焦炭与一定量的水蒸气,在温度
的反应,在一个体积固定的恒温容器内投入足量焦炭与一定量的水蒸气,在温度 下达到平衡时水蒸气的转化率为
下达到平衡时水蒸气的转化率为 ,下图的三条曲线分别代表了达到平衡时不同的转化率
,下图的三条曲线分别代表了达到平衡时不同的转化率 对应的水蒸气分压、
对应的水蒸气分压、 分压、体系的总压,则代表
分压、体系的总压,则代表 分压的曲线是
分压的曲线是 ,则初始充入水蒸气的压强应为
,则初始充入水蒸气的压强应为 (结果保留两位有效数字)。
(结果保留两位有效数字)。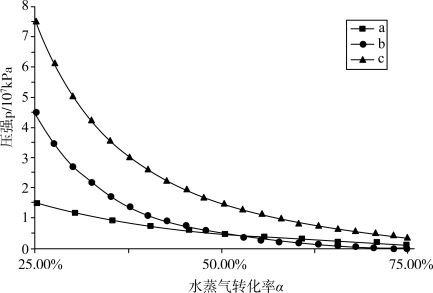
 ,生成
,生成 。除了以外,钙还有多种氧化物。
。除了以外,钙还有多种氧化物。(4)
 在大约
在大约 的高压条件下还可以进一步与
的高压条件下还可以进一步与 反应得到由
反应得到由 和
和 构成的另一种钙的氧化物
构成的另一种钙的氧化物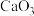 ,预测
,预测 的VSEPR模型名称是
的VSEPR模型名称是(5)反应生成的
 在自然界中会被溶解有
在自然界中会被溶解有 的雨水溶蚀,该过程的离子方程式为
的雨水溶蚀,该过程的离子方程式为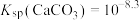 ,碳酸的
,碳酸的 (碳酸浓度以
(碳酸浓度以 形式计算)、
形式计算)、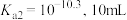 某雨水恰好能够溶解
某雨水恰好能够溶解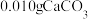 ,此时该雨水中的
,此时该雨水中的 浓度为
浓度为 ,忽略固体溶解产生的体积变化,则此时该雨水的
,忽略固体溶解产生的体积变化,则此时该雨水的 为
为
您最近一年使用:0次
2024-04-21更新
|
405次组卷
|
4卷引用:压轴题13?化学反应原理综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
(已下线)压轴题13?化学反应原理综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)湖南省新高考教学教研联盟2023-2024学年高三下学期第二次联考化学试题河北省重点高中2023-2024学年高三下学期5月高考模拟化学试题(二)福建省福建师范大学附属中学2023-2024学年高三下学期4月末化学综合模拟测试
2024高三下·全国·专题练习
2 . 电镀在工业生产中具有重要作用,某电镀厂生产的废水经预处理后含有 和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
若废水中还含有Cd2+,pH=4时Cd2+的浓度为_______ mol·L-1,用该结果说明Cd2+影响上述流程进行分离的原因是_______ (设H2S平衡浓度为1.0× 10-6mol·L-1。已知:H2S的K1=1.0×10-7,K2=7.0×10-15,Ksp(CdS)=7.0×10-27)
 和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。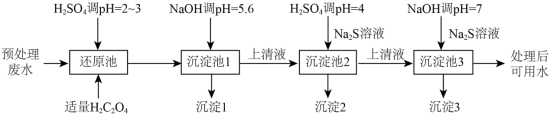
若废水中还含有Cd2+,pH=4时Cd2+的浓度为
您最近一年使用:0次
3 . 甲酸是一种有机化工原料,广泛用于农药、皮革、医药和橡胶等工业。请回答:
(1)活性Fe3O4-x催化反应 ,进而可制得甲酸。该反应的
,进而可制得甲酸。该反应的
_______ 0(填“>”或“<”),理由是_______ 。
(2)某温度下,HCOOH电离平衡常数为 ,当HCOOH平衡浓度为xmol/L时,HCOOH已电离的弱电解质分子数的电离度
,当HCOOH平衡浓度为xmol/L时,HCOOH已电离的弱电解质分子数的电离度
_______ (电离度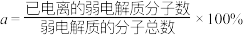 ,用含
,用含 和x的代数式表示,可不化简)。
和x的代数式表示,可不化简)。
(3)某研究小组发现HCOOH水溶液在密封石英管中的分解反应如下:
Ⅰ.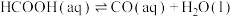
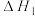
Ⅱ.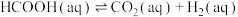
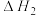
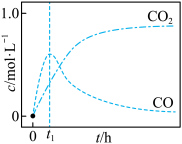
研究发现,在反应Ⅰ、Ⅱ中,H+仅对反应Ⅰ有催化加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。T℃下,在密封石英管内完全充满1.0mol/LHCOOH水溶液,分解产物均完全溶于水中。CO2、CO浓度与反应时间的变化关系如图所示。_______ 。
A.反应Ⅰ活化能小于反应Ⅱ
B.反应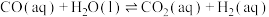
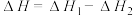
C.混合体系达平衡后: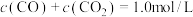
D.若在起始溶液中加入盐酸,则CO达浓度峰值时,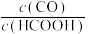 的值与未加盐酸时相同
的值与未加盐酸时相同
②保持其它条件不变,若反应起始时溶液中同时还含有0.10mol/L盐酸,请在上图中画出CO的浓度与反应时间的变化关系图_______ 。
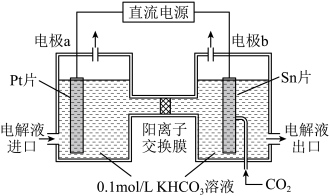
(4)一种由CO2电化学法合成甲酸盐的工作原理如图所示。电极b为_______ 极。电解一段时间后,若两侧电解液中K+的物质的量相差0.08mol,则阳极产生的气体在标准状况下的总体积为_______ L(假设产生的气体全部逸出)。
(1)活性Fe3O4-x催化反应
 ,进而可制得甲酸。该反应的
,进而可制得甲酸。该反应的
(2)某温度下,HCOOH电离平衡常数为
 ,当HCOOH平衡浓度为xmol/L时,HCOOH已电离的弱电解质分子数的电离度
,当HCOOH平衡浓度为xmol/L时,HCOOH已电离的弱电解质分子数的电离度
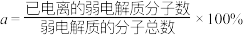 ,用含
,用含 和x的代数式表示,可不化简)。
和x的代数式表示,可不化简)。(3)某研究小组发现HCOOH水溶液在密封石英管中的分解反应如下:
Ⅰ.
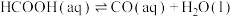
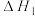
Ⅱ.
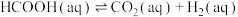
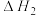
研究发现,在反应Ⅰ、Ⅱ中,H+仅对反应Ⅰ有催化加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。T℃下,在密封石英管内完全充满1.0mol/LHCOOH水溶液,分解产物均完全溶于水中。CO2、CO浓度与反应时间的变化关系如图所示。
A.反应Ⅰ活化能小于反应Ⅱ
B.反应
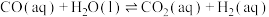
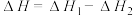
C.混合体系达平衡后:
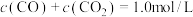
D.若在起始溶液中加入盐酸,则CO达浓度峰值时,
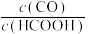 的值与未加盐酸时相同
的值与未加盐酸时相同②保持其它条件不变,若反应起始时溶液中同时还含有0.10mol/L盐酸,请在上图中画出CO的浓度与反应时间的变化关系图
(4)一种由CO2电化学法合成甲酸盐的工作原理如图所示。电极b为
您最近一年使用:0次
4 . Ⅰ.柠檬酸是一种重要的工业原料,化学式可表示为H3Cit,属于三元弱酸。25℃时,柠檬酸的电离常数如下:Ka1=7.4×10-4、Ka2=1.7×10-5、Ka3=4.0×10-7。
(1)25℃时,不同pH范围内,H3Cit、H2Cit-、HCit2-和Cit3-所占的比例(该微粒浓度与四种微粒浓度之和的比值)如下图所示,则其中代表HCit2-的是___________。
(2)25℃时,0.1 mol∙L-1下列溶液中微粒的浓度关系正确的是___________。
(3)已知25℃时,碳酸的电离常数为:Ka1=4.4×10-7、Ka2=4.7×10-11,向NaHCO3溶液中加入NaH2Cit溶液,请写出反应的化学方程式___________ 。
Ⅱ.电子元器件经处理后可得贵金属溶液。在适宜条件下,柠檬酸亚铁中的Fe2+可将贵金属溶液中的AuCl 还原为金颗粒沉淀。
还原为金颗粒沉淀。
(4)请写出离子反应方程式,并标出电子转移的方向和数目。___________ 。
Ⅲ.柠檬酸亚铁是一种高效补铁剂。利用硫铁矿烧渣(主要含Fe2O3及少量CaO、Al2O3)制备柠檬酸亚铁的工艺流程如图。
(5)基态Fe原子价电子排布式为___________ 。
(6)滤渣1为___________ 。(填化学式)
(7)“沉铝”过程中,为了使铝充分沉淀的同时减少铁的损失,需要精确控制氨水的加入量。已知溶液中[Al3+]≤10-5 mol•L-1,认为已经沉淀完全。请计算:(计算结果保留2位有效数字),Al3+恰好沉淀完全时,溶液中[OH-] =___________ 。
(8)“沉铁”过程需控制温度在35℃以下,可能原因是___________ 。
(9)“合成”过程中,需加入少量的抗氧化剂,下列试剂合适的是___________。
(1)25℃时,不同pH范围内,H3Cit、H2Cit-、HCit2-和Cit3-所占的比例(该微粒浓度与四种微粒浓度之和的比值)如下图所示,则其中代表HCit2-的是___________。
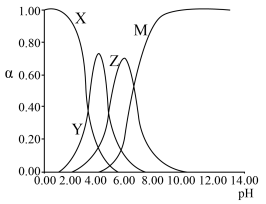
| A.X | B.Y | C.Z | D.M |
(2)25℃时,0.1 mol∙L-1下列溶液中微粒的浓度关系正确的是___________。
| A.Na3Cit溶液中,[Na+]+[H+]=[OH-]+ [H2Cit-]+[HCit2-]+ [Cit3-] |
| B.Na3Cit溶液中, [OH-]>[H+] |
| C.NaH2Cit溶液中,[Na+]=[H3Cit]+[H2Cit-]+[HCit2-]+ [Cit3-] |
| D.Na2HCit溶液中,[OH-]>[H+] |
(3)已知25℃时,碳酸的电离常数为:Ka1=4.4×10-7、Ka2=4.7×10-11,向NaHCO3溶液中加入NaH2Cit溶液,请写出反应的化学方程式
Ⅱ.电子元器件经处理后可得贵金属溶液。在适宜条件下,柠檬酸亚铁中的Fe2+可将贵金属溶液中的AuCl
 还原为金颗粒沉淀。
还原为金颗粒沉淀。(4)请写出离子反应方程式,并标出电子转移的方向和数目。
Ⅲ.柠檬酸亚铁是一种高效补铁剂。利用硫铁矿烧渣(主要含Fe2O3及少量CaO、Al2O3)制备柠檬酸亚铁的工艺流程如图。

(5)基态Fe原子价电子排布式为
(6)滤渣1为
(7)“沉铝”过程中,为了使铝充分沉淀的同时减少铁的损失,需要精确控制氨水的加入量。已知溶液中[Al3+]≤10-5 mol•L-1,认为已经沉淀完全。请计算:(计算结果保留2位有效数字),Al3+恰好沉淀完全时,溶液中[OH-] =
(8)“沉铁”过程需控制温度在35℃以下,可能原因是
(9)“合成”过程中,需加入少量的抗氧化剂,下列试剂合适的是___________。
| A.FeSO4 | B.Fe | C.Cu | D.H2O2 |
您最近一年使用:0次
名校
解题方法
5 . 已知 时,部分电解质的电离常数如下表所示:
时,部分电解质的电离常数如下表所示:
(1)根据在 时,用蒸馏水稀释
时,用蒸馏水稀释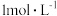 的醋酸溶液至
的醋酸溶液至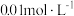 ,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)
,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)
(2)常温下,同浓度的下列物质的水溶液 最小的是_____。(单选)
最小的是_____。(单选)
(3)常温下,下列操作(忽略过程中温度变化)可以使亚硫酸稀溶液中的 增大的是_____。(单选)
增大的是_____。(单选)
(4)下列关于 溶液中微粒关系错误的是_____。(不定项)
溶液中微粒关系错误的是_____。(不定项)
(5)向 溶液中通入少量
溶液中通入少量 ,写出反应的离子方程式
,写出反应的离子方程式_____ 。
(6)含镉 废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下,
废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下, 、
、 。若用
。若用 处理
处理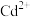 实现沉淀转化,写出反应的离子方程式:
实现沉淀转化,写出反应的离子方程式:_____ ,此时该反应的化学平衡常数为_____ 。
 时,部分电解质的电离常数如下表所示:
时,部分电解质的电离常数如下表所示:| 电解质 |  | 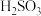 |
| 电离常数 | 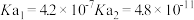 | 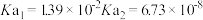 |
| 电解质 | 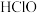 |  |
| 电离常数 |  | 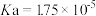 |
 时,用蒸馏水稀释
时,用蒸馏水稀释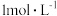 的醋酸溶液至
的醋酸溶液至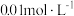 ,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)
,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)A. | B.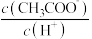 |
C.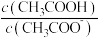 | D. |
 最小的是_____。(单选)
最小的是_____。(单选)A.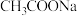 | B. | C. | D. |
 增大的是_____。(单选)
增大的是_____。(单选)A.通入 气体 气体 | B.通入 气体 气体 | C.加入 固体 固体 | D.加入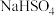 固体 固体 |
 溶液中微粒关系错误的是_____。(不定项)
溶液中微粒关系错误的是_____。(不定项)A.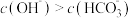 |
B.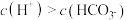 |
C. |
D.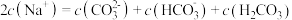 |
 溶液中通入少量
溶液中通入少量 ,写出反应的离子方程式
,写出反应的离子方程式(6)含镉
 废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下,
废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下, 、
、 。若用
。若用 处理
处理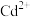 实现沉淀转化,写出反应的离子方程式:
实现沉淀转化,写出反应的离子方程式:
您最近一年使用:0次
名校
解题方法
6 . 活性炭载钯(Pd/C)催化剂被广泛应用于医药和化工行业,某废钯催化剂(钯碳)的杂质主要含炭、有机物及少量Fe、Zn等。如图是利用钯碳制备氧化钯( )和Pd的流程。
)和Pd的流程。______ (填仪器名称)中模拟“焚烧”过程。 为二元弱碱,常温下
为二元弱碱,常温下 的电离常数
的电离常数 、
、 ,则常温下0.1mol/L
,则常温下0.1mol/L  水溶液pH=
水溶液pH=______ 。
(2)“溶浸”步骤中钯与王水发生反应生成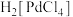 和一种有毒的无色气体A,A为
和一种有毒的无色气体A,A为______ (填化学式),钯的浸出率与反应的时间、温度的关系如图所示,则最佳的浸取时间和温度为______ ,写出“除锌铁”步骤中钯的化合物与试剂Ⅰ反应的化学方程式______ 。______ (填名称),加入该试剂的目的是______ 。
(4)海绵钯具有优良的储氢功能。假设海绵钯的密度为 ,其吸附的氢气是其体积的n倍(标准状况),则此条件下,氢气的浓度
,其吸附的氢气是其体积的n倍(标准状况),则此条件下,氢气的浓度
______ mol(氢气的浓度r为1mol Pd吸附氢气的物质的量,用含 、n的分数式表示)。
、n的分数式表示)。
 )和Pd的流程。
)和Pd的流程。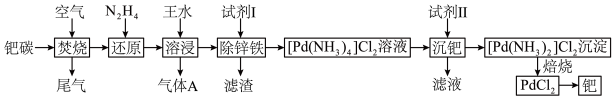
 为二元弱碱,常温下
为二元弱碱,常温下 的电离常数
的电离常数 、
、 ,则常温下0.1mol/L
,则常温下0.1mol/L  水溶液pH=
水溶液pH=(2)“溶浸”步骤中钯与王水发生反应生成
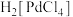 和一种有毒的无色气体A,A为
和一种有毒的无色气体A,A为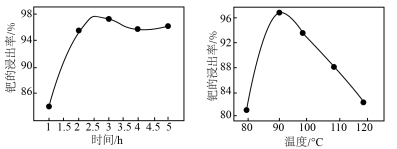
(4)海绵钯具有优良的储氢功能。假设海绵钯的密度为
 ,其吸附的氢气是其体积的n倍(标准状况),则此条件下,氢气的浓度
,其吸附的氢气是其体积的n倍(标准状况),则此条件下,氢气的浓度
 、n的分数式表示)。
、n的分数式表示)。
您最近一年使用:0次
2024-03-15更新
|
503次组卷
|
4卷引用:山东省聊城市2024年高考模拟试题(一) 化学
山东省聊城市2024年高考模拟试题(一) 化学山东省聊城市2023-2024学年高三下学期一模化学试题 (已下线)化学(山东卷02)-2024年高考押题预测卷2024届四川省绵阳南山中学高三下学期高考仿真演练(一) 理科综合试题-高中化学
解题方法
7 . 二氧化碳的捕集和资源化利用是缓解温室效应的重要战略方向。回答下列问题:
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。总反应可表示为:

该反应一般认为通过如下步骤来实现:
①

②

(1)若反应①为慢反应,请在图中接着完善画出反应②的能量变化曲线,标注出相应的物质(含聚集状态)以及总反应的 (含具体数值)
(含具体数值) _______ 。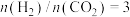 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为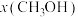 ,在
,在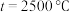 下的
下的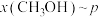 、在
、在 下的
下的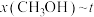 如图所示。
如图所示。_______ (填“a”或“b”),判断的理由_______ 。
(b)当 时,
时, 的平衡转化率
的平衡转化率
_______ 。
Ⅱ.催化CO2加氢合成乙酸在减少碳排放的同时还可以生产重要的化工原料。弱电解质的电离度是指弱电解质在溶液中达到电离平衡时,已电离的电解质分子数占原来总分子数(包括已电离的和未电离的>的百分数,用a表示。而在实验测定中,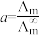 ,
,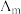 为一定浓度下电解质的摩尔电导率,
为一定浓度下电解质的摩尔电导率,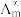 为无限稀释时溶液的摩尔电导率,
为无限稀释时溶液的摩尔电导率,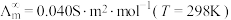 。某小组实验测得
。某小组实验测得 时,
时, 乙酸的
乙酸的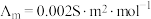 。
。
(3)在298K时,乙酸的电离平衡常数
_______ (列出计算式,不需化简)。
(4)在298K时,几种离子的摩尔电导率如下表所示。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择,最适宜的电解质为_______ (填化学式)。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。总反应可表示为:


该反应一般认为通过如下步骤来实现:
①


②


(1)若反应①为慢反应,请在图中接着完善画出反应②的能量变化曲线,标注出相应的物质(含聚集状态)以及总反应的
 (含具体数值)
(含具体数值) 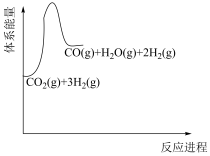
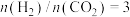 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为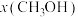 ,在
,在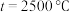 下的
下的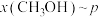 、在
、在 下的
下的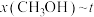 如图所示。
如图所示。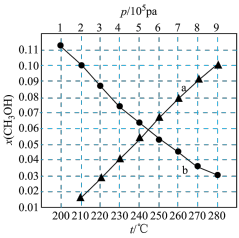
(b)当
 时,
时, 的平衡转化率
的平衡转化率
Ⅱ.催化CO2加氢合成乙酸在减少碳排放的同时还可以生产重要的化工原料。弱电解质的电离度是指弱电解质在溶液中达到电离平衡时,已电离的电解质分子数占原来总分子数(包括已电离的和未电离的>的百分数,用a表示。而在实验测定中,
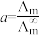 ,
,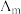 为一定浓度下电解质的摩尔电导率,
为一定浓度下电解质的摩尔电导率,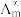 为无限稀释时溶液的摩尔电导率,
为无限稀释时溶液的摩尔电导率,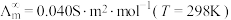 。某小组实验测得
。某小组实验测得 时,
时, 乙酸的
乙酸的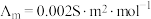 。
。(3)在298K时,乙酸的电离平衡常数

(4)在298K时,几种离子的摩尔电导率如下表所示。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择,最适宜的电解质为
| 离子种类 |  |  |  |  |  |  |
摩尔电导率/( ) ) | 349.82 | 79.80 | 76.34 | 50.18 | 73.52 | 50.11 |
您最近一年使用:0次
8 . 联氨(N2H4)又称“肼”,具高吸湿性、沸点386.5K、毒性强、还原性强等特性,燃烧释放出大量的热,常用于做火箭的燃料以及分析试剂中的还原剂。
I.联氨的制备
(1)联氨可用次氯酸钠溶液氧化过量的氨气制得,写出此反应得离子方程式___________ ;此反应中,被氧化的元素是_____ 。每生成1mol肼,转移的电子数为________ 。
Ⅱ .联氨的结构
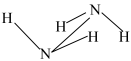
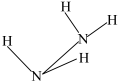
(2)联氨具强极性,推测下列结构最接近联氨分子真实结构的是________ 。
Ⅲ .联氨的性质
(3)①一定条件下, 联氨与二氯化钴(CoCl2)溶液能形成配位化合物Co(N2H4)6Cl2,关于此配位化合物的下列说法中不正确的是_____ 。
A.中心离子是Co2+ B.配位数是8
C.配位原子是N原子 D.向此配合物的溶液中滴入硝酸银,会产生白色沉淀
②联氨具高吸湿性,原因是_____ 。
③联氨水溶液与氨水类性质相似,将联氨溶于一定浓度的稀硫酸中,除形成N2H6SO4外,还可以生成的盐是_____ (填写化学式)。实验发现0.1mol·L-1N2H6SO4溶液显酸性,原因是_____ (用离子方程式表示),溶液中各种含氮微粒存在关系c(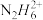 )+c(N2H6OH+)
)+c(N2H6OH+)____ 0.1-c(N2H4·2H2O)(选填“>”,“<”或“=”)。
(4)1mol液态联氨在空气中完全燃烧生成氮气和水蒸气放出621.74KJ的热量,此反应的热化学方程式是_______ 。肼有剧毒,但目前仍被普遍用作火箭的燃料,原因是________ 。
(5)联氨在一定条件下被亚硝酸氧化为叠氮酸(HN3),室温下亚硝酸、叠氮酸的电离平衡常数如表所示:
室温下,则同浓度的HNO2和HN3,其pH值:HNO2____ HN3(选填“>”、“<”或“=”),  反应性能类似卤素离子,则难溶物AgN3的Ksp表达式为
反应性能类似卤素离子,则难溶物AgN3的Ksp表达式为_________ 。
(6)某研究小组研究联氨和双氧水反应,查阅相关键能数据
并已知1molN2H4(l)→N2H4(g)与2molH2O2(l)→H2O2(g)共吸热23.76kJ,据此估算化学反应N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)的焓变ΔH=_______ kJ·mol-1,反应的熵变ΔS _____ 0(选填“>”、“<”)。研究小组利用此反应设计出如下电池,负极电极反应式:N2H4+4OH-−4e-=N2+4H2O。则正极电极反应式:________ 。
I.联氨的制备
(1)联氨可用次氯酸钠溶液氧化过量的氨气制得,写出此反应得离子方程式
Ⅱ .联氨的结构
(2)联氨具强极性,推测下列结构最接近联氨分子真实结构的是
|
|
| A. 反式结构 | B. 顺式结构 |
Ⅲ .联氨的性质
(3)①一定条件下, 联氨与二氯化钴(CoCl2)溶液能形成配位化合物Co(N2H4)6Cl2,关于此配位化合物的下列说法中不正确的是
A.中心离子是Co2+ B.配位数是8
C.配位原子是N原子 D.向此配合物的溶液中滴入硝酸银,会产生白色沉淀
②联氨具高吸湿性,原因是
③联氨水溶液与氨水类性质相似,将联氨溶于一定浓度的稀硫酸中,除形成N2H6SO4外,还可以生成的盐是
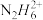 )+c(N2H6OH+)
)+c(N2H6OH+)(4)1mol液态联氨在空气中完全燃烧生成氮气和水蒸气放出621.74KJ的热量,此反应的热化学方程式是
(5)联氨在一定条件下被亚硝酸氧化为叠氮酸(HN3),室温下亚硝酸、叠氮酸的电离平衡常数如表所示:
| 酸名 | 亚硝酸(HNO2) | 叠氮酸(HN3) |
| 电离平衡常数 | 5.1 x 10-4 | 1.8 x 10-5 |
 反应性能类似卤素离子,则难溶物AgN3的Ksp表达式为
反应性能类似卤素离子,则难溶物AgN3的Ksp表达式为(6)某研究小组研究联氨和双氧水反应,查阅相关键能数据
| 化学键 | N-H | O-H | O-O | N-N | N≡N |
| 键能(kJ·mol-1) | 391 | 467 | 138 | 159 | 945 |
您最近一年使用:0次
名校
9 . 研究海洋中珊瑚礁(主要成分CaCO3)的形成机制及其影响具有重要意义,相关主要反应有:
反应Ⅰ:CO2(aq)+H2O(l)
 (aq)+H+(aq) K1=4.5×10-7
(aq)+H+(aq) K1=4.5×10-7
反应Ⅱ: (aq)
(aq)
 (aq)+H+(aq) K2= 4.7×10-11
(aq)+H+(aq) K2= 4.7×10-11
反应Ⅲ:CaCO3(s) Ca2+(aq)+
Ca2+(aq)+ (aq) K3=3.4×10-9
(aq) K3=3.4×10-9
请回答:
(1)珊瑚礁形成的总反应可表示为Ca2+(aq)+2 (aq)=CaCO3(s)+CO2(aq)+H2O(l)。有利于珊瑚礁形成的环境是
(aq)=CaCO3(s)+CO2(aq)+H2O(l)。有利于珊瑚礁形成的环境是_______ (填“温暖海域”或“冰冷海域”),该反应的平衡常数K=_______ (用K1、K2、K3表示)。
(2)海水的pH为8.0~8.3,下列有关珊瑚礁形成过程的叙述中正确的是_______。
(3)温室气体CO2的浓度上升,会导致海水酸化,促使珊瑚礁的溶解。科学家模拟海洋环境探究不同温度下海水中CO2浓度与 浓度间的关系。已知T1℃下测得c(CO2)与c(
浓度间的关系。已知T1℃下测得c(CO2)与c( )的关系如图,请画出T2℃(T2>T1)时c(
)的关系如图,请画出T2℃(T2>T1)时c( )随c(CO2)的变化趋势
)随c(CO2)的变化趋势_______ 。_______ 0(填“>”“<”或“=”);随温度的升高,容器中CO2的浓度在T3温度下出现最低值的原因是_______ 。
反应Ⅰ:CO2(aq)+H2O(l)

 (aq)+H+(aq) K1=4.5×10-7
(aq)+H+(aq) K1=4.5×10-7反应Ⅱ:
 (aq)
(aq)
 (aq)+H+(aq) K2= 4.7×10-11
(aq)+H+(aq) K2= 4.7×10-11反应Ⅲ:CaCO3(s)
 Ca2+(aq)+
Ca2+(aq)+ (aq) K3=3.4×10-9
(aq) K3=3.4×10-9请回答:
(1)珊瑚礁形成的总反应可表示为Ca2+(aq)+2
 (aq)=CaCO3(s)+CO2(aq)+H2O(l)。有利于珊瑚礁形成的环境是
(aq)=CaCO3(s)+CO2(aq)+H2O(l)。有利于珊瑚礁形成的环境是(2)海水的pH为8.0~8.3,下列有关珊瑚礁形成过程的叙述中正确的是_______。
A.海水中最主要的含碳微粒为 |
B.海水中的c(Ca2+)>c( )+c( )+c( ) ) |
C. 、 、 的水解反应是海水呈弱碱性的主要原因 的水解反应是海水呈弱碱性的主要原因 |
D.珊瑚礁形成的反应阻碍了 的电离 的电离 |
(3)温室气体CO2的浓度上升,会导致海水酸化,促使珊瑚礁的溶解。科学家模拟海洋环境探究不同温度下海水中CO2浓度与
 浓度间的关系。已知T1℃下测得c(CO2)与c(
浓度间的关系。已知T1℃下测得c(CO2)与c( )的关系如图,请画出T2℃(T2>T1)时c(
)的关系如图,请画出T2℃(T2>T1)时c( )随c(CO2)的变化趋势
)随c(CO2)的变化趋势

您最近一年使用:0次
10 . 回答下列问题
(1)99℃时, ,该温度下测得
,该温度下测得
 溶液的
溶液的 。
。 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ 。
(2)常温下, 为二元弱酸,
为二元弱酸,
 溶液的
溶液的 ,则该溶液中下列微粒的浓度
,则该溶液中下列微粒的浓度
① ②
② ③
③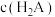 ④
④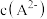 ⑤
⑤ 由大到小的顺序为
由大到小的顺序为___________ (填序号)。
(3)①25℃时,向1L0.1mol/LCH3COOH溶液中加入0.1molCH3COONa固体,则醋酸的电离平衡向___________ (填“正”或“逆”)反应方向移动:水的电离程度将___________ (填“增大”、“减小”或“不变”)。
②25℃时,CH3COOH的电离平衡常数Ka=1.75×10-5,则CH3COONa水解常数Kh=___________ (保留三位有效数字)。改变下列条件,能使CH3COONa稀溶液中 增大的是
增大的是___________ 。
a.降温 b.加入 固体 c.稀释 d.加入
固体 c.稀释 d.加入 固体
固体
(4)在剧烈运动中,因缺氧肌肉会产生乳酸(HL),而血液中,乳酸与碳酸氢盐发生复分解反应。已知乳酸(HL)是一元酸,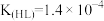 。碳酸的电离平衡常数为:
。碳酸的电离平衡常数为: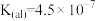 ,
,
① 乳酸的
乳酸的 为
为___________ (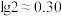 ,
,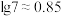 )
)
②乳酸和碳酸氢盐反应的平衡常数的数值___________ 。
(1)99℃时,
 ,该温度下测得
,该温度下测得
 溶液的
溶液的 。
。 在水溶液中的电离方程式为
在水溶液中的电离方程式为(2)常温下,
 为二元弱酸,
为二元弱酸,
 溶液的
溶液的 ,则该溶液中下列微粒的浓度
,则该溶液中下列微粒的浓度①
 ②
② ③
③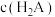 ④
④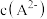 ⑤
⑤ 由大到小的顺序为
由大到小的顺序为(3)①25℃时,向1L0.1mol/LCH3COOH溶液中加入0.1molCH3COONa固体,则醋酸的电离平衡向
②25℃时,CH3COOH的电离平衡常数Ka=1.75×10-5,则CH3COONa水解常数Kh=
 增大的是
增大的是a.降温 b.加入
 固体 c.稀释 d.加入
固体 c.稀释 d.加入 固体
固体(4)在剧烈运动中,因缺氧肌肉会产生乳酸(HL),而血液中,乳酸与碳酸氢盐发生复分解反应。已知乳酸(HL)是一元酸,
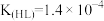 。碳酸的电离平衡常数为:
。碳酸的电离平衡常数为: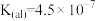 ,
,
①
 乳酸的
乳酸的 为
为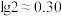 ,
,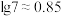 )
)②乳酸和碳酸氢盐反应的平衡常数的数值
您最近一年使用:0次