名校
解题方法
1 . 一种制备 的工艺路线如图所示,反应
的工艺路线如图所示,反应 所得溶液pH在3~4之间,反应
所得溶液pH在3~4之间,反应 需及时补加
需及时补加 以保持反应在
以保持反应在 条件下进行。常温下,
条件下进行。常温下, 的电离平衡常数
的电离平衡常数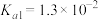 ,
,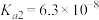 。下列说法正确的是
。下列说法正确的是
 的工艺路线如图所示,反应
的工艺路线如图所示,反应 所得溶液pH在3~4之间,反应
所得溶液pH在3~4之间,反应 需及时补加
需及时补加 以保持反应在
以保持反应在 条件下进行。常温下,
条件下进行。常温下, 的电离平衡常数
的电离平衡常数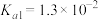 ,
,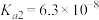 。下列说法正确的是
。下列说法正确的是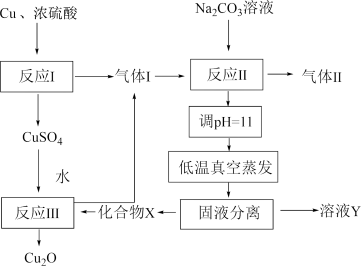
A.反应 、 、 、 、 均为氧化还原反应 均为氧化还原反应 |
B.低温真空蒸发主要目的是防止 被氧化 被氧化 |
C.溶液Y可循环用于反应 所在操作单元吸收气体 所在操作单元吸收气体 |
D.若 产量不变,参与反应 产量不变,参与反应 的X与 的X与 物质的量之比 物质的量之比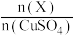 增大时,需补加 增大时,需补加 的量增多 的量增多 |
您最近一年使用:0次
昨日更新
|
65次组卷
|
3卷引用:福建省福州第三中学2023-2024学年高三上学期第五次质量检测化学试题
解题方法
2 . 全球大气 浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
(1)已知25℃时,大气中的 溶于水存在以下过程:
溶于水存在以下过程:
①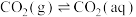

②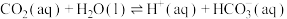

过程①的混合平衡常数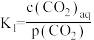 ,其中
,其中 表示溶液中的
表示溶液中的 浓度,
浓度,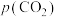 表示大气中
表示大气中 的分压(单位:kPa)。温度升高,
的分压(单位:kPa)。温度升高,
_______ (填“增大”或“减小”);当大气压强为akPa,溶液中的 (忽略
(忽略 和水的电离)时,大气中
和水的电离)时,大气中 的体积分数为
的体积分数为_______ 。
(2)由 转化制甲醇具有重要的经济效益。反应
转化制甲醇具有重要的经济效益。反应 。在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
。在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。_______ ,有催化剂时决速步骤的活化能为_______ eV。
(3) 催化加氢制甲醇反应历程中某一步基元反应的Arthenius经验公式的实验数据如图所示,已知Arthenius经验公式为
催化加氢制甲醇反应历程中某一步基元反应的Arthenius经验公式的实验数据如图所示,已知Arthenius经验公式为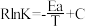 (其中Ea为活化能,K为速率常数,R和C为常数)。
(其中Ea为活化能,K为速率常数,R和C为常数)。
①该反应的活化能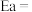
_______ kJ/mol;
②当使用更高效的催化剂时,在图中画出Rlnk与 关系的示意图
关系的示意图_______ 。 催化加氢制甲醇过程中也存在竞争反应
催化加氢制甲醇过程中也存在竞争反应
 ,在恒温密闭容器中,维持压强和投料比不变,将
,在恒温密闭容器中,维持压强和投料比不变,将 和
和 按一定流速通过反应器,
按一定流速通过反应器, 转化率和甲醇选择性
转化率和甲醇选择性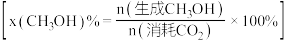 随温度变化关系如下图所示:
随温度变化关系如下图所示:_______ 。
②在压强为P的恒温恒压密闭容器中,加入 和
和 反应并达到平衡状态
反应并达到平衡状态 平衡转化率为20%,甲醇的选择性为50%,计算
平衡转化率为20%,甲醇的选择性为50%,计算 ,在该温度下的平衡常数
,在该温度下的平衡常数
_______ (列出计算式)。
 浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:(1)已知25℃时,大气中的
 溶于水存在以下过程:
溶于水存在以下过程:①
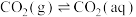

②
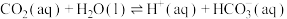

过程①的混合平衡常数
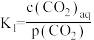 ,其中
,其中 表示溶液中的
表示溶液中的 浓度,
浓度,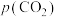 表示大气中
表示大气中 的分压(单位:kPa)。温度升高,
的分压(单位:kPa)。温度升高,
 (忽略
(忽略 和水的电离)时,大气中
和水的电离)时,大气中 的体积分数为
的体积分数为(2)由
 转化制甲醇具有重要的经济效益。反应
转化制甲醇具有重要的经济效益。反应 。在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
。在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。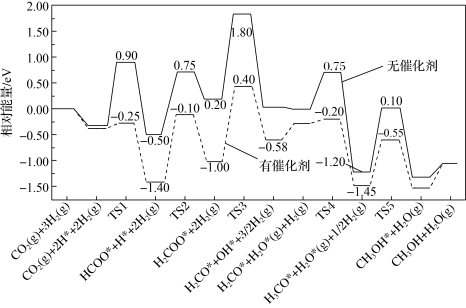
(3)
 催化加氢制甲醇反应历程中某一步基元反应的Arthenius经验公式的实验数据如图所示,已知Arthenius经验公式为
催化加氢制甲醇反应历程中某一步基元反应的Arthenius经验公式的实验数据如图所示,已知Arthenius经验公式为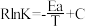 (其中Ea为活化能,K为速率常数,R和C为常数)。
(其中Ea为活化能,K为速率常数,R和C为常数)。①该反应的活化能
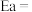
②当使用更高效的催化剂时,在图中画出Rlnk与
 关系的示意图
关系的示意图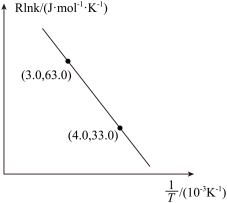
 催化加氢制甲醇过程中也存在竞争反应
催化加氢制甲醇过程中也存在竞争反应
 ,在恒温密闭容器中,维持压强和投料比不变,将
,在恒温密闭容器中,维持压强和投料比不变,将 和
和 按一定流速通过反应器,
按一定流速通过反应器, 转化率和甲醇选择性
转化率和甲醇选择性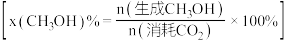 随温度变化关系如下图所示:
随温度变化关系如下图所示: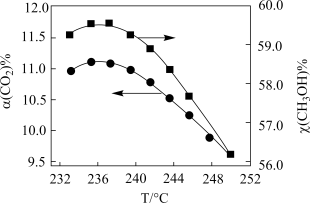
②在压强为P的恒温恒压密闭容器中,加入
 和
和 反应并达到平衡状态
反应并达到平衡状态 平衡转化率为20%,甲醇的选择性为50%,计算
平衡转化率为20%,甲醇的选择性为50%,计算 ,在该温度下的平衡常数
,在该温度下的平衡常数
您最近一年使用:0次
3 . 在菠菜等植物中含有丰富的草酸,草酸对生命活动有重要影响。
 溶液的pH,溶液中的
溶液的pH,溶液中的 、
、 、
、 的物质的量分数
的物质的量分数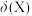 随pH的变化如图所示:
随pH的变化如图所示: )在水中的电离方程式:
)在水中的电离方程式:___________ 。
(2)要使溶液中草酸的电离程度增大,采取的措施为___________ 。(写两点)
(3)草酸溶液中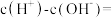
___________ 。(用含碳微粒表示)
(4)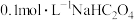 溶液中
溶液中
___________  。(填“<”“>”“=”)
。(填“<”“>”“=”)
(5) 时,
时,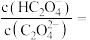
___________ 。

 溶液的pH,溶液中的
溶液的pH,溶液中的 、
、 、
、 的物质的量分数
的物质的量分数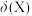 随pH的变化如图所示:
随pH的变化如图所示: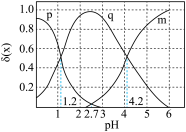
 )在水中的电离方程式:
)在水中的电离方程式:(2)要使溶液中草酸的电离程度增大,采取的措施为
(3)草酸溶液中
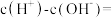
(4)
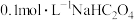 溶液中
溶液中
 。(填“<”“>”“=”)
。(填“<”“>”“=”)(5)
 时,
时,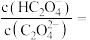
您最近一年使用:0次
4 . 25℃时,几种酸的电离平衡常数如下表所示:
| 酸 | CH3COOH | HCN | H2CO3 | HNO2 |
 | 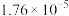 |  | 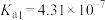  |  |
A.反应 能够发生 能够发生 |
| B.等物质的量的CH3COOH和CH3COONa的混合溶液呈碱性 |
C.CO2通入NaCN溶液中,反应的离子方程式为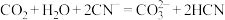 |
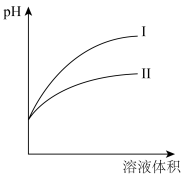
| D.常温下,等pH的醋酸和盐酸分别加等体积水稀释(如上图),I表示盐酸的稀释过程 |
您最近一年使用:0次
名校
解题方法
5 . 常温下,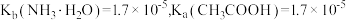 ,向20mL浓度均为
,向20mL浓度均为 的盐酸和醋酸的混合溶液中逐滴加入
的盐酸和醋酸的混合溶液中逐滴加入 的氨水,测得过程中电导率和pH变化曲线如图所示。
的氨水,测得过程中电导率和pH变化曲线如图所示。
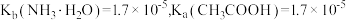 ,向20mL浓度均为
,向20mL浓度均为 的盐酸和醋酸的混合溶液中逐滴加入
的盐酸和醋酸的混合溶液中逐滴加入 的氨水,测得过程中电导率和pH变化曲线如图所示。
的氨水,测得过程中电导率和pH变化曲线如图所示。
| A.a点溶液中,c(CH3COO-)数量级为10-5 |
B.b点溶液中,存在c(Cl-)>c(NH )>c(CH3COOH)>c(H+)>c(OH-) )>c(CH3COOH)>c(H+)>c(OH-) |
C.c点溶液中,存在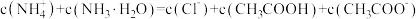 |
D.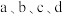 点溶液中,d点水的电离程度最大 点溶液中,d点水的电离程度最大 |
您最近一年使用:0次
2024-03-17更新
|
348次组卷
|
6卷引用:湖南省醴陵市第一中学2023届高三第六次月考化学试题
湖南省醴陵市第一中学2023届高三第六次月考化学试题湖南省涟源市第一中学2023届高三第六次月考化学试题河南省洛阳市新安县第一高级中学2023届高三下学期入学检测化学试题(已下线)素养卷05 电解质溶液中微粒变化图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)辽宁省实验中学2024届高三高考适应性测试(二)化学试题安徽省六安第一中学2024届高三下学期质量检测化学试卷(四)
6 . 硼及其化合物在制造、化工等领域都有广泛应用,回答下列问题:
(1)基态硼原子的价电子排布图为__________ ,其占据最高能级电子的电子云轮廓图形状为__________ ,基态硼原子比基态氮原子的第一电离能 小,其原因为
小,其原因为__________ 。
(2) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得:
反应制得:
① 由
由 和
和 构成,
构成, 的空间结构为
的空间结构为__________ 。
② 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为__________ 。
③ 的键角为
的键角为__________ 。
(3)写出B与 溶液反应的离子方程式:
溶液反应的离子方程式:__________ 。
(4) 为一元弱酸[常温下,
为一元弱酸[常温下,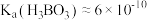 ]:
]:
① 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为__________ 。
②常温下, 的硼酸的pH约为
的硼酸的pH约为__________ (已知: ,
, )。
)。
(1)基态硼原子的价电子排布图为
 小,其原因为
小,其原因为(2)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得:
反应制得:①
 由
由 和
和 构成,
构成, 的空间结构为
的空间结构为②
 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为③
 的键角为
的键角为(3)写出B与
 溶液反应的离子方程式:
溶液反应的离子方程式:(4)
 为一元弱酸[常温下,
为一元弱酸[常温下,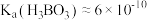 ]:
]:①
 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为②常温下,
 的硼酸的pH约为
的硼酸的pH约为 ,
, )。
)。
您最近一年使用:0次
2024-03-07更新
|
128次组卷
|
2卷引用:河北省邢台市四校联盟2023-2024学年高二上学期11月月考化学试题
7 .  时,用
时,用 的
的 溶液、
溶液、 的盐酸分别滴定
的盐酸分别滴定 溶液、
溶液、 溶液,滴定曲线如图所示.下列说法正确的是
溶液,滴定曲线如图所示.下列说法正确的是
 时,用
时,用 的
的 溶液、
溶液、 的盐酸分别滴定
的盐酸分别滴定 溶液、
溶液、 溶液,滴定曲线如图所示.下列说法正确的是
溶液,滴定曲线如图所示.下列说法正确的是
A. 为强酸, 为强酸, 为弱碱 为弱碱 |
B.曲线Ⅰ:滴加 溶液时有 溶液时有 |
| C.交点p是两种滴定反应中的恰好完全反应点 |
D.曲线Ⅱ:滴加溶液过程中始终存在 |
您最近一年使用:0次
名校
解题方法
8 . 室温下,通过下列实验探究亚硫酸盐的性质。已知:Ka1(H2SO3)=1.54×10−2、Ka2(H2SO3)=1.02×10−7。
下列说法错误的是
| 实验 | 实验操作和现象 |
| 1 | 向10mL0.1mol/LNaOH溶液中通入11.2mL(标准状况)SO2,测得pH约为9 |
| 2 | 向10mL0.1mol/LNaOH溶液中通入SO2至溶液pH=6 |
| 3 | 向10mL0.1mol/LNaOH溶液中通入22.4mL(标准状况)SO2,测得pH约为3 |
| 4 | 取实验3所得溶液1mL,加入1mL0.01mol/LBaCl2溶液,产生白色沉淀 |
A.实验1得到的溶液中:c( )+c( )+c( )+c(H+)>c(OH-) )+c(H+)>c(OH-) |
B.实验2得到的溶液中:2c( )+c( )+c( )>c(Na+) )>c(Na+) |
C.实验3得到的溶液中:c(H+)+c(Na+)<c( )+2c(H2SO3)+c(OH-) )+2c(H2SO3)+c(OH-) |
| D.实验4中可知:Ksp(BaSO3)<2.55×10−8 |
您最近一年使用:0次
名校
解题方法
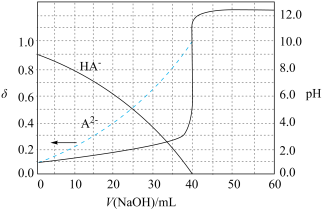
9 . 常温下,以酚酞作指示剂,用 的
的 溶液滴定
溶液滴定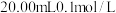 的二元酸
的二元酸 溶液。溶液中pH、含A微粒的分布系数
溶液。溶液中pH、含A微粒的分布系数 (物质的量分数)随滴加
(物质的量分数)随滴加 溶液体积
溶液体积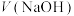 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是
 的
的 溶液滴定
溶液滴定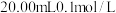 的二元酸
的二元酸 溶液。溶液中pH、含A微粒的分布系数
溶液。溶液中pH、含A微粒的分布系数 (物质的量分数)随滴加
(物质的量分数)随滴加 溶液体积
溶液体积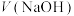 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是
A. 在水中电离的方程式为: 在水中电离的方程式为: , , |
B.当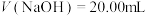 时,溶液中离子浓度大小顺序为: 时,溶液中离子浓度大小顺序为: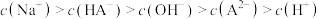 |
C.当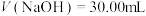 时, 时,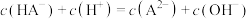 |
D.常温下, 的电离常数约为 的电离常数约为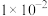 |
您最近一年使用:0次
2024-02-24更新
|
206次组卷
|
2卷引用:山东省济宁市第一中学2023-2024学年高二上学期第三次月考化学试题
解题方法
10 . 二氧化碳的捕集和资源化利用是缓解温室效应的重要战略方向。回答下列问题:
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。总反应可表示为:

该反应一般认为通过如下步骤来实现:
①

②

(1)若反应①为慢反应,请在图中接着完善画出反应②的能量变化曲线,标注出相应的物质(含聚集状态)以及总反应的 (含具体数值)
(含具体数值) _______ 。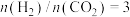 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为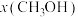 ,在
,在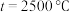 下的
下的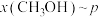 、在
、在 下的
下的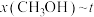 如图所示。
如图所示。_______ (填“a”或“b”),判断的理由_______ 。
(b)当 时,
时, 的平衡转化率
的平衡转化率
_______ 。
Ⅱ.催化CO2加氢合成乙酸在减少碳排放的同时还可以生产重要的化工原料。弱电解质的电离度是指弱电解质在溶液中达到电离平衡时,已电离的电解质分子数占原来总分子数(包括已电离的和未电离的>的百分数,用a表示。而在实验测定中,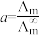 ,
,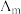 为一定浓度下电解质的摩尔电导率,
为一定浓度下电解质的摩尔电导率,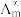 为无限稀释时溶液的摩尔电导率,
为无限稀释时溶液的摩尔电导率,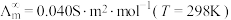 。某小组实验测得
。某小组实验测得 时,
时, 乙酸的
乙酸的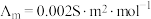 。
。
(3)在298K时,乙酸的电离平衡常数
_______ (列出计算式,不需化简)。
(4)在298K时,几种离子的摩尔电导率如下表所示。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择,最适宜的电解质为_______ (填化学式)。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。总反应可表示为:


该反应一般认为通过如下步骤来实现:
①


②


(1)若反应①为慢反应,请在图中接着完善画出反应②的能量变化曲线,标注出相应的物质(含聚集状态)以及总反应的
 (含具体数值)
(含具体数值) 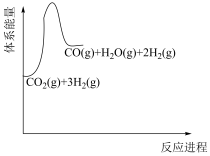
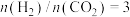 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为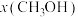 ,在
,在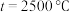 下的
下的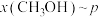 、在
、在 下的
下的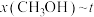 如图所示。
如图所示。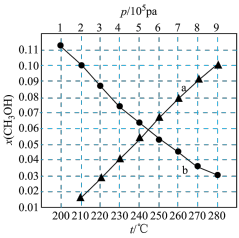
(b)当
 时,
时, 的平衡转化率
的平衡转化率
Ⅱ.催化CO2加氢合成乙酸在减少碳排放的同时还可以生产重要的化工原料。弱电解质的电离度是指弱电解质在溶液中达到电离平衡时,已电离的电解质分子数占原来总分子数(包括已电离的和未电离的>的百分数,用a表示。而在实验测定中,
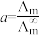 ,
,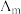 为一定浓度下电解质的摩尔电导率,
为一定浓度下电解质的摩尔电导率,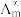 为无限稀释时溶液的摩尔电导率,
为无限稀释时溶液的摩尔电导率,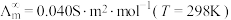 。某小组实验测得
。某小组实验测得 时,
时, 乙酸的
乙酸的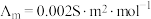 。
。(3)在298K时,乙酸的电离平衡常数

(4)在298K时,几种离子的摩尔电导率如下表所示。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择,最适宜的电解质为
| 离子种类 |  |  |  |  |  |  |
摩尔电导率/( ) ) | 349.82 | 79.80 | 76.34 | 50.18 | 73.52 | 50.11 |
您最近一年使用:0次



