解题方法
1 . 新冠疫情期间,家庭常备84消毒液、医用酒精等。某瓶84消毒液所贴标签的部分内容见图。有关该瓶消毒液的说法正确的是
84 消毒液 [用途]适用于一般物品的表面消毒,含餐具、果蔬、白色织物等。可杀灭肠道致病菌、化脓性球菌。 [性状]无色透明液体 [有效成分]次氯酸 [规格]500mL/瓶,约505g [含量]氯含量为 6.00% [贮藏]阴凉处密封保存 |
| A.每瓶消毒液含次氯酸钠约505g |
| B.消毒液的密度为1.10g⋅cm-3 |
| C.密封保存的目的是防止次氯酸钠见光分解 |
D.每瓶消毒液中含氯微粒的物质的量浓度约为1.71 |
您最近一年使用:0次
名校
解题方法
2 . 一定条件下, 溶液存在水解平衡:
溶液存在水解平衡: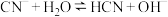 ,下列说法正确的是
,下列说法正确的是
 溶液存在水解平衡:
溶液存在水解平衡: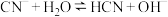 ,下列说法正确的是
,下列说法正确的是A.加入少量 固体, 固体,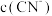 减小 减小 |
B.稀释溶液,溶液的 增大 增大 |
C.加入少量 固体, 固体,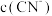 减小 减小 |
D.加入适量氢氰酸 得到的酸性混合溶液中 得到的酸性混合溶液中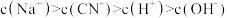 |
您最近一年使用:0次
3 . 用棕黄色 溶液探究影响盐类水解的因素,根据实验现象和原理,下列对水解程度判断正确的是
溶液探究影响盐类水解的因素,根据实验现象和原理,下列对水解程度判断正确的是
 溶液探究影响盐类水解的因素,根据实验现象和原理,下列对水解程度判断正确的是
溶液探究影响盐类水解的因素,根据实验现象和原理,下列对水解程度判断正确的是| 选项 | 实验 | 现象 | 水解程度 |
| A | 加入 固体 固体 | 溶液变成红褐色 | 变大 |
| B | 加热 溶液 溶液 | 溶液变成红褐色 | 不变 |
| C | 通入 气体 气体 | 溶液颜色变浅 | 减小 |
| D | 加入 溶液 溶液 | 溶液颜色变浅 | 不变 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-11更新
|
288次组卷
|
4卷引用:上海市浦东新区2022-2023学年高三上学期期末练习化学试题
上海市浦东新区2022-2023学年高三上学期期末练习化学试题(已下线)专题06 酸碱中和与盐类水解及难溶电解质的沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)(已下线)考点28 盐类的水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)第三章 水溶液中的离子反应与平衡 第三节 盐类的水解 第2课时 影响盐类水解的因素 水解原理的应用
名校
解题方法
4 . 下列叙述正确的是


| A.用如图装置制取无水氯化镁 |
| B.泡沫灭火器的主要原料是硫酸铝与碳酸钠溶液 |
C.稀释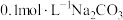 溶液,水解程度增大,溶液的 溶液,水解程度增大,溶液的 增大 增大 |
D.向滴有酚酞的 溶液中加入足量 溶液中加入足量 溶液,溶液红色褪去 溶液,溶液红色褪去 |
您最近一年使用:0次
5 . 25℃时,向 的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是
的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是
 的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是
的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是| A.氨水与氯化铵发生化学反应 |
B.氯化铵溶液水解显酸性,增加了 |
C.铵根离子浓度增大,抑制了氨水的电离,使 减小 减小 |
| D.氯化铵不稳定,分解产生了HCl |
您最近一年使用:0次
名校
6 . 对下列实验的分析,错误的是
| A | B | C | D |
 |  |  |  |
 水解平衡右移,pH减小 水解平衡右移,pH减小 |  的水解程度增大, 的水解程度增大, 减小 减小 |  可促进 可促进 的水解 的水解 | 混合液中  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-14更新
|
167次组卷
|
2卷引用:上海市杨浦区2022-2023学年高三上学期一模测试化学试题
14-15高二上·湖北荆州·期末
名校
解题方法
7 . NH4Al(SO4)2常作食品加工中的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其原理是_______ (用离子方程式说明)。
(2)相同条件下,0.1mol∙L-1NH4Al(SO4)2溶液中的c( )
)_______ (填“等于”“大于”或“小于”)0.1mol∙L-1NH4HSO4溶液中的c( )。
)。
(3)几种均为0.1mol∙L-1的电解质溶液的pH随温度变化的曲线如图所示。
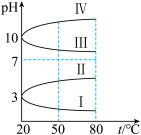
①其中符合0.1mol∙L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是_______ (填罗马数字),导致NH4Al(SO4)2溶液的pH随温度变化的原因是_______ 。
②20℃时,0.1mol∙L-1NH4Al(SO4)2溶液中2c c
c 3cAl3=
3cAl3=_______ molL1。
(4)室温时,向100mL0.1mol∙L-1NH4HSO4溶液中滴加0.1mol∙L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图乙所示。

试分析图中a、b、c、d四个点,水的电离程度最大的是_______ 点;在b点,溶液中各离子浓度由大到小的排列顺序是_______ 。
(1)NH4Al(SO4)2可作净水剂,其原理是
(2)相同条件下,0.1mol∙L-1NH4Al(SO4)2溶液中的c(
 )
) )。
)。(3)几种均为0.1mol∙L-1的电解质溶液的pH随温度变化的曲线如图所示。

①其中符合0.1mol∙L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是
②20℃时,0.1mol∙L-1NH4Al(SO4)2溶液中2c
 c
c 3cAl3=
3cAl3=(4)室温时,向100mL0.1mol∙L-1NH4HSO4溶液中滴加0.1mol∙L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图乙所示。

试分析图中a、b、c、d四个点,水的电离程度最大的是
您最近一年使用:0次
2022-12-01更新
|
1388次组卷
|
57卷引用:上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题
上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题(已下线)2013-2014学年湖北省荆州市部分县市高二上学期期末考试化学试卷(已下线)2014届山西省山大附中高三下学期第一次月考化学试卷2016-2017学年内蒙古包头九中高二上10月月考化学卷2016-2017学年四川省成都七中高二上11月考试化学卷2015—2016学年河南省郑州一中高二上学期期末考试化学试卷湖南省临武一中、嘉禾一中2017-2018学年高二12月联考化学试题河北省永年县第二中学2017-2018学年高二12月月考化学试题宁夏育才中学2017-2018学年高二上学期期末考试化学试题湖北省宜昌市第一中学2017-2018学年高二上学期期末考试化学试题高二人教版选修4 期末学业测评(一)山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题(已下线)2019年1月5日 《每日一题》人教选修4-周末培优吉林省松原市扶余市第一中学2018-2019学年高二上学期期末考试化学试题【全国百强校】江苏省扬州中学2018-2019学年高二第二学期五月检测化学试题(已下线)2019年10月13日《每日一题》2020年高考一轮复习——每周一测四川省武胜烈面中学校2019-2020学年高二上学期期中考试化学试题苏教版选修四化学反应原理专题3第三单元 盐类的水解 同步检测试卷(已下线)考点14 化学基本理论——《备战2020年高考精选考点专项突破题集》(已下线)2019年12月30日 《每日一题》人教版(选修4)——盐类水解的影响因素河北省沧州市泊头市第一中学2019-2020学年高二上学期第三次月考化学试题山东省淄博市2019-2020学年高二上学期期中考试化学试题四川省成都市射洪县2018-2019学年高二下学期期末能力素质监测理综化学试题(英才班)山西省晋中市祁县中学校2019-2020学年高二11月月考化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时3 水解平衡的移动和水解原理的应用河南省南阳市第一中学2021届高三上学期第二次月考(9月)化学试题高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三节 盐类的水解 课时2 盐类水解的影响因素及应用(已下线)第3章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)浙江省苍南县金乡卫城中学2020-2021学年高二上学期第一次月考化学试题(已下线)3.3.2 影响盐类水解的主要因素和盐类水解的应用(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)湖北省黄石市有色第一中学2020-2021学年高二上学期期末考试化学试题江苏省南通市海门实验学校2020-2021学年高二上学期期中考试化学试题福建省莆田锦江中学2020-2021学年高二上学期期末考试化学试题(已下线)第25讲 盐类水解(精练)-2022年高考化学一轮复习讲练测选择性必修1 专题3 第三单元 课时2 盐类水解的影响因素及应用安徽省皖南八校2022届高三上学期摸底联考化学试题(已下线)3.3.1 盐类的水解-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)第23讲 盐类水解(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)章末培优3 专题3 水溶液中的离子反应-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)(已下线)3.3.3 盐类水解的应用-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)3.3.2 影响盐类水解的主要因素-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第15练 反应原理综合-2022年【寒假分层作业】高二化学(人教版2019选择性必修2)辽宁省渤海大学附属高级中学2021-2022学年高二上学期期中考试化学试题四川省资阳中学2021-2022学年高二下学期3月月考化学试题山西省运城市教育发展联盟2021-2022学年高二上学期11月期中检测化学试题(已下线)3.3.2 影响盐类的水解的主要因素-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)第20讲 盐类水解的影响因素及应用(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)专题十三水溶液中的离子平衡四川省成都市树德中学2022-2023学年高二上学期期末考试化学试题四川省宜宾市第四中学校2022-2023学年高二下学期开学考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第49练 盐类的水解(已下线)专题突破卷09 水溶液中的离子反应与平衡 ?-2024年高考化学一轮复习考点通关卷(新教材新高考)广东省广州市华南师范大学附属中学2022-2023学年高二上学期12月月考化学试题(已下线)盐类的水解黑龙江省大庆铁人中学2023-2024学年高二上学期期中考试化学试题山西省朔州市怀仁县阳高一中2023-2024学年高二上学期11月化学试卷
名校
8 . 下列指定微粒数目一定相等的是
| A.等体积的CO2与SO2中含有的分子数 |
| B.等质量的C2H4与CO中含有的碳原子数 |
| C.等物质的量的S分别与足量Fe和Cu反应时转移的电子数 |
D.等体积等物质的量浓度的NH4Cl与NH4HCO3溶液中的NH 数 数 |
您最近一年使用:0次
9 . 冰壶比赛称为“冰上的国际象棋”,制作冰壶用的标准砥石的化学成分为石英碱长正长岩,常见的组分有钾长石K[AlSi3O8]和钠长石Na[AlSi3O8]等。完成下列填空:
(1)上述所涉及的元素中,具有相同电子数的简单离子半径由大到小的顺序是_______ ,原子核外有两个未成对电子的元素有_______ 。
(2)用一个化学方程式比较钠和铝的金属性的强弱_______ ,并用原子结构知识的观点解释原因_______ 。
(3)我国科学家发展了一种在200℃熔盐体系中,采用金属Al还原二氧化硅或硅酸盐、钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能,配平下列方程式_______ 。
______Al+_______K[AlSi3O8]+_______AlCl3→_______Si+_______AlOCl+_______KAlO2;
上述反应中若产生14g硅,转移的电子数为_______ 。
(4)KAlO2溶液中,n(K+)_______ n(AlO )(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因
)(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因_______ 。
(1)上述所涉及的元素中,具有相同电子数的简单离子半径由大到小的顺序是
(2)用一个化学方程式比较钠和铝的金属性的强弱
(3)我国科学家发展了一种在200℃熔盐体系中,采用金属Al还原二氧化硅或硅酸盐、钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能,配平下列方程式
______Al+_______K[AlSi3O8]+_______AlCl3→_______Si+_______AlOCl+_______KAlO2;
上述反应中若产生14g硅,转移的电子数为
(4)KAlO2溶液中,n(K+)
 )(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因
)(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因
您最近一年使用:0次
解题方法
10 . I.联氨(N2H4)及其衍生物是一类重要的火箭燃料。N2H4与N2O4反应能放出大量的热。
(1)在25℃时,1.00gN2H4(l)与足量N2O4(1)完全反应生成N2(g)和H2O(1),放出19.14kJ的热量。写出该反应的热化学方程式_______ 。
II.NO2是氮的常见氧化物,能自发发生如下反应:2NO2(g)⇌N2O4(g) =-57.20kJ/mol
=-57.20kJ/mol
(2)写出该反应的平衡常数表达式K=_______ 。已知:在一定温度下的密闭容器中,该反应已达到平衡。保持其他条件不变,下列措施能提高NO2转化率的是_______ 。
a.减小NO2的浓度 b.降低温度 c.增大压强 d.升高温度
III.Na2CO3俗称纯碱,是生活中的常用物质。某化学兴趣小组的同学对Na2CO3溶液显碱性的原因进行了探究,设计了如下实验方案进行操作并记录实验现象。
(3)①该实验表明,Na2CO3溶液显碱性的原因是_______ (请结合化学用语,简要说明)。
②从形成盐的酸和碱的强弱角度看,Na2CO3属于_______ 盐。
③为了使Na2CO3溶液中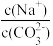 的比值变小,可适量加入(或通入)的物质是
的比值变小,可适量加入(或通入)的物质是_______ 。
a.CO2气体 b.KOH固体 c.HCl气体 d.Na2CO3固体
(1)在25℃时,1.00gN2H4(l)与足量N2O4(1)完全反应生成N2(g)和H2O(1),放出19.14kJ的热量。写出该反应的热化学方程式
II.NO2是氮的常见氧化物,能自发发生如下反应:2NO2(g)⇌N2O4(g)
 =-57.20kJ/mol
=-57.20kJ/mol(2)写出该反应的平衡常数表达式K=
a.减小NO2的浓度 b.降低温度 c.增大压强 d.升高温度
III.Na2CO3俗称纯碱,是生活中的常用物质。某化学兴趣小组的同学对Na2CO3溶液显碱性的原因进行了探究,设计了如下实验方案进行操作并记录实验现象。
| 实验操作 | 实验现象 |
| 取少量Na2CO3固体,加入无水酒精,充分振荡、静置 | 溶液为无色 |
| 取上层清液于试管中,滴加酚酞试剂 | 溶液为无色 |
| 在试管中继续加入少量水 | 溶液变为红色 |
| 向该红色溶液中滴加足量BaCl2溶液(中性) | 红色褪去 |
②从形成盐的酸和碱的强弱角度看,Na2CO3属于
③为了使Na2CO3溶液中
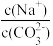 的比值变小,可适量加入(或通入)的物质是
的比值变小,可适量加入(或通入)的物质是a.CO2气体 b.KOH固体 c.HCl气体 d.Na2CO3固体
您最近一年使用:0次
2022-04-28更新
|
228次组卷
|
2卷引用:上海市宝山区2021-2022学年高三年级下学期等级考测化学试题



