10-11高二下·福建福州·期末
1 . 在一定条件下,Na2CO3溶液存在水解平衡: +H2O⇌
+H2O⇌ +OH-。下列说法正确的是
+OH-。下列说法正确的是
 +H2O⇌
+H2O⇌ +OH-。下列说法正确的是
+OH-。下列说法正确的是| A.稀释溶液,水解平衡常数增大 | B.通入CO2,平衡朝正反应方向移动 |
C.升高温度,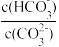 减小 减小 | D.加入NaOH固体,溶液pH减小 |
您最近一年使用:0次
2020-12-23更新
|
2122次组卷
|
48卷引用:安徽省滁州市定远县民族中学2018-2019学年高二上学期12月月考化学试题
安徽省滁州市定远县民族中学2018-2019学年高二上学期12月月考化学试题安徽省泗县第一中学2020-2021学年高二上学期第二次月考化学试题安徽省芜湖市无为襄安中学2022-2023学年高二上学期12月月考化学试题(已下线)2010-2011年福建省福州八中高二下学期期末考试化学试卷(已下线)2012-2013学年福建省福州八县一中高二上学期期末联考化学试卷(已下线)2013-2014学年山东省山师附中高二上学期期中考试化学试卷2014-2015学年甘肃省武威市六中高二上学期期中化学(理)试卷2014-2015宁夏回族自治区银川一中高二上学期期末考试化学试卷2015届天津市津南区高三4月模拟练习理科综合化学试卷2015-2016学年内蒙古杭锦后旗奋斗中学高二下期中化学卷2016-2017学年辽宁省鞍山一中高二上期中化学试卷山东省曲阜师范大学附属中学2017-2018学年高二上学期期中考试化学试题福建省福州市2016-2017学年高二上学期期中考试化学试题甘肃省兰州市第四中学2017-2018学年高二上学期期末考试化学试题甘肃省靖远四中2018-2019学年高二第二学期开学检测化学试题(已下线)专题8.3 盐类水解(讲)-《2020年高考一轮复习讲练测》山东省德州市陵城区第一中学2019-2020学年高二12月月考化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——盐类水解平衡的影响因素及探究(强化练习)湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题7 盐类水解的基础知识复习题黑龙江省牡丹江市东部地区四校联考2019-2020学年高二上学期期末考试化学试题河北省石家庄市元氏县第四中学2020-2021学年高二上学期第一次月考化学试题河北省石家庄市辛集市第一中学2020-2021学年高二上学期第一次考试化学试题(已下线)第27讲 盐类水解(精讲)——2021年高考化学一轮复习讲练测(已下线)3.3.2 影响盐类水解的主要因素 盐类水解的应用(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)贵州省安顺市大洋实验学校2020-2021学年高二上学期期中考试化学试题江西省赣县第三中学2020-2021学年高二上学期12月月考化学试题江西省吉安县立中学2020-2021学年高二上学期期中考试化学试题河南省鹤壁市高中2020-2021学年高二年级上学期尖子生联赛调研(三)化学试题宁夏吴忠中学2020-2021学年高二上学期期末考试化学试题(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时42 盐类的水解影响因素及应用-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题3.3.2 影响盐类水解的主要因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)3.3.2 影响盐类水解的主要因素-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)3.3.2 影响盐类水解的主要因素(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)湖南省长沙市南雅中学2018-2019学年高二上学期期中考试化学试题甘肃省张掖市第二中学2021-2022学年高二上学期11月月考化学试题江西省抚州市南城县第二中学2021-2022年高二上学期第二次月考化学试题贵州省毕节市第一中学2021-2022学年高二上学期第二次阶段性考试化学试题四川省乐山市峨眉第二中学校2021-2022学年高二下学期3月月考化学试题(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)河南省三门峡市渑池县第二高级中学2021-2022学年高二上学期第二次月考化学试题天津市第二中学2022-2023学年高二上学期期中检测化学试题陕西省延安市富县高级中学2021-2022学年高二上学期期中考试化学试题3.3.2影响盐类水解的因素 课前浙江省杭州第十一中学2023-2024学年高二上学期期末考试化学试题
名校
2 . 通入HCl气体或加入NaOH固体会使下列离子浓度都减小的是
A. | B.Al3+ | C.CH3COO- | D. |
您最近一年使用:0次
名校
3 . 为了配制CH3COO-与Na+离子浓度为1:1的CH3COONa溶液,可向CH3COONa溶液中加入
| A.适量NaCl晶体 | B.适量NaOH固体 |
| C.适量盐酸 | D.适量KOH固体 |
您最近一年使用:0次
解题方法
4 . 某班同学用如下实验探究Fe2+、Fe3+的性质。
请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol·L-1的溶液.在FeCl2溶液中需加入少量铁屑,其目的是____ 。
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为:___ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是___ 。
(4)丙组同学取l0mL0.lmol·L-1KI溶液,加入6mL0.lmol·L-1FeCl3溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
①第一支试管中加入lmLCCl4充分振荡、静置,CCl4层显紫色;
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀:
③第三支试行中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是(填离子符号)___ ;实验①和③说明:在I-过量的情况下,溶液中仍含有(填离子符号)____ ,由此可以证明该氧化还原反应为___ 。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为____ ;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是___ ;生成沉淀的原因是(用平衡移动原理解释)____ 。
(6)戊组同学模拟工业上用NaClO3氧化酸性FeCl2废液制备FeCl3。
①若酸性FeCl2废液中:c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1,c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为___ 。
②完成NaClO3氧化FeCl2的离子方程式:___ 。
 ClO
ClO +
+ Fe2++
Fe2++ ___=
___= Cl-+
Cl-+ Fe3++
Fe3++ ___
___
③FeCl3具有净水作用,其原理是___ 。
请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol·L-1的溶液.在FeCl2溶液中需加入少量铁屑,其目的是
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为:
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
(4)丙组同学取l0mL0.lmol·L-1KI溶液,加入6mL0.lmol·L-1FeCl3溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
①第一支试管中加入lmLCCl4充分振荡、静置,CCl4层显紫色;
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀:
③第三支试行中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是(填离子符号)
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
(6)戊组同学模拟工业上用NaClO3氧化酸性FeCl2废液制备FeCl3。
①若酸性FeCl2废液中:c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1,c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为
②完成NaClO3氧化FeCl2的离子方程式:
 ClO
ClO +
+ Fe2++
Fe2++ ___=
___= Cl-+
Cl-+ Fe3++
Fe3++ ___
___③FeCl3具有净水作用,其原理是
您最近一年使用:0次
5 . 回答下列问题:
(1)已知:H2S:Ka1=1.3×10-7 Ka2=7.1×10-15 H2CO3:Ka1=4.3×10-7 Ka2=5.6×10-11 CH3COOH:Ka=1.8×10-5 NH3·H2O:Kb=1.8×10-5
①常温下,0.1mol·L-1Na2S溶液和0.1mol·L-1Na2CO3溶液,碱性更强的是______ ,其原因是_______ 。
②25℃时,CH3COONH4溶液显______ 性。NaHCO3溶液的pH______ (填“大于”或“小于”)CH3COONa溶液的pH。
③NH4HCO3溶液显______ 性,原因是_______ 。
(2)25 ℃时,H2SO3⇌HSO +H+的电离常数Ka=1.0×10-2,则该温度下NaHSO3的水解常数Kh=
+H+的电离常数Ka=1.0×10-2,则该温度下NaHSO3的水解常数Kh=___ ;若向NaHSO3溶液中加入少量的I2,则溶液中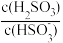 将
将______ (填“增大”“减小”或“不变”)。
(3)能证明Na2SO3溶液中存在SO +H2O⇌HSO
+H2O⇌HSO +OH-水解平衡的事实是
+OH-水解平衡的事实是_____ (填字母,下同)。
A.滴入酚酞溶液变红,再加H2SO4溶液红色褪去
B.滴入酚酞溶液变红,再加BaCl2溶液后产生沉淀且红色褪去
C.滴入酚酞溶液变红,再加氯水后红色褪去
(4)已知:Ka(HClO2)=1.1×10-2,Ka(CH3COOH)=1.8×10-5。25℃时,浓度均为0.1mol·L-1的NaClO2溶液和CH3COONa溶液,两溶液中c(ClO )
)______ (填“>”“<”或“=”)c(CH3COO-)。若要使两溶液的pH相等应________ 。
a.向NaClO2溶液中加适量水
b.向NaClO2溶液中加适量NaOH
c.向CH3COONa溶液中加CH3COONa固体
d.向CH3COONa溶液中加适量的水
(5)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是_______ (用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是________ 。
(1)已知:H2S:Ka1=1.3×10-7 Ka2=7.1×10-15 H2CO3:Ka1=4.3×10-7 Ka2=5.6×10-11 CH3COOH:Ka=1.8×10-5 NH3·H2O:Kb=1.8×10-5
①常温下,0.1mol·L-1Na2S溶液和0.1mol·L-1Na2CO3溶液,碱性更强的是
②25℃时,CH3COONH4溶液显
③NH4HCO3溶液显
(2)25 ℃时,H2SO3⇌HSO
 +H+的电离常数Ka=1.0×10-2,则该温度下NaHSO3的水解常数Kh=
+H+的电离常数Ka=1.0×10-2,则该温度下NaHSO3的水解常数Kh=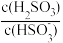 将
将(3)能证明Na2SO3溶液中存在SO
 +H2O⇌HSO
+H2O⇌HSO +OH-水解平衡的事实是
+OH-水解平衡的事实是A.滴入酚酞溶液变红,再加H2SO4溶液红色褪去
B.滴入酚酞溶液变红,再加BaCl2溶液后产生沉淀且红色褪去
C.滴入酚酞溶液变红,再加氯水后红色褪去
(4)已知:Ka(HClO2)=1.1×10-2,Ka(CH3COOH)=1.8×10-5。25℃时,浓度均为0.1mol·L-1的NaClO2溶液和CH3COONa溶液,两溶液中c(ClO
 )
)a.向NaClO2溶液中加适量水
b.向NaClO2溶液中加适量NaOH
c.向CH3COONa溶液中加CH3COONa固体
d.向CH3COONa溶液中加适量的水
(5)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是
您最近一年使用:0次
2020-12-09更新
|
407次组卷
|
2卷引用:安徽省肥东县高级中学2020-2021学年高二上学期期中考试化学试题
名校
6 . 欲使醋酸钠溶液中 的水解程度减小,
的水解程度减小, 增大,可采用的方法是
增大,可采用的方法是
 的水解程度减小,
的水解程度减小, 增大,可采用的方法是
增大,可采用的方法是| A.加热 | B.加水稀释 |
| C.加入少量NaOH固体 | D.加入少量 固体 固体 |
您最近一年使用:0次
2020-11-26更新
|
352次组卷
|
5卷引用:安徽省六安市新安中学2020-2021学年高二12月月考化学(A)试题
名校
7 . 下列说法正确的是
A.向0.1 mol•L−1的氨水中加少量硫酸铵固体,则溶液中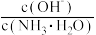 增大 增大 |
| B.常温下,0.1 mol·L−1一元酸(HA)溶液pH=3,则该溶液中,c2(H+)=c(H+)×c(A−)+KW |
C.向盐酸中加入氨水至中性,溶液中 |
| D.将Ca(ClO)2、Na2SO3、FeCl3、NaAlO2溶液蒸干均得不到原溶质 |
您最近一年使用:0次
名校
8 . 弱酸的电离平衡常数与对应酸根的水解平衡常数存在某种定量关系。
(1)NO2可用氨水吸收生成NH4NO3。25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是___ (用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将___ (填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为___ mol·L-1(NH3·H2O的电离平衡常数取Kb=2×10-5)。
(2)已知常温下CN-的水解常数Kh=1.61×10-5。
①含等物质的量浓度HCN与NaCN的混合溶液显___ (填“酸”“碱”或“中”)性,c(CN-)___ (填“>”“<”或“=”)c(HCN)。溶液中各离子浓度由大到小的顺序为___ 。
②常温下,若将cmol·L-1的盐酸与0.62mol·L-1的KCN等体积混合后恰好得到中性溶液,则c=___ (小数点后保留4位数字)。
(1)NO2可用氨水吸收生成NH4NO3。25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是
(2)已知常温下CN-的水解常数Kh=1.61×10-5。
①含等物质的量浓度HCN与NaCN的混合溶液显
②常温下,若将cmol·L-1的盐酸与0.62mol·L-1的KCN等体积混合后恰好得到中性溶液,则c=
您最近一年使用:0次
2020-11-04更新
|
131次组卷
|
2卷引用:安徽涡阳县育萃中学2020-2021学年高二上学期第二次月考化学试题
名校
9 . 有pH分别为8、9、10的三种相同物质的量浓度的盐溶液NaA、NaB、NaC,以下说法中不正确的是
| A.在三种酸HA、HB、HC中以HC酸性相对最弱 |
| B.中和1mol三种酸,需要的NaOH均为1mol |
| C.在A-、B-、C-三者中,A-结合H+的能力最强 |
| D.HA、HB、HC三者均为弱酸 |
您最近一年使用:0次
2020-10-15更新
|
282次组卷
|
3卷引用:安徽省阜阳市太和第一中学2020-2021学年高二上学期10月月考化学试题
名校
10 . 采取下列措施后,溶液颜色变深的是
| A.加热明矾溶液(滴有酚酞试液) |
B.加热 溶液(滴有酚酞试液) 溶液(滴有酚酞试液) |
C.氨水(滴有酚酞试液)中加入少量 固体 固体 |
D.小苏打溶液(滴有酚酞试液)中加入少量 固体 固体 |
您最近一年使用:0次
2020-10-13更新
|
521次组卷
|
5卷引用:安徽省安庆市怀宁县第二中学2023-2024学年高二上学期期末化学试题
安徽省安庆市怀宁县第二中学2023-2024学年高二上学期期末化学试题人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第三节 盐类的水解 课时2 影响盐类水解的主要因素和盐类水解的应用吉林省长春市第二实验中学2020-2021学年高二上学期期中考试化学试题(已下线)3.3.2 影响盐类水解的主要因素(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)吉林油田第十一中学2021-2022学年高二上学期期中考试化学试题



