解题方法
1 . 化学与生活、生产息息相关。下列说法正确的是
| A.铁管上镶嵌锌块,铁管不易被腐蚀 |
| B.铵态氮肥和草木灰混合施用肥效更好 |
C.医疗上常用 作X射线透视肠胃的内服剂 作X射线透视肠胃的内服剂 |
| D.盐酸的腐蚀性比醋酸大,不能用于卫生洁具的清洁 |
您最近一年使用:0次
名校
2 . 化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度的变化,用公式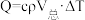 计算获得。(注:实验所用酸、碱、盐溶液的密度和比热容与水相同,忽略水以外各物质吸收的热量,忽略实验装置的比热容,c和
计算获得。(注:实验所用酸、碱、盐溶液的密度和比热容与水相同,忽略水以外各物质吸收的热量,忽略实验装置的比热容,c和 分别取4.18
分别取4.18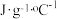 和1.0
和1.0 ,下同)请回答下列问题:
,下同)请回答下列问题:
(1)NaOH溶液浓度的测定:移取20.00mL待测液,加入指示剂,用0.5000 的盐酸溶液滴定至终点,消耗盐酸溶液22.00mL。在测定过程中,滴定操作的顺序为检查是否漏水→蒸馏水洗涤→
的盐酸溶液滴定至终点,消耗盐酸溶液22.00mL。在测定过程中,滴定操作的顺序为检查是否漏水→蒸馏水洗涤→___ (用序号表示)→滴定→达到滴定终点,停止滴定,记录读数。
a.轻轻转动滴定管的活塞,使滴定管尖嘴部分充满溶液,无气泡
b.调整管中液面至“0”或“0”刻度以下,记录读数
c.将洗涤液从滴定管下部放入预置的烧杯中
d.装入标准溶液至“0”刻度以上2~3mL,固定好滴定管
e.从滴定管上口加入3mL所要盛装的溶液,倾斜着转动滴定管
(2)热量的测定:取上述NaOH溶液和盐酸各50mL进行反应。
①实验室现有纸条、硬纸板(中心有两个小孔)、量筒、100mL烧杯,为了完成该实验,还需要图中的实验仪器是_______ (填序号)。 、
、 ,则该过程放出的热量为
,则该过程放出的热量为______ J(用含 、
、 的式子表示)。
的式子表示)。
(3)借鉴(2)的方法,甲同学测量放热反应: 的焓变
的焓变 (忽略温度对焓变的影响,下同)。实验结果见下表:
(忽略温度对焓变的影响,下同)。实验结果见下表:
温度:b、c、d的大小关系为_______ 。结果表明,该方法可行。
(4)乙同学也借鉴(2)的方法,测量反应A: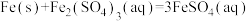 的焓变△H。
的焓变△H。
查阅资料:配制 溶液时需加入酸。
溶液时需加入酸。
提出猜想:Fe粉与 溶液混合,在反应A进行的过程中,可能存在反应B:
溶液混合,在反应A进行的过程中,可能存在反应B:_______ (填化学方程式)。
验证猜想:用pH试纸测得 溶液的pH不大于1;向少量
溶液的pH不大于1;向少量 溶液中加入Fe粉,观察到的现象为
溶液中加入Fe粉,观察到的现象为____ ,说明同时存在反应A和B。
实验小结:猜想成立,不能直接测得反应A的焓变 。
。
教师指导:结合甲同学的测定结果及盖斯定律可以计算无法直接测定的反应热。
优化设计:根据相关原理,丙同学还需要测定反应_______ (填化学方程式)的焓变 ,通过计算可得反应A的焓变
,通过计算可得反应A的焓变
______ (用含 和
和 的式子表示)。
的式子表示)。
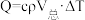 计算获得。(注:实验所用酸、碱、盐溶液的密度和比热容与水相同,忽略水以外各物质吸收的热量,忽略实验装置的比热容,c和
计算获得。(注:实验所用酸、碱、盐溶液的密度和比热容与水相同,忽略水以外各物质吸收的热量,忽略实验装置的比热容,c和 分别取4.18
分别取4.18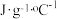 和1.0
和1.0 ,下同)请回答下列问题:
,下同)请回答下列问题:(1)NaOH溶液浓度的测定:移取20.00mL待测液,加入指示剂,用0.5000
 的盐酸溶液滴定至终点,消耗盐酸溶液22.00mL。在测定过程中,滴定操作的顺序为检查是否漏水→蒸馏水洗涤→
的盐酸溶液滴定至终点,消耗盐酸溶液22.00mL。在测定过程中,滴定操作的顺序为检查是否漏水→蒸馏水洗涤→a.轻轻转动滴定管的活塞,使滴定管尖嘴部分充满溶液,无气泡
b.调整管中液面至“0”或“0”刻度以下,记录读数
c.将洗涤液从滴定管下部放入预置的烧杯中
d.装入标准溶液至“0”刻度以上2~3mL,固定好滴定管
e.从滴定管上口加入3mL所要盛装的溶液,倾斜着转动滴定管
(2)热量的测定:取上述NaOH溶液和盐酸各50mL进行反应。
①实验室现有纸条、硬纸板(中心有两个小孔)、量筒、100mL烧杯,为了完成该实验,还需要图中的实验仪器是
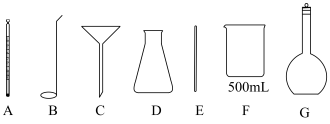
 、
、 ,则该过程放出的热量为
,则该过程放出的热量为 、
、 的式子表示)。
的式子表示)。(3)借鉴(2)的方法,甲同学测量放热反应:
 的焓变
的焓变 (忽略温度对焓变的影响,下同)。实验结果见下表:
(忽略温度对焓变的影响,下同)。实验结果见下表:| 序号 | 反应试剂 | 体系温度/℃ | ||
| 反应前 | 反应后 | |||
| ⅰ | 0.2  溶液100mL 溶液100mL | 0.56g铁粉 | a | b |
| ⅱ | 1.12g铁粉 | a | c | |
| ⅲ | 1.68g铁粉 | a | d | |
(4)乙同学也借鉴(2)的方法,测量反应A:
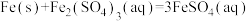 的焓变△H。
的焓变△H。查阅资料:配制
 溶液时需加入酸。
溶液时需加入酸。提出猜想:Fe粉与
 溶液混合,在反应A进行的过程中,可能存在反应B:
溶液混合,在反应A进行的过程中,可能存在反应B:验证猜想:用pH试纸测得
 溶液的pH不大于1;向少量
溶液的pH不大于1;向少量 溶液中加入Fe粉,观察到的现象为
溶液中加入Fe粉,观察到的现象为实验小结:猜想成立,不能直接测得反应A的焓变
 。
。教师指导:结合甲同学的测定结果及盖斯定律可以计算无法直接测定的反应热。
优化设计:根据相关原理,丙同学还需要测定反应
 ,通过计算可得反应A的焓变
,通过计算可得反应A的焓变
 和
和 的式子表示)。
的式子表示)。
您最近一年使用:0次
解题方法
3 . 乙二胺( ,简写为X)为二元弱碱。25℃时,向
,简写为X)为二元弱碱。25℃时,向 其盐酸盐溶液
其盐酸盐溶液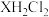 中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中
中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中 、
、 、X三种粒子浓度的对数值(
、X三种粒子浓度的对数值( )与
)与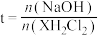 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 ,简写为X)为二元弱碱。25℃时,向
,简写为X)为二元弱碱。25℃时,向 其盐酸盐溶液
其盐酸盐溶液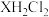 中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中
中加入固体NaOH(溶液体积变化忽略不计),溶液pOH与体系中 、
、 、X三种粒子浓度的对数值(
、X三种粒子浓度的对数值( )与
)与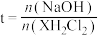 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是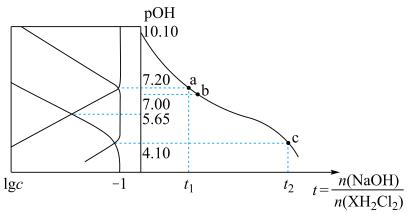
A.乙二胺第一、二步电离常数的数量级分别为 、 、 |
B.当 时, 时, |
C.b点时,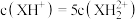 |
D.c点时,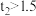 |
您最近一年使用:0次
4 . 按要求填空
(1)NaHCO3的水溶液呈___________ (填“酸”、“中”、“碱”)性,实验室保存NaHCO3溶液的试剂瓶应用___________ 塞,原因___________ (写出有关的离子方程式,下同);Al2(SO4)3显酸性,溶液蒸干最后得到的固体产物是___________ 。
(2)常温下,下列溶液中,c(H+)由小到大的排列顺序是___________ 。
①0.1mol/LHCl溶液 ②0.1mol/LH2SO4溶液 ③0.1mol/LNaOH溶液 ④0.1mol/LCH3COOH溶液。
(3)25℃时,有 的盐酸和
的盐酸和 的
的 溶液中由水电离出的c(H+)之比为
溶液中由水电离出的c(H+)之比为___________ 。
(4)已知: :
: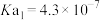 ;
; ,
, :
: 。
。
①相同条件下,试比较 、
、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为___________ 。
②则将 气体通入足量的
气体通入足量的 溶液中的离子反应方程式为
溶液中的离子反应方程式为___________ 。
(1)NaHCO3的水溶液呈
(2)常温下,下列溶液中,c(H+)由小到大的排列顺序是
①0.1mol/LHCl溶液 ②0.1mol/LH2SO4溶液 ③0.1mol/LNaOH溶液 ④0.1mol/LCH3COOH溶液。
(3)25℃时,有
 的盐酸和
的盐酸和 的
的 溶液中由水电离出的c(H+)之比为
溶液中由水电离出的c(H+)之比为(4)已知:
 :
: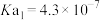 ;
; ,
, :
: 。
。①相同条件下,试比较
 、
、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为②则将
 气体通入足量的
气体通入足量的 溶液中的离子反应方程式为
溶液中的离子反应方程式为
您最近一年使用:0次
解题方法
5 . 已知溶液A中含有Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀时的pH如下表:
___________ 。
(2)加入CuO作用是调节pH,则pH的范围:___________ 。还可以用哪些物质来代替CuO?___________ 。
(3)操作1为___________ ,操作2为___________ 。
| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| pH | 开始沉淀 | 1.9 | 7.0 | 4.7 |
| 完全沉淀 | 3.2 | 9.0 | 6.7 | |
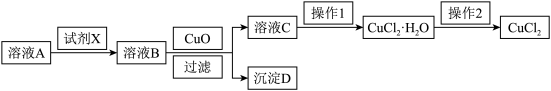
(2)加入CuO作用是调节pH,则pH的范围:
(3)操作1为
您最近一年使用:0次
名校
解题方法
6 . 钛白粉(纳米级 )广泛用作功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料,是白色颜料中着色力最强的一种,具有优良的遮盖力和着色牢度,适用于不透明的白色制品。以钛铁矿(主要成分为
)广泛用作功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料,是白色颜料中着色力最强的一种,具有优良的遮盖力和着色牢度,适用于不透明的白色制品。以钛铁矿(主要成分为 、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图。
、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图。 不反应。钛元素在整个流程中化合价没有变化。
不反应。钛元素在整个流程中化合价没有变化。
(1)稀硫酸浸出的目的是_______ 。
(2)下图分别为不同固液比、温度下滤渣与热浓硫酸反应时的Ti浸出率,据图分析,最适合的固液比和温度分别是_______ 、_______ 。 ,则浓硫酸与
,则浓硫酸与 反应的化学方程式为
反应的化学方程式为_______ 。
(4)“一系列操作”包括_______ ,过滤,洗涤,干燥。得到的绿矾先用稀钛液洗涤,再用冰水洗涤。用冰水洗涤的优点是_______ 。
(5)将钛液加热煮沸的目的是_______ 。
(6)若取10kg钛铁矿( 的质量分数为95%,)经过上述流程(钛元素在整个流程中损失率为5%),则可制得钛白粉固体的质量为
的质量分数为95%,)经过上述流程(钛元素在整个流程中损失率为5%),则可制得钛白粉固体的质量为_______ kg。
 )广泛用作功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料,是白色颜料中着色力最强的一种,具有优良的遮盖力和着色牢度,适用于不透明的白色制品。以钛铁矿(主要成分为
)广泛用作功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料,是白色颜料中着色力最强的一种,具有优良的遮盖力和着色牢度,适用于不透明的白色制品。以钛铁矿(主要成分为 、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图。
、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图。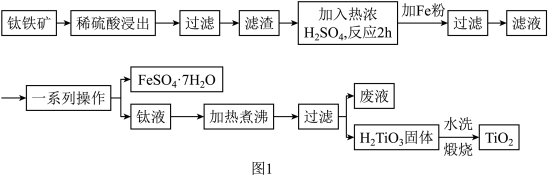
 不反应。钛元素在整个流程中化合价没有变化。
不反应。钛元素在整个流程中化合价没有变化。(1)稀硫酸浸出的目的是
(2)下图分别为不同固液比、温度下滤渣与热浓硫酸反应时的Ti浸出率,据图分析,最适合的固液比和温度分别是
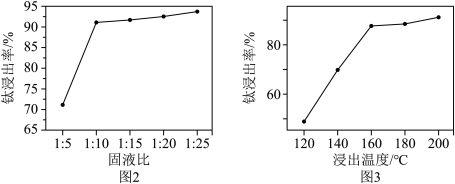
 ,则浓硫酸与
,则浓硫酸与 反应的化学方程式为
反应的化学方程式为(4)“一系列操作”包括
(5)将钛液加热煮沸的目的是
(6)若取10kg钛铁矿(
 的质量分数为95%,)经过上述流程(钛元素在整个流程中损失率为5%),则可制得钛白粉固体的质量为
的质量分数为95%,)经过上述流程(钛元素在整个流程中损失率为5%),则可制得钛白粉固体的质量为
您最近一年使用:0次
7 . 铜(Ⅰ)配合物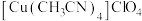 的制备及纯度分析步骤如下。
的制备及纯度分析步骤如下。
1.制备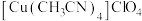
将乙腈的 ,
, ,过量钢材混合于圆底烧瓶,控温85°C、磁力搅拌,至反应完全(装置如图),经一系列操作,得到白色固体产品。
,过量钢材混合于圆底烧瓶,控温85°C、磁力搅拌,至反应完全(装置如图),经一系列操作,得到白色固体产品。
取 产品完全溶解于足量浓硝酸中,再加水、醋酸钠溶液配成250.0mL溶液。取25.0mL溶液,加入指示剂后,再用
产品完全溶解于足量浓硝酸中,再加水、醋酸钠溶液配成250.0mL溶液。取25.0mL溶液,加入指示剂后,再用 EDTA标准溶液滴定至终点。平行滴定三次,消耗EDTA溶液的平均体积为
EDTA标准溶液滴定至终点。平行滴定三次,消耗EDTA溶液的平均体积为 。
。
已知:① 沸点为81℃.酸性条件下遇水生成
沸点为81℃.酸性条件下遇水生成
②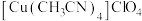 (
(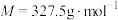 )较易被空气氧化:
)较易被空气氧化:
③EDTA与 形成1:1配合物:
形成1:1配合物:
④滴定需在弱碱性条件下进行。
回答下列问题:
(1)图中仪器 的作用是
的作用是______ , 中应加入
中应加入______ 作为最佳传热介质。
(2)加入过量铜粉能提高产物的纯度,可能的原因是______ .
(3)“一系列操作”依次为过滤分离出滤液、______ 冷却结晶、过滤、洗涤、干燥。
(4) 与足量浓硝酸发生反应的离子方程式为
与足量浓硝酸发生反应的离子方程式为______ .
(5)加入醋酸钠溶液的主要目的是______ .
(6)测得产品的纯度为______ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(7)下列情况会导致产品纯度测定结果偏高的有______.
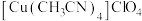 的制备及纯度分析步骤如下。
的制备及纯度分析步骤如下。1.制备
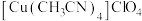
将乙腈的
 ,
, ,过量钢材混合于圆底烧瓶,控温85°C、磁力搅拌,至反应完全(装置如图),经一系列操作,得到白色固体产品。
,过量钢材混合于圆底烧瓶,控温85°C、磁力搅拌,至反应完全(装置如图),经一系列操作,得到白色固体产品。
取
 产品完全溶解于足量浓硝酸中,再加水、醋酸钠溶液配成250.0mL溶液。取25.0mL溶液,加入指示剂后,再用
产品完全溶解于足量浓硝酸中,再加水、醋酸钠溶液配成250.0mL溶液。取25.0mL溶液,加入指示剂后,再用 EDTA标准溶液滴定至终点。平行滴定三次,消耗EDTA溶液的平均体积为
EDTA标准溶液滴定至终点。平行滴定三次,消耗EDTA溶液的平均体积为 。
。已知:①
 沸点为81℃.酸性条件下遇水生成
沸点为81℃.酸性条件下遇水生成
②
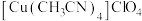 (
(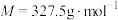 )较易被空气氧化:
)较易被空气氧化:③EDTA与
 形成1:1配合物:
形成1:1配合物:④滴定需在弱碱性条件下进行。
回答下列问题:
(1)图中仪器
 的作用是
的作用是 中应加入
中应加入(2)加入过量铜粉能提高产物的纯度,可能的原因是
(3)“一系列操作”依次为过滤分离出滤液、
(4)
 与足量浓硝酸发生反应的离子方程式为
与足量浓硝酸发生反应的离子方程式为(5)加入醋酸钠溶液的主要目的是
(6)测得产品的纯度为
 、
、 、
、 的代数式表示)。
的代数式表示)。(7)下列情况会导致产品纯度测定结果偏高的有______.
A.产品中含有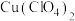 | B.滴定终点时俯视读数 |
| C.盛装EDTA溶液的滴定管未润洗 | D.产品干燥不充分 |
您最近一年使用:0次
名校
解题方法
8 . 由硫铁矿烧渣(含 等)制取无水氯化铁的实验原理和装置
等)制取无水氯化铁的实验原理和装置不 能达到实验目的的是
 等)制取无水氯化铁的实验原理和装置
等)制取无水氯化铁的实验原理和装置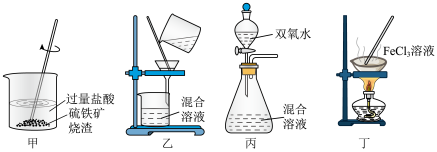
| A.用装置甲溶解硫铁矿烧渣 | B.用装置乙过滤得到含 混合溶液 混合溶液 |
C.用装置丙氧化得到 溶液 溶液 | D.用装置丁蒸干溶液获得 |
您最近一年使用:0次
解题方法
9 . 下列有关离子方程式书写错误的是
A.用纯碱溶液浸泡锅炉水垢(CaSO4):CaSO4(s)+ (aq) (aq)  (aq)+CaCO3(s) (aq)+CaCO3(s) |
B.泡沫灭火器工作原理:Al3++3 =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
C.纯碱溶液去除油污: +H2O +H2O  +OH- +OH- |
D.明矾净水的原理:Al3++3H2O Al(OH)3↓+3H+ Al(OH)3↓+3H+ |
您最近一年使用:0次
10 . 下列生产、生活或化学实验中的应用,不能利用勒夏特列原理进行解释的是
| A.使用含氟牙膏可预防龋齿 |
| B.使用碳酸钠溶液处理锅炉水垢 |
C.实验室保存和配制 溶液时,加入 溶液时,加入 固体 固体 |
D.保存 溶液常在溶液中加铁粉 溶液常在溶液中加铁粉 |
您最近一年使用:0次



