名校
1 . 化学与生活,工业生产息息相关。下列有关说法错误的是
| A.明矾和漂白粉常用于自来水的处理,但二者作用的原理不同 |
| B.用硫酸清洗锅炉中的水垢(主要成分是碳酸钙) |
C.工业上常用 作沉淀剂除去废水中的 作沉淀剂除去废水中的 和 和 |
D.实验室盛放 溶液的试剂瓶应用橡皮塞,而不能用玻璃塞 溶液的试剂瓶应用橡皮塞,而不能用玻璃塞 |
您最近一年使用:0次
2023-12-12更新
|
399次组卷
|
3卷引用:辽宁省沈阳市第二中学2023-2024学年高二上学期第二次月考化学试题
名校
2 . 下列应用与盐类水解无主要关系的是
A. 不能用复分解反应的方法在溶液中制取,而只能用干法制备 不能用复分解反应的方法在溶液中制取,而只能用干法制备 |
B.用 溶液清洗油污时,加热可以增强去污效果 溶液清洗油污时,加热可以增强去污效果 |
C. 溶液制备 溶液制备 晶体时,不能直接蒸干结晶获取 晶体时,不能直接蒸干结晶获取 |
| D.实验室盛放硅酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞 |
您最近一年使用:0次
2023-12-12更新
|
123次组卷
|
2卷引用:天津市第四十七中学2023-2024学年高二上学期11月期中考试化学试题
24-25高二上·全国·假期作业
解题方法
3 . 在生产、生活和科学研究中,常常需要促进或抑制盐的水解。试回答下列问题:
(1) 溶液呈
溶液呈___________ (填“酸”“中”或“碱”)性,原因是(用离子方程式表示):___________ 。实验室在配制 溶液时,常将
溶液时,常将 固体先溶于较浓的盐酸中,以
固体先溶于较浓的盐酸中,以___________ (填“促进”或“抑制”)其水解,然后用蒸馏水稀释到所需的浓度。
(2)普通泡沫灭火器是利用 溶液跟
溶液跟 溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是
溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是___________ 。
(3)将 溶液加热蒸干所得主要固体为
溶液加热蒸干所得主要固体为________ ,灼烧所得到固体为________ 。
(1)
 溶液呈
溶液呈 溶液时,常将
溶液时,常将 固体先溶于较浓的盐酸中,以
固体先溶于较浓的盐酸中,以(2)普通泡沫灭火器是利用
 溶液跟
溶液跟 溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是
溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是(3)将
 溶液加热蒸干所得主要固体为
溶液加热蒸干所得主要固体为
您最近一年使用:0次
4 . Ⅰ.2022年2月4日至20日,北京冬季奥运会由北京市和河北省张家口市联合举办。手抄报、冰丝带、绿交通呼应中国碳达峰、碳中和的承诺。在节能减排措施上离不开化学元素与技术。
国家速滑馆“冰丝带”是北京冬奥会最具科技含量的场馆,它采用了当前冬季运动场馆最环保的制冰技术之一为二氧化碳跨临界直接制冰技术。

(1)CO2由气体变成固体的过程中,下列判断正确的是___________。
(2)关于CO2叙述不正确的是___________。
(3)为吸收CO2,下列处理CO2的转化关系不能 实现是___________。
Ⅱ.基于新材料及3D打印技术,科学家研制出的微胶囊吸收剂,它能将排放的CO2以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入(NH4)2CO3溶液,其原理如图所示。

已知:(NH4)2CO3(aq)+CO2(aq)+H2O(l) 2NH4HCO3(aq) ΔH=-25.3 kJ·mol-1
2NH4HCO3(aq) ΔH=-25.3 kJ·mol-1
(4)吸收CO2时宜选用___________ (选填“低温”或“高温”)理由 ___________ 、___________ (列举两点)。
(5)已知一水合氨和碳酸室温下电离平衡常数如下:
试结合电离平衡常数,判断并解释0.1 mol·L-1NH4HCO3溶液的酸碱性___________ 。
(6)吸收CO2过程中,胶囊内部溶液的n(NH )
)___________ (“增大”、“减小”、“几乎不变”),理由是___________ (不考虑其他副反应及溶液体积变化)。
Ⅲ.北京冬奥会全部场馆100%使用太阳能、氢能等清洁能源供电,着力打造“绿色冬奥”。冬奥会火炬“飞扬”,以氢气为燃料。氢燃料电池车则是北京冬奥会期间的交通服务用车。
(7)北京举办的两届奥运会火炬“飞扬”和“祥云”分别使用氢气和丙烷作为燃料
2022冬奥会“飞扬”:①2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ·mol-1
2008奥运会“祥云”:②C3H8(g)+5O2(g)=3CO2(g)+4H2O(g) ΔH=-2039kJ·mol-1
①常压下,单位质量燃料完全燃烧放出热量叫做该燃料的热值。热值:H2___________ C3H8(填写“大于”、“小于”或“等于”)
②试计算工业制备丙烷反应的焓变:3CO2(g)+10H2(g)=C3H8(g)+6H2O(g) ΔH=___________ 。
(8)冬奥会赛区内使用氢燃料清洁能源车辆,某氢氧燃料电池工作示意图如下,电解质溶液可分别使用氢氧化钾溶液和稀硫酸。使用不同电解质溶液时,有关说法不正确 的是___________

国家速滑馆“冰丝带”是北京冬奥会最具科技含量的场馆,它采用了当前冬季运动场馆最环保的制冰技术之一为二氧化碳跨临界直接制冰技术。

(1)CO2由气体变成固体的过程中,下列判断正确的是___________。
| A.ΔH>0,ΔS>0 | B.ΔH>0,ΔS<0 | C.ΔH<0,ΔS>0 | D.ΔH<0,ΔS<0 |
(2)关于CO2叙述不正确的是___________。
| A.CO2属于酸性氧化物 | B.CO2溶于水形成的溶液能导电 |
| C.CO2属于非电解质 | D.CO2是共价晶体 |
(3)为吸收CO2,下列处理CO2的转化关系
A.NaOH(aq) Na2CO3(aq) Na2CO3(aq) |
B.NaCl(aq) NaHCO3(s) NaHCO3(s) |
C.Ca(ClO)2(aq) CaCO3(s) CaCO3(s) |
D.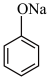 (aq) (aq) 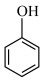 (aq) (aq) |
Ⅱ.基于新材料及3D打印技术,科学家研制出的微胶囊吸收剂,它能将排放的CO2以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入(NH4)2CO3溶液,其原理如图所示。

已知:(NH4)2CO3(aq)+CO2(aq)+H2O(l)
 2NH4HCO3(aq) ΔH=-25.3 kJ·mol-1
2NH4HCO3(aq) ΔH=-25.3 kJ·mol-1(4)吸收CO2时宜选用
(5)已知一水合氨和碳酸室温下电离平衡常数如下:
| 弱电解质 | H2CO3 | NH3·H2O |
| 电离平衡常数 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Kb=1.8×10-5 |
(6)吸收CO2过程中,胶囊内部溶液的n(NH
 )
)Ⅲ.北京冬奥会全部场馆100%使用太阳能、氢能等清洁能源供电,着力打造“绿色冬奥”。冬奥会火炬“飞扬”,以氢气为燃料。氢燃料电池车则是北京冬奥会期间的交通服务用车。
(7)北京举办的两届奥运会火炬“飞扬”和“祥云”分别使用氢气和丙烷作为燃料
2022冬奥会“飞扬”:①2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ·mol-1
2008奥运会“祥云”:②C3H8(g)+5O2(g)=3CO2(g)+4H2O(g) ΔH=-2039kJ·mol-1
①常压下,单位质量燃料完全燃烧放出热量叫做该燃料的热值。热值:H2
②试计算工业制备丙烷反应的焓变:3CO2(g)+10H2(g)=C3H8(g)+6H2O(g) ΔH=
(8)冬奥会赛区内使用氢燃料清洁能源车辆,某氢氧燃料电池工作示意图如下,电解质溶液可分别使用氢氧化钾溶液和稀硫酸。使用不同电解质溶液时,有关说法

| A.能量转化方式相同 |
| B.电极a均作负极 |
| C.电极b附近发生的电极反应相同 |
| D.转移等量电子,消耗氧气物质的量相等 |
您最近一年使用:0次
名校
解题方法
5 . 氧化还原反应不管在工业生产还是在日常生活中都随处可见,可以用于实现化学能到电能的转化,还可用于测定某一溶液的物质的量浓度。
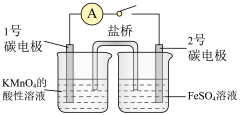
(1)已知当电路闭合后,左侧烧杯中溶液逐渐褪色,试使用半反应的形式解释原因___________ 。
(2)使用该装置时,有人发现右侧溶液在未闭合电路时已出现变色现象,试根据 的性质选择合适的溶液配制方法:
的性质选择合适的溶液配制方法:___________ 。

(1)已知当电路闭合后,左侧烧杯中溶液逐渐褪色,试使用半反应的形式解释原因
(2)使用该装置时,有人发现右侧溶液在未闭合电路时已出现变色现象,试根据
 的性质选择合适的溶液配制方法:
的性质选择合适的溶液配制方法:
您最近一年使用:0次
名校
解题方法
6 . 电子工业中,可用FeCl3-HCl溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
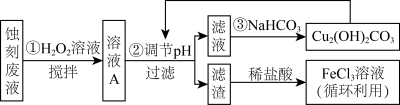
已知: Fe3+在溶液中会发生水解,当溶液呈酸性时可以抑制其水解
(1)步骤①中,为加快反应速率,除搅拌外,还可以___________ (任写一点)
(2)步骤②过滤中,用到的玻璃仪器,除烧杯外,还需要___________
(3)用FeCl3—HCl溶液刻蚀铜板时反应的离子方程式为___________ 。
(4)FeCl3蚀刻液中加入盐酸的目的是___________ 。
(5)步骤①中加入H2O2溶液的目的是(用离子方程式表示)___________ 。
(6)生成氢氧化物沉淀的pH如下表根据表中数据推测调节pH的范围是___________ 。
(7)上述流程路线中,除FeCl3溶液外,还可用于循环利用的物质是___________ 。

已知: Fe3+在溶液中会发生水解,当溶液呈酸性时可以抑制其水解
(1)步骤①中,为加快反应速率,除搅拌外,还可以
(2)步骤②过滤中,用到的玻璃仪器,除烧杯外,还需要
(3)用FeCl3—HCl溶液刻蚀铜板时反应的离子方程式为
(4)FeCl3蚀刻液中加入盐酸的目的是
(5)步骤①中加入H2O2溶液的目的是(用离子方程式表示)
(6)生成氢氧化物沉淀的pH如下表根据表中数据推测调节pH的范围是
| Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 4.7 | 7.0 | 1.9 |
| 沉淀完全时 | 6.7 | 9.0 | 3.2 |
(7)上述流程路线中,除FeCl3溶液外,还可用于循环利用的物质是
您最近一年使用:0次
名校
7 . 利用下列装置和试剂进行实验,设计合理且能达到实验目的的是
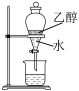 | 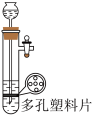 | 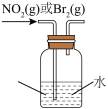 | 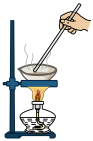 |
| A.分离乙醇和水 | B.用铜片与浓硫酸制取SO2 | C.鉴别Br2(g)和NO2(g) | D.蒸发MgCl2溶液,得到无水MgCl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-11更新
|
256次组卷
|
3卷引用:广西梧州高级中学2023-2024学年高二上学期期中考试化学试题
名校
8 . H2O2 是一种绿色氧化还原试剂,在化学研究中应用广泛。
Ⅰ.某研究性学习小组设计如图所示实验装置,探究影响H2O2分解反应速率的因素。

(1)用以上装置测定H2O2分解反应速率,需要测定实验数据是_______ (要求所测得的数据能直接体现反应速率大小)
(2)探究影响H2O2分解反应速率的因素实验方案如下表所示,先向锥形瓶中加入质量分数为10%的H2O2溶液,再依次通过分液漏斗向锥形瓶中加入一定量的蒸馏水和0.2 mol/LFeCl3溶液。
①通过实验Ⅱ、Ⅲ探究的是_______ 对反应速率影响。
②实验Ⅱ、Ⅲ中溶液颜色变为红褐色的原因是_______ 。
③向实验Ⅱ中反应后的溶液滴加KSCN溶液,溶液变红色,2 min后溶液红色褪去;继续滴加KSCN溶液,溶液又变红色,一段时间后又褪色,此时再向溶液中滴加盐酸酸化后的BaCl2溶液,产生白色沉淀,从平衡移动角度分析溶液红色褪去的原因_______ 。
Ⅱ.五氧化二氮是有机合成中常用的绿色硝化剂,常温下为白色固体,与水反应生成硝酸。某实验小组用滴定法测定N2O5粗品中N2O4的含量,具体操作为:取2.0 g粗品,加入20.00 mL0.1250mol/L酸性高锰酸钾溶液,充分反应后,用0.1000 mol/LH2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。(已知:H2O2 与HNO3不反应且不考虑其分解)
(3)产品中N2O4与KMnO4发生反应的离子方程式为_______ 。
(4)判断滴定终点的方法是_______ 。
(5)产品中N2O4的质量分数为_______ 。
Ⅰ.某研究性学习小组设计如图所示实验装置,探究影响H2O2分解反应速率的因素。

(1)用以上装置测定H2O2分解反应速率,需要测定实验数据是
(2)探究影响H2O2分解反应速率的因素实验方案如下表所示,先向锥形瓶中加入质量分数为10%的H2O2溶液,再依次通过分液漏斗向锥形瓶中加入一定量的蒸馏水和0.2 mol/LFeCl3溶液。
| 序号 | H2O2/mL | 蒸馏水/mL | FeCl3溶液/mL | 现象 |
| Ⅰ | 10 | a | 0 | 无明显变化 |
| Ⅱ | 10 | b | 2 | 锥形瓶变热,溶液迅速变红褐色,并有较多气泡产生;2 min时,反应变缓,溶液颜色明显变浅 |
| Ⅲ | 5 | 5 | 2 | 锥形瓶变热,溶液变红褐色,开始5 s后产生较少的气泡 |
②实验Ⅱ、Ⅲ中溶液颜色变为红褐色的原因是
③向实验Ⅱ中反应后的溶液滴加KSCN溶液,溶液变红色,2 min后溶液红色褪去;继续滴加KSCN溶液,溶液又变红色,一段时间后又褪色,此时再向溶液中滴加盐酸酸化后的BaCl2溶液,产生白色沉淀,从平衡移动角度分析溶液红色褪去的原因
Ⅱ.五氧化二氮是有机合成中常用的绿色硝化剂,常温下为白色固体,与水反应生成硝酸。某实验小组用滴定法测定N2O5粗品中N2O4的含量,具体操作为:取2.0 g粗品,加入20.00 mL0.1250mol/L酸性高锰酸钾溶液,充分反应后,用0.1000 mol/LH2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。(已知:H2O2 与HNO3不反应且不考虑其分解)
(3)产品中N2O4与KMnO4发生反应的离子方程式为
(4)判断滴定终点的方法是
(5)产品中N2O4的质量分数为
您最近一年使用:0次
名校
9 . Ⅰ.盐类水解知识。
(1)氯化铁水溶液呈___________ 性,原因是用离子方程式表示:___________ ;把 溶液蒸干,灼烧,最后得到的主要固体产物是
溶液蒸干,灼烧,最后得到的主要固体产物是___________ ;普通泡沫灭火器是利用溶液跟溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是:___________ 。
Ⅱ.已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(2)物质的量浓度均为 的四种溶液:pH
的四种溶液:pH由小到大 排列的顺序是___________ (用编号填写)
a. b.
b. c.NaClO d.
c.NaClO d.
(3)常温下,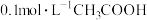 溶液加水稀释过程中,下列表达式的数据
溶液加水稀释过程中,下列表达式的数据变大 的是___________
A. B.
B. C.
C. D.
D. E.
E.
(4)25℃时,将 的醋酸与
的醋酸与 氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为
氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为___________ 。
(1)氯化铁水溶液呈
 溶液蒸干,灼烧,最后得到的主要固体产物是
溶液蒸干,灼烧,最后得到的主要固体产物是Ⅱ.已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
| 化学式 |  |  | HClO |
| 电离平衡常数 |  |   |  |
 的四种溶液:pH
的四种溶液:pHa.
 b.
b. c.NaClO d.
c.NaClO d.
(3)常温下,
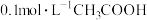 溶液加水稀释过程中,下列表达式的数据
溶液加水稀释过程中,下列表达式的数据A.
 B.
B. C.
C. D.
D. E.
E.
(4)25℃时,将
 的醋酸与
的醋酸与 氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为
氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为
您最近一年使用:0次
名校
解题方法
10 . 根据生活经验,判断下列物质按酸碱性的一定顺序依次排列正确的是
①洁厕灵(主要成分为 )②厨房清洁剂(主要成分为
)②厨房清洁剂(主要成分为 )③食醋④肥皂⑤食盐
)③食醋④肥皂⑤食盐
①洁厕灵(主要成分为
 )②厨房清洁剂(主要成分为
)②厨房清洁剂(主要成分为 )③食醋④肥皂⑤食盐
)③食醋④肥皂⑤食盐| A.①②⑤③④ | B.①③⑤④② | C.③①②⑤④ | D.④③⑤②① |
您最近一年使用:0次
2023-12-08更新
|
94次组卷
|
6卷引用:北京丰台区2018-2019学年高二下学期期末考试化学试题
北京丰台区2018-2019学年高二下学期期末考试化学试题河北省张家口市第一中学2019-2020学年高二上学期期中考试(实验班)化学试题辽宁省凌源市第三中学2019-2020学年高二下学期第一次月考化学试题北京市清华大学附属中学2023-2024学年高二上学期第三单元化学统练(已下线)寒假作业06 盐类的水解-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)河北省保定市高碑店市崇德实验中学2023-2024学年高二上学期1月考试化学试题



