1 . 氯水具有漂白和杀菌作用.下列浓度关系正确的是
A.氯水中: |
B.氯水中: |
C.氯水中: |
D.等体积等浓度的次氯酸钠溶液与次氯酸溶液混合后,溶液呈碱性: |
您最近一年使用:0次
名校
2 . 向NaOH和NaAlO2混合溶液中滴加NaHCO3溶液,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积的变化情况如图所示。下列说法不正确 的是
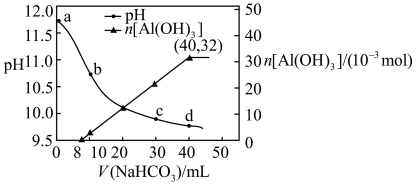

| A.加入的NaHCO3先与NaOH反应 |
B.b点和c点均有c(Na+)<2c(CO )+c(HCO )+c(HCO ) ) |
| C.NaHCO3溶液的物质的量浓度为1.125mol/L |
D.d点时:c(Na+)=2c(CO )+2c(HCO )+2c(HCO )+2c(H2CO3) )+2c(H2CO3) |
您最近一年使用:0次
2020-10-09更新
|
299次组卷
|
6卷引用:广东省佛山市顺德区容山中学2021届高三10月月考化学试题
名校
解题方法
3 . 用亚硫酸盐(X)吸收烟气中的SO2。已知吸收过程中含硫组分物质的量分数(δ)与溶液pH的变化关系如下图所示。下列说法中不正确 的是


A.若X为Na2SO3,当吸收液pH=1.85时:c(Na+)=c( )+c(H2SO3) )+c(H2SO3) |
B.若X为Na2SO3,当吸收液呈中性时:2c( )+c( )+c( )=c(Na+) )=c(Na+) |
C.若X为 (NH4)2SO3,(NH4)2SO3溶液呈碱性,说明水解程度: > > |
D.若X为 (NH4)2SO3,图中b点溶液中n( )∶n( )∶n( )= 1∶3 )= 1∶3 |
您最近一年使用:0次
2020-08-06更新
|
522次组卷
|
10卷引用:广东省佛山市李兆基中学、郑裕彤中学两校2021-2022学年高三下学期3月联考化学试题
广东省佛山市李兆基中学、郑裕彤中学两校2021-2022学年高三下学期3月联考化学试题甘肃省兰州市第一中学2020届高三冲刺模拟考试(二)理科综合化学试题(已下线)第25讲 盐类水解(精练)-2022年高考化学一轮复习讲练测湖南省怀化市沅陵县第一中学2021-2022学年高三下学期期中考试化学试题(已下线)押新高考卷13题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(新高考通版)上海市黄浦区联合体2021-2022学年高二下学期联合体期末模拟考试化学试题北京市北京师范大学附属实验中学2022-2023学年高三上学期月考化学试题湖北省圆创联考2021-2022学年高三下学期第二次联合测评化学试题陕西省西安市蓝田县部分学校联考2023-2024学年高二上学期11月期中化学试题湖南省岳阳市岳阳县第一中学2023-2024学年高三下学期3月月考化学试题
名校
解题方法
4 . 常温下,用 的盐酸滴定
的盐酸滴定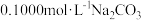 溶液
溶液 。用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是
。用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是

 的盐酸滴定
的盐酸滴定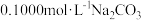 溶液
溶液 。用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是
。用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是 
A.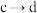 发生的主要离子反应: 发生的主要离子反应: |
B.在b点时, |
C.在d点时, |
D.在e点时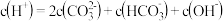 |
您最近一年使用:0次
2019-12-27更新
|
198次组卷
|
3卷引用:广东省佛山市第一中学2021-2022学年高三上学期10月月考化学试题
名校
5 . 电解质的电导率越大,导电能力越强。用0.100mol·L-1的KOH溶液分别滴定体积均为20.00mL、浓度均为0.100mol•L-1的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是( )
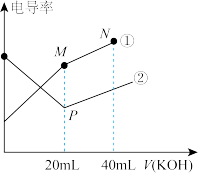

| A.曲线②代表滴定CH3COOH溶液的曲线 |
| B.在相同温度下,P点水电离程度大于M点 |
| C.M点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1mol·L-1 |
| D.N点溶液中:c(K+)>c(OH-)>c(CH3COO-)>c(H+) |
您最近一年使用:0次
2019-06-21更新
|
1609次组卷
|
11卷引用:广东省佛山市石门中学2021届高三模拟化学试题
广东省佛山市石门中学2021届高三模拟化学试题【全国百强校】广东省深圳外国语学校2017-2018学年高二上学期期中化学试题河北省衡水中学2020届高三下学期一调理综化学试题天津市第二十五中学2020届高三下学期3月网络测试化学试题(已下线)考点12 盐类水解及其应用-2020年高考化学命题预测与模拟试题分类精编新疆维吾尔自治区新源县第二中学2020届高三下学期第一次测试化学试题解题达人.化学选择题(2021全国卷)精编特训04内蒙古赤峰二中2021-2022学年高三上学期第一次月考化学试题江西省临川一中暨临川一中实验学校2021-2022学年高二上学期期末考试化学试题四川省遂宁市高2023届高三零诊考试化学试题湖南省名校联盟2023届高三下学期3月调研考试化学试题
名校
6 . 下列说法正确的是
| A.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |
| B.一定量的(NH4)2SO4溶液与NH3·H2O混合所得的酸性溶液中:c(NH4+)<2c(SO42-) |
| C.物质的量浓度均为0.01 mol/L的CH3COOH和CH3COONa溶液等体积混合后所得溶液中:c(CH3COOH)+c(CH3COO-)=0.02 mol/L |
| D.物质的量浓度相等的①NH4HSO4溶液②NH4HCO3溶液③NH4Cl溶液中c(NH4+)的大小关系:①>②>③ |
您最近一年使用:0次
2019-02-26更新
|
338次组卷
|
3卷引用:广东省佛山市第一中学2021-2022学年高二上学期第二次段考化学试题
真题
名校
7 . 在25℃时将pH=11 的NaOH 溶液与pH=3 的CH3COOH溶掖等体积混合后,下列关系式中正确的是
| A.c(Na+)=c(CH3COO-)+c(CH3COOH) |
| B.c(H+)==c(CH3COO-)+c(OH一) |
| C.c(Na+) >c(CH3COO-)>c(OH-)>c(H+) |
| D.c (CH3COO-)>c(Na+)>c(H+)>c(OH-) |
您最近一年使用:0次
2019-01-30更新
|
1825次组卷
|
51卷引用:2011届广东省佛山一中等三校高三2月联考理综化学部分
(已下线)2011届广东省佛山一中等三校高三2月联考理综化学部分2007年普通高等学校招生全国统一考试(四川卷)理综化学部分(已下线)2011-2012年黑龙江省鹤岗一中高二上学期期中考试化学试卷(已下线)2011-2012学年河南省卫辉市第一中学高二上学期期中考试化学试卷(已下线)2011-2012学年度北京五中高三第一学期期中考试化学试卷(已下线)2011—2012学年福建省漳州市芗城中学高二上学期期末考试化学试卷(已下线)2012届海南省琼海市高考模拟测试(一)化学试卷(已下线)2011-2012年陕西宁强天津中学高二下学期期中考试化学试卷(已下线)2011-2012学年湖北省武汉市四校高二上学期期中考试化学试卷(已下线)2011-2012学年海南省海南中学高二1班下学期期末考试化学试卷(已下线)2012-2013学年吉林省长春二中高二上学期期末考试化学试卷(已下线)2014年高中化学鲁科版选修四第3章 物质在水溶液中的行为练习卷(已下线)2013-2014四川省宜昌市部分市级示范高中春季期中考试高二化学试卷(已下线)2013-2014广西柳州高中高二上学期段考化学试卷(已下线)2013-2014福建省三明一中下学期期中考试高二化学试卷2014-2015福建省三明一中高二上学期第二次月考化学试卷2014-2015湖南省娄底市湘中名校高二上学期期末化学(理)试卷2016届山东省枣庄八中南校区高三上学期10月阶段测化学试卷2015-2016学年河北省永年县第二中学高二上学期12月月考化学试卷2015-2016学年山西省忻州一中高二上学期期末理化学试卷2015-2016学年福建省漳州一中高二上学期期末化学试卷2016-2017学年河南省郏县一高、叶县二高等五校高二上期中化学卷2016-2017学年内蒙古包头一中高二上学期期中化学试卷陕西省咸阳市西藏民族学院附中2016-2017学年高二12月月考化学卷2016-2017学年河北省涿鹿县涿鹿中学高二上调研三化学卷湖北省孝感市七校教学联盟2016-2017学年高二下学期期末考试化学试题河南省焦作市博爱县第一中学2018届高三上学期收心考试化学试题江西省临川第二中学2017-2018学年高二上学期期中考试化学试题河南省鹤壁市淇滨高级中学2017-2018学年高二上学期第三次月考化学试题甘肃省武威市第一中学2017-2018学年度第一学期 高二化学期末试卷重庆市巫溪县中学校2017-2018学年高二上学期第二次月考化学试题河北省永年县第二中学2017-2018学年高二12月月考化学试题宁夏青铜峡市高级中学2017-2018学年高二上学期期末考试化学试题人教版高二化学选修4 第三章离子浓度大小比较重点难点专题辽宁省普兰店市第一中学2018-2019学年高二(理)上学期期中考试化学试题福建省莆田市第二十五中学2018-2019学年高二下学期第一次月考化学试题上海市复旦中学2019-2020学年高二上学期第一次月考化学试题安徽省滁州市定远县育才学校2019-2020学年高二上学期期末考试(普通班)化学试题四川省绵阳南山中学2019-2020学年高二下学期期中考试化学试题上海市格致中学2020届高三上学期12月月考化学试题湖南省五市十校2020-2021学年高二上学期第一次联考化学试题宁夏海原第一中学2020-2021学年高二上学期第二次月考化学试题湖北省应城市第一高级中学2020—2021学年高二12月月考化学试题河北省任丘市第一中学2020-2021学年高二上学期第二次阶段考试化学试题四川省遂宁市射洪中学2020—2021学年高二下学期期中考试化学试题内蒙古集宁新世纪中学2020-2021学年高二下学期质量检测月考化学试题上海市晋元高级中学2020-2021学年高三上学期期中考试(等级考)化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期第四次教学质量检测化学试题(已下线)3.3.4 溶液中的粒子浓度(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)专题20 用守恒思想破解溶液中粒子浓度大小的比较-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)第3课时 溶液中粒子浓度的大小比较
真题
名校
8 . 室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
下列判断不正确的是
| 实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
下列判断不正确的是
| A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+) |
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)= mol/L mol/L |
| C.实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1 |
| D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+) |
您最近一年使用:0次
2019-01-30更新
|
2820次组卷
|
36卷引用:2016届广东省佛山市顺德六校高三上学期期中理综化学试卷
2016届广东省佛山市顺德六校高三上学期期中理综化学试卷2013年全国普通高等学校招生统一考试理科综合能力测试化学(四川卷)(已下线)2014届四川省成都市高三第二次诊断考试理综化学试卷(已下线)2014高考名师推荐化学盐类水解的概念与离子浓度大小比较(已下线)2013-2014天津市天津一中高三上学期第二次月考化学试卷(已下线)2013-2014云南省玉溪一中高二下学期第二次月考化学试卷(已下线)2014-2015学年吉林省实验中学高二上学期模块一测试化学试卷(已下线)2014-2015四川省成都七中高三上期期中理综化学试卷2015-2016学年河南省许昌市三校高二下第四次联考化学试卷(已下线)同步君 选修4 第3章 第3节 盐类水解的影响因素2016-2017学年四川省简阳市高二上学期期末化学试卷2017届辽宁省抚顺市高三3月模拟考试理科综合化学试卷北京市朝阳外国语学校2018届高三9月月考化学试题高中化学人教版 选修四 第三章 水溶液中的离子反应 第三节 盐类的水解 盐类的水解第二课时(盐类的水解的影响因素和应用)2018-2019学年鲁科版高中化学选修四:第3章检测题山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题(已下线)2019年4月11日 《每日一题》三轮复习——离子浓度大小比较类试题苏教版选修四化学反应原理专题3第三单元 盐类的水解 同步检测试卷宁夏育才中学孔德学区2019-2020学年高二上学期第二次月考化学试题云南省玉溪第一中学2019-2020学年高二上学期第二次月考化学试题山西省太原市实验中学2019-2020学年高二12月月考化学试题安徽省黄山市2019-2020学年高二上学期期末质量检测 化学(理)试题湖北省黄冈市黄梅国际育才高级中学2019-2020学年高二上学期期中考试化学试题安徽省合肥市第一中学2019-2020学年高二上学期段二(期中)考试化学试题鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第2节 弱电解质的电离盐类的水解人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第三节 盐类的水解 作业帮鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时4 溶液中粒子浓度的大小关系(已下线)练习11 盐类的水解-2020-2021学年【补习教材·寒假作业】高二化学(人教版)河北省石家庄市辛集市第一中学2020-2021学年高二月考第四次考试(一)化学试题(已下线)第三章第三节 盐类的水解(第2课时 影响盐类水解的主要因素和盐类水解的利用)(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)(已下线)3.3.2 溶液中离子浓度大小的比较-同步学习必备知识湖北省十堰市汉江中学2021-2022学年高二上学期期中考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第50练 溶液中“粒子”浓度关系3.3.3盐类水解的应用 课后(已下线)微专题 溶液中“粒子”浓度关系河南省济源第一中学2022-2023学年高二上学期11月月考 化学试题
9 . 常温下,向20mL0.1moL/L的H3PO4溶液中滴加0.1moL/L的 NaOH溶液,所得溶液的pH与NaOH溶液体积的关系如图所示,下列说法正确的是


| A.H3PO4溶液第一步滴定可用酚酞作指示剂 |
| B.A点溶液中c(H2PO4-)>c(H3PO4)>c(HPO42-) |
C.图象中A、B、C三处溶液中 相等 相等 |
| D.B点溶液存在2c(Na+)=c(PO43-)+c(H2PO4-)+c(HPO42-)+c(H3PO4) |
您最近一年使用:0次
2019-01-14更新
|
817次组卷
|
2卷引用:【市级联考】广东佛山市2019届高三上学期普通髙中教学质量检测(一)理科综合化学试题
名校
解题方法
10 . 乙二胺(H2NCH2CH2NH2) 与NH3相似,水溶液呈碱性,25℃时,向10mL0.1mol·L-1乙二胺溶液中滴加0.1 mol·L-1盐酸,各组分的物质的量分数δ随溶液pH的变化曲线如图所示,下列说法错误的是
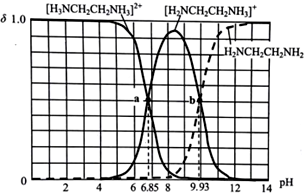

| A.混合溶液呈中性时,滴加盐酸的体积小于10mL |
| B.Kb2[H2NCH2CH2NH2] 的数量级为10-8 |
| C.a 点所处的溶液中:c(H+)+3c([H3NCH2CH2NH3]2+)=c(OH-) +(Cl-) |
| D.水的电离程度:a>b |
您最近一年使用:0次
2018-04-21更新
|
2379次组卷
|
2卷引用:广东省佛山市2018届高三普通高中教学质量检测(二)理科综合化学试题



