名校
解题方法
1 . X是合成碳酸二苯酯的一种有效的氧化还原催化助剂,可由EDTA与Fe3+反应得到。
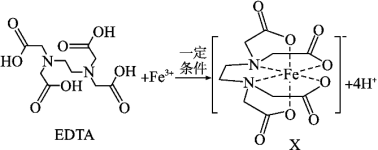
(1)基态Si原子的价层电子的运动状态有_______ 种,若其电子排布式表示为[Ne]3s2 违背了
违背了_______ 。
(2)EDTA中碳原子杂化轨道类型为_______ ,EDTA中四种元素的电负性由小到大的顺序为_______ 。C、N、O第一电离能由小到大的顺序为_______ 。
(3)Fe3+基态价层电子排布式为_______ 。
(4)EDTA与正二十一烷的相对分子质量非常接近,但EDTA的沸点比正二十一烷的沸点高的原因是_______ 。
(5)设NA代表阿伏加德罗常数的值,1mol碳酸分子中含有σ键的数目为_______ 。

(1)基态Si原子的价层电子的运动状态有
 违背了
违背了(2)EDTA中碳原子杂化轨道类型为
(3)Fe3+基态价层电子排布式为
(4)EDTA与正二十一烷的相对分子质量非常接近,但EDTA的沸点比正二十一烷的沸点高的原因是
(5)设NA代表阿伏加德罗常数的值,1mol碳酸分子中含有σ键的数目为
您最近一年使用:0次
名校
2 . 磷酸锌常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰(主要含ZnO,还含少量FeO、Al2O3、CuO及SiO2)为原料制取磷酸锌的工艺流程如图所示:
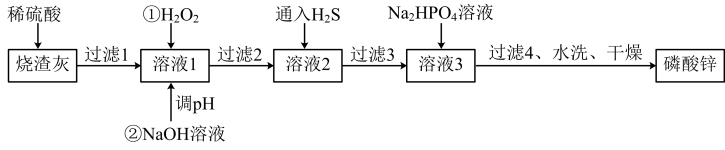
已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
(1)基态Zn原子的价电子排布式为______
(2)用硫酸浸烧渣灰,为提高酸浸时锌的浸出率,可以采取的措施是______ (填一条)。
(3)加入H2O2的作用_______
(4)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是______ 。
(5)加入Na2HPO4溶液发生反应的离子方程式为_____ 。
(6)洗涤磷酸锌沉淀时应选用____ (填“冷水”或“热水”),确认磷酸锌洗涤干净的操作是_____ 。
(7)通入H2S是为了除铜离子,25°C时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1mol·L-1,此时溶液中c(Cu2+)=6.3×10-15mol·L-1,则CuS的溶度积Ksp=______ (已知:25°C时,H2S的电离平衡常数Ka1=1×10-7,Ka2=1×10-15)。

已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4 | 6.5 |
| 完全沉淀的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(2)用硫酸浸烧渣灰,为提高酸浸时锌的浸出率,可以采取的措施是
(3)加入H2O2的作用
(4)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是
(5)加入Na2HPO4溶液发生反应的离子方程式为
(6)洗涤磷酸锌沉淀时应选用
(7)通入H2S是为了除铜离子,25°C时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1mol·L-1,此时溶液中c(Cu2+)=6.3×10-15mol·L-1,则CuS的溶度积Ksp=
您最近一年使用:0次
2022-08-25更新
|
490次组卷
|
3卷引用:云南师范大学附属中学2022-2023学年高三上学期高考适应性月考卷(二)理科综合化学试题
解题方法
3 . 已知短周期元素X、Y、Z、W、Q和R在周期表中的相对位置如图所示,X能与W形成两种常见的离子化合物,阴阳离子个数比均为1∶2。回答下列问题:
(1)化合物XR的电子式为____ 。
(2)基态W原子的最外层有____ 个未成对电子。
(3)Z单质与Q的最高价氧化物对应水化物的浓溶液在加热条件下反应的化学方程式为____ 。
(4)Y在Z的最高价氧化物中燃烧的化学方程式为____ 。
| Z | W | |||||
| X | Y | Q | R |
(2)基态W原子的最外层有
(3)Z单质与Q的最高价氧化物对应水化物的浓溶液在加热条件下反应的化学方程式为
(4)Y在Z的最高价氧化物中燃烧的化学方程式为
您最近一年使用:0次
4 . 短周期元素X、Y、Q、R、W原子最外层电子数与原子序数的关系如图所示。下列说法错误的是
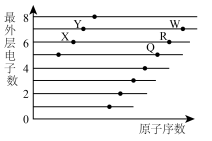

| A.X元素位于元素周期表p区 |
| B.简单氢化物的沸点:X>Y>R |
| C.第一电离能:W>R>Q |
| D.最高价氧化物对应水化物的酸性:W>R |
您最近一年使用:0次
2022-08-22更新
|
115次组卷
|
2卷引用:云南省昆明市五华区2023届高三教学质量摸底检测化学试题
名校
5 . Ⅰ.双氰胺结构简式如图。
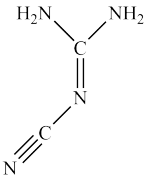
(1)双氰胺的晶体类型为_______ 。
(2)双氰胺所含元素中,_______ (填元素名称)元素基态原子核外未成对电子数最多。
(3)双氰胺分子中σ键和π键数目之比为_______ 。
Ⅱ.硼的最简单氢化物——乙硼烷球棍模型如下图,由它制取硼氢化锂的反应为2LiH+B2H6=2LiBH4
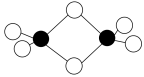
(4)乙硼烷分子中硼原子的杂化轨道类型为_______ 。
(5)BH 为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为
为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为_______ (填序号)。
A.离子键 B.金属键 C.氢键 D.配位键 E.极性键 F.非极性键
(6)根据以上反应判断,其中涉及元素的电负性从小到大的顺序为_______ (填元素符号)。
(7)碳的最简单氢化物是CH4,而硼的最简单氢化物不是BH3,其原因为_______ 。

(1)双氰胺的晶体类型为
(2)双氰胺所含元素中,
(3)双氰胺分子中σ键和π键数目之比为
Ⅱ.硼的最简单氢化物——乙硼烷球棍模型如下图,由它制取硼氢化锂的反应为2LiH+B2H6=2LiBH4

(4)乙硼烷分子中硼原子的杂化轨道类型为
(5)BH
 为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为
为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为A.离子键 B.金属键 C.氢键 D.配位键 E.极性键 F.非极性键
(6)根据以上反应判断,其中涉及元素的电负性从小到大的顺序为
(7)碳的最简单氢化物是CH4,而硼的最简单氢化物不是BH3,其原因为
您最近一年使用:0次
名校
解题方法
6 . 原子序数依次增大的四种元素A、B、C、D分别处于第1~4周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D原子外围电子排布为3d104s1。请回答下列问题:
(1)这四种元素中电负性最大的是____ (填元素符号,下同),第一电离能最小的是____ 。
(2)C所在的主族元素气态氢化物中,沸点最低的是____ (填化学式)。
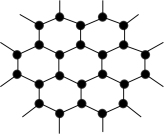
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为____ 。
(4)D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是____ (填选项序号)。

①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如图:
D单质 棕色的烟
棕色的烟 绿色溶液
绿色溶液 蓝色沉淀
蓝色沉淀 蓝色溶液
蓝色溶液 黑色沉淀
黑色沉淀
请书写第⑤步反应的离子方程式:____ 。
(1)这四种元素中电负性最大的是
(2)C所在的主族元素气态氢化物中,沸点最低的是
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为

(4)D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是

①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如图:
D单质
 棕色的烟
棕色的烟 绿色溶液
绿色溶液 蓝色沉淀
蓝色沉淀 蓝色溶液
蓝色溶液 黑色沉淀
黑色沉淀请书写第⑤步反应的离子方程式:
您最近一年使用:0次
7 . 同周期有下列电子排布式的原子中,第一电离能最小的是
| A.ns2np3 | B.ns2np4 |
| C.ns2np5 | D.ns2np6 |
您最近一年使用:0次
2022-07-26更新
|
453次组卷
|
46卷引用:2012届云南省玉溪一中高三上学期中考试理科综合试题(化学部分)
(已下线)2012届云南省玉溪一中高三上学期中考试理科综合试题(化学部分)山东济宁市兖州区2020届高三网络模拟考试化学试题(已下线)《2020年新高考政策解读与配套资源》2020年山东新高考化学全真模拟卷(四)菏泽一中2020届高三3月份化学质量检测肥城一中2020届高三3月份在线检测化学试题山东省青岛58中2020届高三3月化学模拟考试试题(已下线)课时54 原子结构与性质-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第38练 原子结构与元素的性质-2023年高考化学一轮复习小题多维练(全国通用)(已下线)2010年内蒙古赤峰市田家炳中学高二上学期期中考试化学试卷(已下线)2011-2012学年新疆喀什二中高一下学期第一次月考检测化学试卷(已下线)2011-2012学年新疆农七师高中高二下学期第二阶段考试化学试卷(已下线)2011-2012学年福建省上杭一中高二下学期期末考试化学试卷(已下线)2012-2013学年辽宁省沈阳二中高二下学期期中考试化学试卷2014-2015黑龙江省哈尔滨六中高二上期末化学试卷2015-2016学年四川省雅安市天全中学高二9月月考化学试卷(已下线)同步君 选修3 第一章 第二节 元素周期律江苏省江阴市四校2016-2017学年高二下学期期中考试化学试题陕西省黄陵中学2016-2017学年高二(重点班)下学期第三学月考化学试题广西宾阳县宾阳中学2016-2017学年高二下学期7月期末考试化学试题高中化学人教版 选修三 第1章 原子结构与性质 元素周期律【全国市级联考】山东省菏泽市2017-2018学年高二下学期期中考试(B卷)化学试题贵州省普定县一中2018-2019学年高二上学期期中考试化学试题甘肃省武威市第十八中学 2017-2018学年高二下学期期中考试化学试题福建省罗源市第一中学2018-2019学年高二下学期3月月考化学试题黑龙江省大庆市三校联考2018-2019学年高二下学期期末考试化学试题广西壮族自治区蒙山县第一中学2019-2020学年高二下学期期末考试化学试题广西蒙山一中2018-2019学年高二下学期期末考试化学试题人教化学选修3第一章第二节课时6辽宁省丹东市2018-2019学年高二下学期期末质量监测化学试题吉林省辽源市田家炳高级中学等友好学校2019-2020学年高二下学期期末考试化学试题湖北新高考联考协作体2019-2020学年高二下学期期末考试化学试卷河北省唐山市路北区第十一中学2019-2020学年高二下学期期末考试化学试题黑龙江省哈尔滨市第六中学2020-2021学年高二上学期期末考试化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质 课时2 元素周期律——原子半径、电离能、电负性的递变规律鲁科版2019选择性必修2第1章 原子结构与元素性质 第3节 元素性质及其变化规律 第1课时 原子半径 元素的电离能(人教版2019)选择性必修2第一章 原子结构与性质 第二节 原子结构与元素的性质 第2课时 原子半径、元素的电离能及其变化规律(已下线)模块同步卷02 原子结构与元素的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)河北省元氏县第四中学2020-2021学年高二上学期期末考试化学试题河南省汤阴县五一中学2019-2020学年高二下学期期中考试化学试题江苏省泗阳县众兴中学2020-2021学年高二上学期10月月考化学试题广西蒙山县第一中学2018-2019学年高二下学期第二次月考化学试题江苏省泗阳县实验高级中学2021-2022学年高二上学期第一次质量调研化学试题福建省莆田第十五中学2021-2022学年高二下学期期中考试化学试题河北省沧州市东光县等三县联考2022-2023学年高二下学期4月月考化学试题陕西省西安市铁一中学2022-2023学年高二下学期4月期中考试化学试题河南省焦作市2022-2023学年第四中学高二下学期3月月考 化学试卷
名校
解题方法
8 . 下列说法正确的是
| A.H3O+的空间结构:平面三角形 | B.冰中的氢键示意图: |
C.基态氧原子价电子排布图: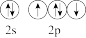 | D.基态Cr原子电子排布式:[Ar]3d44s2 |
您最近一年使用:0次
2022-07-07更新
|
298次组卷
|
3卷引用:云南省玉溪第一中学2023届高三上学期开学考试化学试题
9 . A、B、C、D、E、F是6种原子序数依次增大的前四周期元素,部分元素性质或原子结构如下:
(1)E元素的基态原子的核外电子排布式为_______ 。
(2)用电子式表示化合物DC2的形成过程:_______ 。
(3)A、B、C三种元素简单氢化物的沸点由高到低的顺序为_______ (用化学式表示)。
(4)F元素的单质与A元素的最高价氧化物对应水化物的稀溶液反应的化学方程式为_______ 。
| 元素 | 元素性质或原子结构 |
| A | 基态原子价层电子排布为nsnnpn+1 |
| C | 元素周期表中电负性最大的元素 |
| D | 原子核外有三个电子层,且最外层电子数是核外电子总数的 |
| E | E3+的3d轨道为半充满状态 |
| F | 基态原子的M层全充满,N层只有一个电子 |
(2)用电子式表示化合物DC2的形成过程:
(3)A、B、C三种元素简单氢化物的沸点由高到低的顺序为
(4)F元素的单质与A元素的最高价氧化物对应水化物的稀溶液反应的化学方程式为
您最近一年使用:0次
2022-07-01更新
|
288次组卷
|
2卷引用:云南师范大学附属中学2023届高考适应性月考卷(一)化学试题
名校
10 . 下列化学用语表达正确的是
| A.乙烯的结构简式: CH2CH2 |
B.Cl-的结构示意图: |
C.乙醇中官能团的电子式: |
| D.基态碘原子的简化电子排布式: [ Kr ]5s25p5 |
您最近一年使用:0次
2022-07-01更新
|
641次组卷
|
3卷引用:云南师范大学附属中学2023届高考适应性月考卷(一)化学试题



