名校
1 . 现有A、B、C、D四种元素,A是第五周期第ⅣA族元素,B是第三周期元素,B、C、D的价电子数分别为2、2、7。四种元素原子序数从小到大的顺序是B、C、D、A。已知C和D的次外层电子数均为18个。
(1)写出A、B、C、D的元素符号:A________ 、B________ 、C________ 、D________ 。
(2)C位于元素周期表的________ 区,C2+的电子排布式______________________________ 。
(3)最高价氧化物对应水化物中碱性最强的化合物是________ (写化学式,下同);最高价氧化物对应水化物中酸性最强的化合物是________ 。
(4)元素的第一电离能最小的是________ ,元素的电负性最大的是________ 。
(1)写出A、B、C、D的元素符号:A
(2)C位于元素周期表的
(3)最高价氧化物对应水化物中碱性最强的化合物是
(4)元素的第一电离能最小的是
您最近一年使用:0次
2019-07-22更新
|
316次组卷
|
10卷引用:云南省丘北二中2018-2019学年高二下学期期末考试化学试题
云南省丘北二中2018-2019学年高二下学期期末考试化学试题云南省富宁县三中2019-2020学年高二上学期期末考试化学试题云南省楚雄州南华县第一中学2019-2020学年高二9月考试化学试题(已下线)2019年11月23日 周末培优-学易试题君之每日一题君2020年高考化学一轮复习云南省玉溪市江川二中2019-2020学年高二上学期期中考试化学试题云南省禄丰县民族中学2019-2020学年高二12月月考化学试题云南省屏边县民族中学2019-2020学年高二上学期12月月考化学试题云南省元阳县第三中学2019-2020学年高二上学期期末考试化学试题云南省施甸县第三中学2019-2020学年高二12月月考化学试题安徽省合肥市第一中学2022-2023学年高二下学期第一次质量检测化学试题
解题方法
2 . 卤族元素是典型的非金属元素,包括F,Cl,Br,I等.请回答下面有关问题:
(1)同主族元素的电负性大小存在一定的规律,卤族元素F,Cl,Br,I的电负性由小到大 的顺序是_______ ;
(2)Br原子的核外电子排布式为_______ ;
(3)用价层电子对互斥理论判断BeCl2的构型为_______ ,BF3分子中B﹣F键的键角为_______ ;
(4)CCl4分子中碳原子的杂化方式为_______ ,NF3分子的空间构型为_______ ;
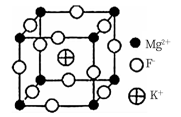
(5)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中 Mg元素的质量分数为_______ 。
(1)同主族元素的电负性大小存在一定的规律,卤族元素F,Cl,Br,I的电负性由小到大 的顺序是
(2)Br原子的核外电子排布式为
(3)用价层电子对互斥理论判断BeCl2的构型为
(4)CCl4分子中碳原子的杂化方式为
(5)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中 Mg元素的质量分数为

您最近一年使用:0次
名校
解题方法
3 . 有A、B、C、D四种元素,其中A元素是1826年一位法国青年科学家发现的,他在研究海水制盐时向剩余的副产物(苦卤)中通入氯气后发现溶液的颜色变深,经过一步提取可得红棕色液体,有刺激性气味;B、C、D的核外电子层数不超过3个,D原子核内的质子数正好等于C原子核内质子数的2倍,而它们的最外层电子数相等;D原子的最内层电子数是B原子核外电子数的2倍。回答下列问题:
(1)四种元素分别为A._____ 、B.____ 、C._____ 、D._____ 。
(2)A原子的电子排布式为________ ,D原子的原子结构示意图为______ 。
(3)写出由上述元素组成的单质和化合物相互作用生成沉淀的两个化学方程式________ 、_______ 。
(1)四种元素分别为A.
(2)A原子的电子排布式为
(3)写出由上述元素组成的单质和化合物相互作用生成沉淀的两个化学方程式
您最近一年使用:0次
2019-07-01更新
|
157次组卷
|
2卷引用:云南省文山州第一中学2021-2022学年高二下学期3月份考试化学试题
名校
4 . 下列叙述不正确的是( )
| A.在多电子原子里,核外电子的能量不同 |
| B.原子核外的电子按其能量不同分层排布 |
| C.电子的能量越低,运动区域离核越远 |
| D.M层电子的能量大于L层电子的能量 |
您最近一年使用:0次
2019-06-20更新
|
584次组卷
|
8卷引用:云南省文山州马关县第一中学2018-2019学年高一6月份考试化学试题
名校
解题方法
5 . 主族元素A和B形成AB2的离子化合物,则A、B两原子价电子排布分别为( )
| A.ns2和ns2np4 | B.ns1和ns2np4 | C.ns2和ns2np5 | D.ns1和ns2 |
您最近一年使用:0次
2019-05-06更新
|
78次组卷
|
6卷引用:云南省广南县二中2021-2022年学年高二下学期开学考试化学试题
真题
名校
6 . 硅是重要的半导体材料,构成了现代电子工业的基础。请回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为________ 、电子数为___________ 。
(2)硅主要以硅酸盐、___________ 等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以___________ 相结合,其晶胞中共有8个原子,其中在面心位置贡献__________ 个原子。
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为___________________________________ 。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是______ 。
②SiH4的稳定性小于CH4,更易生成氧化物,原因是___________________________ 。
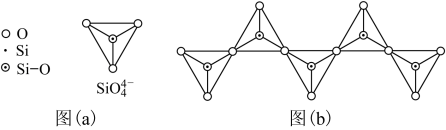
(6)在硅酸盐中,SiO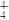 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为______ ,Si与O的原子数之比为_________ ,化学式为__________________ 。
(1)基态Si原子中,电子占据的最高能层符号为
(2)硅主要以硅酸盐、
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C—C | C—H | C—O | Si—Si | Si—H | Si—O |
| 键能/(kJ•mol-1 | 356 | 413 | 336 | 226 | 318 | 452 |
②SiH4的稳定性小于CH4,更易生成氧化物,原因是
(6)在硅酸盐中,SiO
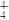 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
您最近一年使用:0次
2019-01-30更新
|
3772次组卷
|
9卷引用:云南省广南县第三中学校2019-2020学年高二上学期期末考试化学试题
12-13高二下·辽宁葫芦岛·期中
名校
7 . 生活中的下列现象与原子核外电子发生跃迁有关的是
| A.节日里燃放的焰火 | B.钢铁长期使用后生锈 |
| C.金属导线可以导电 | D.卫生球久置后消失 |
您最近一年使用:0次
2019-01-30更新
|
1037次组卷
|
18卷引用:云南省广南县二中2021-2022年学年高二下学期开学考试化学试题
云南省广南县二中2021-2022年学年高二下学期开学考试化学试题(已下线)2012-2013学年辽宁葫芦岛第一高级中学高二下学期期中考试化学试卷(已下线)2012-2013学年黑龙江省牡丹江一中高二下学期期末考试化学试卷2014-2015福建省福州市八县高二下学期联考化学试卷【全国百强校】江苏省启东中学2018-2019学年高一(创新班)下学期3月月考化学试题云南省景谷一中2018-2019学年高二下学期第一次月考化学试题宁夏银川市银川二中2019-2020学年高二上学期第一次月考化学试题云南省开远市第二中学校2019-2020学年高二上学期期末考试化学试题(已下线)四川省成都外国语学校2018-2019学年高二下学期期中考试化学试题宁夏长庆高级中学2020-2021学年高二上学期期中考试化学试卷广东省江门市第二中学2021-2022学年高二上学期第一次月考化学试题内蒙古赤峰市元宝山区第一中学2021-2022学年高二下学期4月月考化学试题福建省莆田第二十五中学2021-2022学年高二上学期期末考试化学试题浙江省丽水外国语学校高中部2021-2022学年高二下学期第一次阶段性考试(3月)化学试题湖南省岳阳市华容县2022-2023学年高二上学期期末考试化学试题广东省汕尾市华大实验学校2022-2023学年高二下学期5月月考化学试题广东省茂名化州市第三中学2021-2022学年高二下学期3月月考化学试题云南省大理州实验中学2021-2022学年高二下学期化学期中考试题
8 . A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是______ (填元素符号),其中C原子的核外电子排布式为__________ 。
(2)单质A有两种同素异形体,其中沸点高的是_____ (填分子式),原因是_______ ;A和B的氢化物所属的晶体类型分别为______ 和______ 。
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为______ ,中心原子的杂化轨道类型为______ 。
(4)化合物D2A的立体构型为___ ,中心原子的价层电子对数为______ ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_________ 。
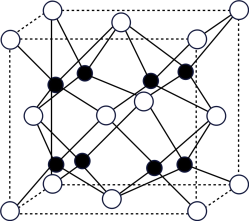
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,F的化学式为______ :晶胞中A原子的配位数为_________ ;列式计算晶体F的密度(g.cm-3)_____ 。
(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为
(4)化合物D2A的立体构型为
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,F的化学式为

您最近一年使用:0次
2019-01-30更新
|
7105次组卷
|
32卷引用:云南省西畴县第二中学2019-2020学年高三上学期期末考试化学试题
云南省西畴县第二中学2019-2020学年高三上学期期末考试化学试题2015年全国普通高等学校招生统一考试化学(新课标II卷)2016届广东省仲元中学高三11月月考理科综合化学试卷2016届重庆市第一中学高三上12月月考理综化学试卷2016届宁夏六盘山中学高三上第一次模拟理综化学试卷2017届江西省九江市十校高三第二次联考理科综合化学试卷新疆生产建设兵团第二中学2016-2017学年高二下学期第二次月考化学试题宁夏六盘山高级中学2017届高三第五次模拟考试理科综合化学试题宁夏石嘴山市第三中学2018届高三9月月考化学试题河北省正定中学2017届高三上学期第三次月考化学试题四川省南充高级中学2018届高三上学期第四次检测理综化学试题山西省临猗县临晋中学2017-2018学年高二下学期期末考试化学试题西藏自治区日喀则市南木林高级中学2019届高三第一次月考理综化学试题河北省唐山市第十一中学2018-2019学年高二下学期期中考试化学试题鲁科版高中化学选修3模块综合测评卷山西省应县第一中学校2018-2019学年高二下学期期中考试化学试题云南省玉溪一中2020届高三上学期期中考试理综化学试题四川省成都市双流棠湖中学2019-2020学年高二下学期第二次月考化学试题2020届浙江省杭州学军中学高三教学质量监测卷化学试题湖南省长沙市礼雅中学2020届高三下学期三月份网络教学质量监测理科综合化学试题吉林省长春市东北师大附中2020届高中毕业班三月份网络教学质量监测卷理科综合化学部分广东省广州市华南师范大学附属中学2020届高三教学质量监测卷理科综合化学试题广东省深圳外国语学校2021届高三上学期11月月考化学试题四川省成都市北大成都附属实验学校2021届高三上学期12月月考理科综合化学试题广东省2021届高三“六校联盟”第三次联考化学试题四川省成都龙泉中学2021届高三下学期4月月考理科综合化学试题吉林省松原市实验高级中学2021届高三5月月考化学试题(已下线)2020年海南卷化学高考真题变式题15-19山东省德州市2021-2022学年高二下学期物质结构与性质模块综合测评化学试题吉林省汪清县汪清四中2020-2021学年高二下学期期末考试化学试题河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题内蒙古通辽市/科左中旗民族职专·实验高中2023-2024学年高三上学期第二次月考化学试卷
名校
9 . 下列有关电负性的说法中不正确的是( )
| A.元素的电负性越大,原子在化合物中吸引电子的能力越强 |
| B.主族元素的电负性越大,元素原子的第一电离能一定越大 |
| C.在元素周期表中,同一周期元素电负性从左到右呈现递增的趋势 |
| D.形成化合物时,电负性越小的元素越容易显示正价 |
您最近一年使用:0次
2019-01-04更新
|
329次组卷
|
7卷引用:云南省麻栗坡民族中学2019-2020学年高二上学期期末考试化学试题
云南省麻栗坡民族中学2019-2020学年高二上学期期末考试化学试题云南省彝良县民族中学2018-2019学年高二上学期12月份考试化学试题(已下线)1.2.3 元素的电负性及其变化规律-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)云南省玉溪市峨山一中2021—2022学年高二下学期3月月考化学试题云南省玉溪市民族中学2021-2022学年高二上学期期末考试化学试题(已下线)第38练 原子结构与元素的性质-2023年高考化学一轮复习小题多维练(全国通用)上海交通大学附属中学2022-2023学年高二上学期开学摸底考试化学试题
10 . 下列说法中正确的是( )
| A.3d3表示3d能级上有3个轨道 |
B.ns能级的原子轨道图都可以用如图表示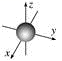 |
| C.1s电子云呈球形,表示电子绕原子核做圆周运动 |
| D.电子云图的黑点密度越大,说明核外空间电子数越多 |
您最近一年使用:0次
2018-12-24更新
|
201次组卷
|
4卷引用:云南省广南县二中2021-2022年学年高二下学期开学考试化学试题



