名校
解题方法
1 . 已知元素周期表中共有18纵行。如图所示实线表示元周期表的边界,按电子排布,可把元素周期表划分为s区、p区、d区、ds等,除ds区外,其他区的名称均按构造原理最后填入电子的能级符号来命名。
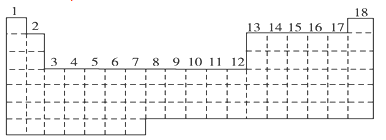
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区_____ 。
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在___________ 区。
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)_____ 。
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:___________ 。
(5)随着科学技术的发展,不断有新的元素被发现。现在第七周期已经排满,则元素周期表共可以排布___________ 种元素。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:
(5)随着科学技术的发展,不断有新的元素被发现。现在第七周期已经排满,则元素周期表共可以排布
您最近一年使用:0次
2022-10-20更新
|
157次组卷
|
2卷引用:云南省玉溪市华宁县第二中学2021-2022年高二下学期开学考试化学试题
解题方法
2 . 原子序数依次增大的五种元素A、B、E、F、G,A是周期表中原子半径最小的元素;B的基态原子价层电子排布为 ;E的基态原子
;E的基态原子 能级有3个单电子;F的基态原子L层电子数是K层电子数的3倍;G2+的
能级有3个单电子;F的基态原子L层电子数是K层电子数的3倍;G2+的 轨道中有6个电子。回答下列问题:
轨道中有6个电子。回答下列问题:
(1)G的基态原子的简化电子排布式为_______ ,价层电子的电子排布图为_______ ,其最外层电子的电子云形状为_______ 。
(2)基态G原子核外电子共占据了_______ 个能级,这些核外电子的空间运动状态有_______ 种。G元素在周期表中位置是_______ ,属于_______ 区元素(选填“s”、“p”、“d”或“ds”)。
(3) A、B、E、F是构成有机物的最重要的四种元素,这四种元素的第一电离能大小顺序为_______ 、电负性大小顺序为_______ 。
(4)基态E原子核外有_______ 种运动状态的电子。
(5)Mg、Al 两种元素中第一电离能较大的是_______ (填元素符号),原因为_______ 。
 ;E的基态原子
;E的基态原子 能级有3个单电子;F的基态原子L层电子数是K层电子数的3倍;G2+的
能级有3个单电子;F的基态原子L层电子数是K层电子数的3倍;G2+的 轨道中有6个电子。回答下列问题:
轨道中有6个电子。回答下列问题:(1)G的基态原子的简化电子排布式为
(2)基态G原子核外电子共占据了
(3) A、B、E、F是构成有机物的最重要的四种元素,这四种元素的第一电离能大小顺序为
(4)基态E原子核外有
(5)Mg、Al 两种元素中第一电离能较大的是
您最近一年使用:0次
解题方法
3 . 下列化学用语或图示表达正确的是
A.F-的结构示意图为 | B.苯的实验式:C6H6 |
C. 的电子式: 的电子式: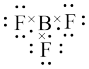 | D.基态氮原子的轨道表示式: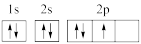 |
您最近一年使用:0次
4 . 已知A、B、C、D、E为原子序数依次增大的前36号元素,A的2p轨道有3个电子;B是地壳中含量最多的元素;C元素的M层有一个电子;D元素形成的单质具有两性;E的基态原子的电子排布为[Ar]3d104S1。回答下列问题(用元素符号或化学式表示):
(1)C的基态原子核外电子排布式为___________ ,E在元素周期表中位于___________ 区。
(2)B、C、D的原子半径由大到小的顺序为___________ (填元素符号)。
(3)A、B的第一电离能的大小关系是___________ (填元素符号)并从结构特点解释原因___________ 。
(4)B、C、D的电负性由大到小的顺序为___________ (填元素符号)。
(1)C的基态原子核外电子排布式为
(2)B、C、D的原子半径由大到小的顺序为
(3)A、B的第一电离能的大小关系是
(4)B、C、D的电负性由大到小的顺序为
您最近一年使用:0次
5 . 下列有关说法不正确的是
| A.基态原子的核外电子排布遵循能量最低原理 |
| B.原子核外电子从基态变成激发态一定需要吸收能量 |
| C.原子核外电子从基态跃迁到激发态时,只能跃迁到稍高的能级,如从2s只能跃迁到2p |
| D.夜幕下的霓虹灯光、军事上使用的激光均与原子核外电子发生跃迁有关 |
您最近一年使用:0次
解题方法
6 . 短周期主族元素X、Y、Z、W、M、O的原子序数逐渐增大,其中部分元素的性质或原子结构如下表:
试回答下列问题:
(1)Y原子最外层电子的轨道表示式为_______ 。
(2)元素Y、Z的简单离子半径大小关系为_______ (填离子符号,用”>"连接)。
(3)X原子的第一电离能_______ Y原子(填“>”、“<”或“=”),理由是_______ 。
(4)下列状态的W的微粒中,电离最外层的一个电子所需能量最小的是_______(填序号)。
(5)元素M与元素O相比,非金属性较强的是_______ (填元素符号),下列表述中能证明这一事实的是_______ (填序号)。
a.常温下,M的单质与O的单质状态不同
b.简单氢化物的稳定性:M<O
c.一定条件下M和O的单质都能与氢氧化钠溶液反应
d.M的电负性为2.5,O的电负性为3.0
| 元素 | 元素性质或原子结构 |
| X | 基态原子最外层电子排布为nsnnpn+1 |
| Z | 单质为银白色固体,质软,在空气中燃烧发出黄色的火焰 |
| W | 其最高价氧化物的水化物呈两性 |
| M | 原子序数是Y原子序数的2倍 |
试回答下列问题:
(1)Y原子最外层电子的轨道表示式为
(2)元素Y、Z的简单离子半径大小关系为
(3)X原子的第一电离能
(4)下列状态的W的微粒中,电离最外层的一个电子所需能量最小的是_______(填序号)。
| A.[Ne] | B.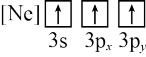 | C.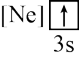 | D.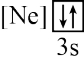 |
a.常温下,M的单质与O的单质状态不同
b.简单氢化物的稳定性:M<O
c.一定条件下M和O的单质都能与氢氧化钠溶液反应
d.M的电负性为2.5,O的电负性为3.0
您最近一年使用:0次
21-22高二·全国·课后作业
名校
7 . 下列原子或离子核外电子排布不属于基态排布的是
| A.Na:1s22s22p53s2 | B.S2-:1s22s22p63s23p6 |
| C.N:1s22s22p3 | D.Si:1s22s22p63s23p2 |
您最近一年使用:0次
2022-10-01更新
|
302次组卷
|
11卷引用:云南省宣威市第三中学2021-2022学年高二下学期3月份考试化学试题
云南省宣威市第三中学2021-2022学年高二下学期3月份考试化学试题天津市河北区2021-2022学年高二上学期期末质量检测化学试题吉林油田第十一中学2021-2022学年高二上学期期末考试化学试题海南省东方市东方中学2021-2022学年高二下学期期中考试化学试题江西省宜春市宜丰中学2022-2023学年高三上学期11月期中考试化学试题(已下线)1.1.2 构造原理与电子排布式(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)四川省南充市嘉陵第一中学2021-2022学年高二上学期第二次月考化学试题四川省宜宾市南溪区第二中学校2021-2022学年高二上学期12月月考化学试题四川省南充市嘉陵第一中学2022-2023学年高二下学期6月月考化学试题湖南省株洲市炎陵县第一中学等2校2022-2023学年高二下学期开学考试化学试题新疆乌鲁木齐市第三十一中学2023-2024学年高二下学期3月月考 化学试题
8 . 铜是人类最早使用的金属之一。回答下列问题:
(1)基态铜原子的价层电子排布图为___________ 。
(2)向 溶液中加入足量氨水得到深蓝色
溶液中加入足量氨水得到深蓝色 溶液,再向其中加入盐酸羟胺(
溶液,再向其中加入盐酸羟胺(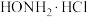 )至溶液变为无色,再通入
)至溶液变为无色,再通入 后析出
后析出 红色沉淀(干燥时极易爆炸)。上述涉及的H、C、N、O、S、Cl、Cu七种元素中第一电离能最大的是
红色沉淀(干燥时极易爆炸)。上述涉及的H、C、N、O、S、Cl、Cu七种元素中第一电离能最大的是___________ (填元素符号); 的空间结构名称为
的空间结构名称为___________ ; 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为___________ ; 在水中的溶解度较小的原因是
在水中的溶解度较小的原因是___________ ; 中碳原子的杂化轨道类型为
中碳原子的杂化轨道类型为___________ 。
(3)上述 、
、 的晶体类型都属于下列中的___________(填标号)。
的晶体类型都属于下列中的___________(填标号)。
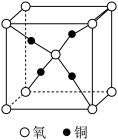
(4)铜和氧形成的一种离子化合物的晶体结构如图所示。若其晶胞边长为a pm,阿伏加德罗常数值为 ,则该晶体密度为
,则该晶体密度为___________  。
。
(1)基态铜原子的价层电子排布图为
(2)向
 溶液中加入足量氨水得到深蓝色
溶液中加入足量氨水得到深蓝色 溶液,再向其中加入盐酸羟胺(
溶液,再向其中加入盐酸羟胺(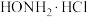 )至溶液变为无色,再通入
)至溶液变为无色,再通入 后析出
后析出 红色沉淀(干燥时极易爆炸)。上述涉及的H、C、N、O、S、Cl、Cu七种元素中第一电离能最大的是
红色沉淀(干燥时极易爆炸)。上述涉及的H、C、N、O、S、Cl、Cu七种元素中第一电离能最大的是 的空间结构名称为
的空间结构名称为 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为 在水中的溶解度较小的原因是
在水中的溶解度较小的原因是 中碳原子的杂化轨道类型为
中碳原子的杂化轨道类型为(3)上述
 、
、 的晶体类型都属于下列中的___________(填标号)。
的晶体类型都属于下列中的___________(填标号)。| A.分子晶体 | B.共价晶体 | C.金属晶体 | D.离子晶体 |
 ,则该晶体密度为
,则该晶体密度为 。
。
您最近一年使用:0次
9 . 全球的海底和冰川底部藏在天然气水合物(又称“可燃冰”)中的天然气,是巨大的潜在能源。我国可燃冰开采技术世界领先。某种可燃冰平均46个 分子构成8个笼,每个笼可以装1个分子,假设其中6个笼里装有
分子构成8个笼,每个笼可以装1个分子,假设其中6个笼里装有 分子,2个笼里装有
分子,2个笼里装有 分子。下列说法错误的是
分子。下列说法错误的是
 分子构成8个笼,每个笼可以装1个分子,假设其中6个笼里装有
分子构成8个笼,每个笼可以装1个分子,假设其中6个笼里装有 分子,2个笼里装有
分子,2个笼里装有 分子。下列说法错误的是
分子。下列说法错误的是A.该可燃冰的组成可表示为 |
| B.其组成元素中电负性最大的是O,最小的是H |
| C.可燃冰可看作由水和甲烷等分子通过非共价键形成的超分子 |
| D.硫化氢分子间也能通过与水分子间类似的相互作用形成分子笼 |
您最近一年使用:0次
10 . X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,其相关信息如表:
请用化学用语填空:
(1)请写出Q元素基态原子的外围电子排布图:____ 。
(2)X、Y、Z、M四种元素的原子半径由小到大的顺序是____ (用元素符号表示)。
(3)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是___ 。
(4)含Z元素的焰火显黄色,主要与____ 有关。
(5)M元素原子的逐级电离能越来越大的原因是____ 。
(6)与M元素成“对角线规则”关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物的水化物反应的化学方程式:____ ;已知T元素和Q元素的电负性分别为1.5和3.0,则它们形成的化合物是____ (填“离子化合物”或“共价化合物”)。
| 元素 | 相关信息 |
| X | 原子核外有6种不同运动状态的电子 |
| Y | 基态原子中s电子总数与p电子总数相等 |
| Z | 原子半径在同周期元素中最大 |
| M | 逐级电离能(kJ·mol-1)依次为578、1817、2745、11575、14830、18376 |
| Q | 基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反 |
| R | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
(1)请写出Q元素基态原子的外围电子排布图:
(2)X、Y、Z、M四种元素的原子半径由小到大的顺序是
(3)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是
(4)含Z元素的焰火显黄色,主要与
(5)M元素原子的逐级电离能越来越大的原因是
(6)与M元素成“对角线规则”关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物的水化物反应的化学方程式:
您最近一年使用:0次



