1 . 以下有关元素性质的说法中不正确的是
| A.①Na、K、Rb,②N、P、As,③O、S、Se,④Na、P、O元素的电负性依次递增的是④ |
| B.下列原子中,①1s22s22p63s23p1,②1s22s22p63s23p2,③1s22s22p63s23p3,④1s22s22p63s23p4对应的第一电离能最大的元素是④ |
| C.某短元素的逐级电离能(kJ∙mol−1)分别为738、1451、7733、10540、13630、17995、21703,该元素可能在第三周期ⅡA族 |
| D.以下原子中,①1s22s22p63s23p2,②1s22s22p3,③1s22s22p2,④1s22s22p63s23p4半径最大的是① |
您最近一年使用:0次
解题方法
2 . 下列给出的基态原子的电子排布式,其中正确的是
| A.11Na:1s22s22p7 | B.47Ag:1s22s22p63s23p63d104s24p64d95s2 |
| C.20Ca:1s22s22p63s23p63d2 | D.35Br:[Ar]3d104s24p5 |
您最近一年使用:0次
2022-09-22更新
|
412次组卷
|
5卷引用:云南省玉溪市通海县第三中学2021-2022学年高二上学期期末考试化学试题
云南省玉溪市通海县第三中学2021-2022学年高二上学期期末考试化学试题专题2 原子结构与元素性质 第一单元 原子核外电子的运动 第2课时 原子核外电子的排布(已下线)1.1.2 电子云与原子轨道-同步学习必备知识2.1.2原子核外电子的排布 课中(已下线)第01讲 原子结构-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)
3 . 硅是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态硅(Si)原子的核外电子排布式为[Ne]___________ ,有___________ 个未成对电子。
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态Ge原子的核外电子占据___________ 个能层、___________ 个能级。
②上述三种元素的电负性由大到小的顺序为___________ (填元素符号)。
③固态CO2可用于人工降雨,SiO2常用于___________ (填一种即可)。
(1)基态硅(Si)原子的核外电子排布式为[Ne]
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态Ge原子的核外电子占据
②上述三种元素的电负性由大到小的顺序为
③固态CO2可用于人工降雨,SiO2常用于
您最近一年使用:0次
名校
解题方法
4 . 工业上用含砷、锑烟灰(主要成分为Sb2O3、As2O3,含Pb、Ag、 Cu的氧化物)制取焦锑酸钠[NaSb(OH)6]和砷酸钠晶体(Na3AsO4 ·12H2O),不仅治理了砷害污染,还可综合回收其他有价金属。其工艺流程如图所示:
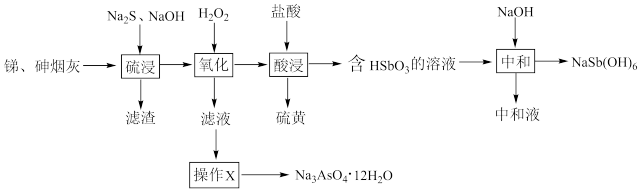
已知:①Pb、Ag、Cu的氧化物不溶于Na2S溶液。
②硫浸后,锑、砷以Na3SbS3、Na3AsS3的形式存在。
③NaSb(OH)6易溶于热水,难溶于冷水,不溶于乙醇。
回答下列问题:
(1)As的核外电子排布式是_______ , 在元素周期表中,Cu处于_______ 区。
(2)“硫浸”时,Sb2O3溶解的离子方程式为_______ 。“氧化”时氧化产物除了锑的含氧酸盐外,还有_______ (填化学式)。
(3)“操作”X为_______ 、过滤、洗涤、干燥。“中和”时生成NaSb( OH)6的化学方程式是_______ 。
(4)研究发现,电解硫浸液中的Na3SbS3-NaOH溶液,可得到单质Sb,则阴极的电极反应式为_______ 。
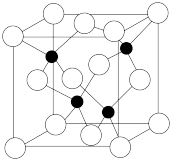
(5)砷的化合物砷化镓是一种重要的半导体材料,已知镓(Ga)是铝的同族元素,砷化镓的晶胞结构如图所示。该晶胞中黑球代表_______ ( 填元素符号),砷化镓的化学式为_______ ,该晶体中含有的化学键为_______ (填“共价键”“配位键”“离子键”),属于_______ 晶体。

已知:①Pb、Ag、Cu的氧化物不溶于Na2S溶液。
②硫浸后,锑、砷以Na3SbS3、Na3AsS3的形式存在。
③NaSb(OH)6易溶于热水,难溶于冷水,不溶于乙醇。
回答下列问题:
(1)As的核外电子排布式是
(2)“硫浸”时,Sb2O3溶解的离子方程式为
(3)“操作”X为
(4)研究发现,电解硫浸液中的Na3SbS3-NaOH溶液,可得到单质Sb,则阴极的电极反应式为
(5)砷的化合物砷化镓是一种重要的半导体材料,已知镓(Ga)是铝的同族元素,砷化镓的晶胞结构如图所示。该晶胞中黑球代表

您最近一年使用:0次
12-13高三上·山西·阶段练习
名校
解题方法
5 . 下列各组原子中,彼此化学性质一定相似的是
| A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 |
| C.2p能级上只有两个电子的X原子与3p能级上只有两个电子的Y原子 |
| D.最外层都只有一个电子的X、Y原子 |
您最近一年使用:0次
2022-08-28更新
|
759次组卷
|
67卷引用:云南省玉溪市峨山一中2021—2022学年高二下学期3月月考化学试题
云南省玉溪市峨山一中2021—2022学年高二下学期3月月考化学试题云南省玉溪市华宁二中2018-2019学年9月份考试高二化学试题云南省香格里拉县一中2018-2019学年高二上学期期中考试化学试题云南省丘北县第二中学2018-2019学年高二下学期6月份考试化学试题福建省龙岩第一中学2021-2022学年高二(实验班)下学期第一次月考化学试题专题2 原子结构与元素性质 第一单元 原子核外电子的运动 第2课时 原子核外电子的排布新疆乌鲁木齐高级中学2021-2022学年高二上学期期末考试化学试题第一节 原子结构 第2课时 构造原理与电子排布式,电子云与原子轨道吉林省吉林第一中学2022-2023学年高二上学期11月月考化学试题(已下线)2013届山西省山西大学附属中学高三10月月考化学试卷(已下线)2012-2013学年福建三明泰宁一中高二下第一次阶段考试化学试卷(已下线)2013-2014江苏省扬州中学高二下学期阶段测试5月 化学试卷2014-2015河北省邢台市第一中学高二12月月考化学试卷2014-2015四川省达州市大竹县文星中学高二3月月考化学试卷2014-2015学年辽宁省沈阳市沈阳二中高二下期中化学试卷2014-2015学年浙江省台州中学高二下第一次统练化学试卷2014-2015学年浙江省绍兴市一中高二下学期期末化学试卷2014-2015学年山东省淄博市高二下学期期末统考化学试卷2015-2016学年黑龙江省哈尔滨六中高二下期中化学试卷2015-2016学年辽宁省沈阳二中高二下期中化学试卷河南省郑州市八校2016-2017学年高二下学期期中联考化学试题黑龙江省牡丹江市第一高级中学2016-2017学年高二下学期期中考试化学试题河南省驻马店市2016-2017学年高二下学期期末考试化学试题宁夏石嘴山市第三中学2016-2017学年高二下学期期末(2018届高三入学)考试化学试题辽宁省实验中学分校2016-2017学年高二下学期期末考试化学试题广西钦州市钦州港经济技术开发区中学2018届高三上学期开学考试化学试题安徽省蚌埠市第二中学2017-2018学年高二上学期期中考试化学试题宁夏吴忠市2017-2018学年高二人教版选修3化学同步练习:第1章 原子结构与性质综合练习1宁夏六盘山高级中学2017-2018学年高二下学期第一次月考考试化学试题吉林省延边市第二中学2017-2018学年高二下学期第一次月考化学试题【全国百强校】黑龙江省实验中学2017-2018学年高二下学期期中考试(理)化学试题四川省遂宁二中2018-2019学年高二上学期半期考试化学试题【全国百强校】山东省潍坊第一中学2018-2019学年高二下学期开学(2月)考试化学试题山西省沁县中学2018-2019学年高二下学期第一次月考化学试题福建省罗源市第一中学2018-2019学年高二下学期3月月考化学试题湖北省宜昌市葛洲坝中学2018-2019学年高二下学期期中考试化学试题【全国百强校】贵州省思南中学2018-2019学年高二下学期期中考试化学试题【全国百强校】河南省林州市第一中学2018-2019学年高二下学期5月月考化学试题吉林省公主岭市范家屯镇第一中学2018-2019学年高二下学期期中考试化学试题安徽省毛坦厂中学2019-2020学年高二上学期期中考试化学试题黑龙江省哈尔滨市第六中学2019-2020学年高二上学期期末考试化学试题山东省烟台第二中学2019-2020学年高二上学期12月月考化学试题(已下线)上海建平高级中学 2012-2013学年高三下学期模拟化学试题江西省宜春市第九中学2019-2020学年高二下学期第二次月考化学(网班)试题湖北省襄阳市第一中学2019-2020学年高二5月月考化学试题辽宁省营口市部分重点高中2017-2018学年高二下学期期末考试化学试题陕西省咸阳市实验中学2019-2020学年高二上学期第一次月考化学试题河北省新乐市第一中学2018--2019学年高二下学期第二次月考化学试题河北省唐山市开滦第二中学2019-2020学年高二6月月考化学试题安徽省六安市舒城中学2019-2020学年高二下学期第一次月考化学试题河北省沧州市盐山县盐山中学2019-2020学年高二下学期期末考试化学试题(已下线)第34讲 原子结构与性质-2021年高考化学一轮复习名师精讲练吉林省吉化第一高级中学校2020-2021学年高二下学期3月月考化学试题黑龙江省实验中学2020-2021学年度下学期高二学年第一次月考化学试题吉林省松原市乾安县第七中学2020-2021学年高二下学期第五次质量检测化学试题新疆维吾尔自治区乌鲁木齐市第四中学2020-2021学年高二年级下学期期中考试化学试题福建省莆田第十五中学2019-2020学年高二下学期期末考试化学试题(已下线)课时54 原子结构与性质-2022年高考化学一轮复习小题多维练(全国通用)甘肃省兰州市第二十七中学2020-2021学年高二下学期期末考试化学试题2019鲁科版高中化学选择性必修2第1章第2节 原子结构与元素周期表课后习题湖北省十堰市普通高中协作体2022-2023学年高二下学期3月月考化学试题福建省永安市第三中学高中校2022-2023学年高三下学期第一次月考(3月)化学试题陕西省宝鸡市金台区2022-2023学年高二下学期期中质量检测化学试题2.1.2原子核外电子的排布 课中湖北省襄阳市第五中学2022-2023学年高二下学期开学考试化学试题辽宁省沈阳市第二中学2023-2024学年高二上学期第二次月考化学试题湖北省恩施高中2023-2024学年高一下学期入学考试化学试题
名校
解题方法
6 . X是合成碳酸二苯酯的一种有效的氧化还原催化助剂,可由EDTA与Fe3+反应得到。
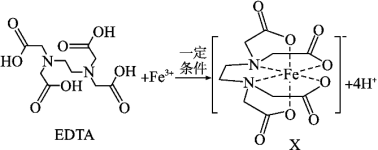
(1)基态Si原子的价层电子的运动状态有_______ 种,若其电子排布式表示为[Ne]3s2 违背了
违背了_______ 。
(2)EDTA中碳原子杂化轨道类型为_______ ,EDTA中四种元素的电负性由小到大的顺序为_______ 。C、N、O第一电离能由小到大的顺序为_______ 。
(3)Fe3+基态价层电子排布式为_______ 。
(4)EDTA与正二十一烷的相对分子质量非常接近,但EDTA的沸点比正二十一烷的沸点高的原因是_______ 。
(5)设NA代表阿伏加德罗常数的值,1mol碳酸分子中含有σ键的数目为_______ 。

(1)基态Si原子的价层电子的运动状态有
 违背了
违背了(2)EDTA中碳原子杂化轨道类型为
(3)Fe3+基态价层电子排布式为
(4)EDTA与正二十一烷的相对分子质量非常接近,但EDTA的沸点比正二十一烷的沸点高的原因是
(5)设NA代表阿伏加德罗常数的值,1mol碳酸分子中含有σ键的数目为
您最近一年使用:0次
7 . 短周期元素D、E、F、W原子序数依次递增,已知:
①D元素的某种同位素通常用于地质年代的鉴定;
②F元素电负性在周期表所有元素中位列第二;
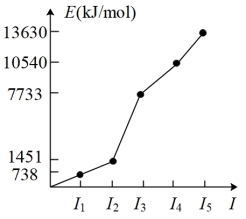
③W的各级电离能如图。
下列判断不正确的是
①D元素的某种同位素通常用于地质年代的鉴定;
②F元素电负性在周期表所有元素中位列第二;
③W的各级电离能如图。

下列判断不正确的是
| A.D、E、F三元素的第一电离能由大到小的顺序是E>F>D |
| B.D、E、F三元素的简单氢化物中可形成氢键的有两种 |
| C.元素W在周期表中的位置是第3周期第IIA族 |
D.基态D原子价电子轨道表示式为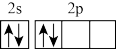 |
您最近一年使用:0次
2022-08-26更新
|
119次组卷
|
2卷引用:云南省曲靖市罗平县第一中学2021-2022学年高二下学期期末理综化学试题
名校
8 . 磷酸锌常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰(主要含ZnO,还含少量FeO、Al2O3、CuO及SiO2)为原料制取磷酸锌的工艺流程如图所示:
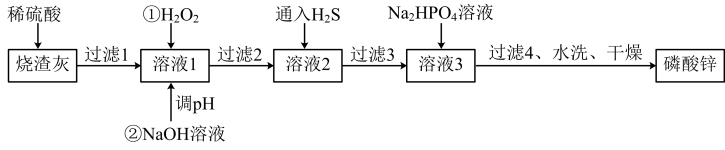
已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
(1)基态Zn原子的价电子排布式为______
(2)用硫酸浸烧渣灰,为提高酸浸时锌的浸出率,可以采取的措施是______ (填一条)。
(3)加入H2O2的作用_______
(4)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是______ 。
(5)加入Na2HPO4溶液发生反应的离子方程式为_____ 。
(6)洗涤磷酸锌沉淀时应选用____ (填“冷水”或“热水”),确认磷酸锌洗涤干净的操作是_____ 。
(7)通入H2S是为了除铜离子,25°C时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1mol·L-1,此时溶液中c(Cu2+)=6.3×10-15mol·L-1,则CuS的溶度积Ksp=______ (已知:25°C时,H2S的电离平衡常数Ka1=1×10-7,Ka2=1×10-15)。

已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4 | 6.5 |
| 完全沉淀的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(2)用硫酸浸烧渣灰,为提高酸浸时锌的浸出率,可以采取的措施是
(3)加入H2O2的作用
(4)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是
(5)加入Na2HPO4溶液发生反应的离子方程式为
(6)洗涤磷酸锌沉淀时应选用
(7)通入H2S是为了除铜离子,25°C时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1mol·L-1,此时溶液中c(Cu2+)=6.3×10-15mol·L-1,则CuS的溶度积Ksp=
您最近一年使用:0次
2022-08-25更新
|
490次组卷
|
3卷引用:云南师范大学附属中学2022-2023学年高三上学期高考适应性月考卷(二)理科综合化学试题
解题方法
9 . 已知短周期元素X、Y、Z、W、Q和R在周期表中的相对位置如图所示,X能与W形成两种常见的离子化合物,阴阳离子个数比均为1∶2。回答下列问题:
(1)化合物XR的电子式为____ 。
(2)基态W原子的最外层有____ 个未成对电子。
(3)Z单质与Q的最高价氧化物对应水化物的浓溶液在加热条件下反应的化学方程式为____ 。
(4)Y在Z的最高价氧化物中燃烧的化学方程式为____ 。
| Z | W | |||||
| X | Y | Q | R |
(2)基态W原子的最外层有
(3)Z单质与Q的最高价氧化物对应水化物的浓溶液在加热条件下反应的化学方程式为
(4)Y在Z的最高价氧化物中燃烧的化学方程式为
您最近一年使用:0次
10 . 短周期元素X、Y、Q、R、W原子最外层电子数与原子序数的关系如图所示。下列说法错误的是
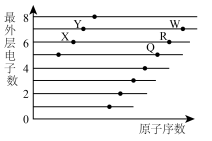

| A.X元素位于元素周期表p区 |
| B.简单氢化物的沸点:X>Y>R |
| C.第一电离能:W>R>Q |
| D.最高价氧化物对应水化物的酸性:W>R |
您最近一年使用:0次
2022-08-22更新
|
115次组卷
|
2卷引用:云南省昆明市五华区2023届高三教学质量摸底检测化学试题



