1 . 下表是元素周期表的一部分,按要求回答下列问题:
(1)⑦的原子结构示意图为________ ,⑨的单质的电子式为________ 。
(2)②③④三种元素对应的简单氢化物中最稳定的是________ (填化学式,下同)。上述九种元素中,最高价氧化物的水化物酸性最强的化合物的化学式是________ 。
(3)③、④、⑥、⑦的简单离子半径由大到小的顺序是________ (用离子符号表示)。
(4)根据“对角线规则”,Be与Al具有相似的化学性质,请写出 与⑥的最高价氧化物的水化物反应的化学方程式
与⑥的最高价氧化物的水化物反应的化学方程式________ 。(生成的盐中阴阳离子个数比为1∶2)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)②③④三种元素对应的简单氢化物中最稳定的是
(3)③、④、⑥、⑦的简单离子半径由大到小的顺序是
(4)根据“对角线规则”,Be与Al具有相似的化学性质,请写出
 与⑥的最高价氧化物的水化物反应的化学方程式
与⑥的最高价氧化物的水化物反应的化学方程式
您最近一年使用:0次
解题方法
2 . 三价铬离子(Cr3+)是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等。回答下列问题:
(1)Cr的价电子排布式为_______ 。
(2)O、N、S的原子半径由大到小的顺序为_______ 。
(3)SO2分子的 VSEPR模型名称为_______
(4)化学式为CrCl3·6H2O的化合物有多种结构,其中一种可表示为[CrCl2(H2O)4]Cl·2H2O,该物质的配离子中提供孤电子对的原子为_______ ,配位数为_______ 。
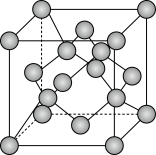
(5)由碳元素形成的某种晶体的晶胞结构如图所示,若阿伏加德罗常数的值为NA,晶体密度为ρg/cm3,则该晶胞的棱长为_______ cm。
(1)Cr的价电子排布式为
(2)O、N、S的原子半径由大到小的顺序为
(3)SO2分子的 VSEPR模型名称为
(4)化学式为CrCl3·6H2O的化合物有多种结构,其中一种可表示为[CrCl2(H2O)4]Cl·2H2O,该物质的配离子中提供孤电子对的原子为
(5)由碳元素形成的某种晶体的晶胞结构如图所示,若阿伏加德罗常数的值为NA,晶体密度为ρg/cm3,则该晶胞的棱长为

您最近一年使用:0次
解题方法
3 . 有W、X,Y、Z、M五种元素,其中W、X、Y、Z为原子序数依次增大的短周期主族元素,W的单质是密度最小的气体,X、Z同主族,且Z的原子序数是X的2倍,Y是所在周期中原子半径最小的金属元素,M为金属元素,其相对原子质量是Z的2倍。回答下列问题:
(1)X、Y、Z的电负性由大到小的顺序是_______ (用元素符号表示)。
(2)五种元素中形成的二元化合物分子含18电子的有_______ (用化学式表示),写出其中一种分子的电子式:_______ 。
(3)甲为X,M元素形成的黑色化合物,甲与 ,在加热条件下生成M的单质和两种无态的物质,写出该反应的化学方程式:
,在加热条件下生成M的单质和两种无态的物质,写出该反应的化学方程式:_______ 。
(4)写出Z的+4价氧化物在酸性环境中被 氧化为Z的最高价氧化物对应的水化物的离子方程式:
氧化为Z的最高价氧化物对应的水化物的离子方程式:_______ 。
(5)电解熔融状态Y的氧化物生成Y的单质的反应中,生成2.7g固体时,收集到的气体为_______ mL(标准状况)。
(1)X、Y、Z的电负性由大到小的顺序是
(2)五种元素中形成的二元化合物分子含18电子的有
(3)甲为X,M元素形成的黑色化合物,甲与
 ,在加热条件下生成M的单质和两种无态的物质,写出该反应的化学方程式:
,在加热条件下生成M的单质和两种无态的物质,写出该反应的化学方程式:(4)写出Z的+4价氧化物在酸性环境中被
 氧化为Z的最高价氧化物对应的水化物的离子方程式:
氧化为Z的最高价氧化物对应的水化物的离子方程式:(5)电解熔融状态Y的氧化物生成Y的单质的反应中,生成2.7g固体时,收集到的气体为
您最近一年使用:0次
名校
4 . 元素周期表中的四种元素的有关信息如下,请用合理的化学用语填写空白。
(1)X元素周期表中的位置为___ ,X、Y、Z三种元素的简单离子半径从大到小的顺序为___ 。
(2)足量W的最高价氧化物的水化物是稀溶液与1mol甲完全反应,放出热量QkJ,请写出表示该过程中和热的热化学方程式:____ 。
(3)下列有关W的气态氢化物丁的说法正确的有___ (选填字母)
a.丁比氯化氢沸点高 b.丁比氯化氢稳定性好
c.丁比氟化氢还原性弱 d.丁比氟化氢酸性弱
(4)请写出丙溶于丁的水溶液的离子方程式___ 。
| 在周期表中的区域 | 元素代号 | 有关信息 |
| 短周期元素 | X | X的最高价氧化物的水化物甲是一种胃酸中和剂,且能溶于强碱溶液 |
| Y | Y的一种氢化物可用于制造纯碱和做制冷剂 | |
| 长周期元素 | Z | Z的一种盐乙可以作净水剂,Z的某种氧化物丙可以做红色涂料 |
| W | W元素大多存在于海藻种,它的银盐可用于人工降雨 |
(1)X元素周期表中的位置为
(2)足量W的最高价氧化物的水化物是稀溶液与1mol甲完全反应,放出热量QkJ,请写出表示该过程中和热的热化学方程式:
(3)下列有关W的气态氢化物丁的说法正确的有
a.丁比氯化氢沸点高 b.丁比氯化氢稳定性好
c.丁比氟化氢还原性弱 d.丁比氟化氢酸性弱
(4)请写出丙溶于丁的水溶液的离子方程式
您最近一年使用:0次
2019-10-23更新
|
202次组卷
|
2卷引用:海南省三亚市第一中学2021-2022学年高三下学期最后一卷化学试题
解题方法
5 . 现有A、B、C、D四种短周期元素,它们的原子序数依次增大。A与D同主族,B与C同周期,B原子的最外层电子数是内层电子数的2.5倍,A与C形成的常见化合物在常温下为液态。
(1)元素A在周期表中的位置是______ ;B、C、D形成的简单离子中半径最小的是______ (填离子符号)。
(2)常温下,氯气能与由A、C、D三种元素组成的一种常见化合物发生反应,该反应的化学方程式为_______ 。
(3)B与C的最简单气态氢化物中稳定性较强的是______ (填化学式)。
(4)元素B和氯元素能形成一种化合物BCl3。BCl3能发生水解反应生成一种弱碱和一种弱酸,写出该反应的化学方程式:________ 。
(1)元素A在周期表中的位置是
(2)常温下,氯气能与由A、C、D三种元素组成的一种常见化合物发生反应,该反应的化学方程式为
(3)B与C的最简单气态氢化物中稳定性较强的是
(4)元素B和氯元素能形成一种化合物BCl3。BCl3能发生水解反应生成一种弱碱和一种弱酸,写出该反应的化学方程式:
您最近一年使用:0次
解题方法
6 . X、Y、Z、M和N均为短周期元素,X、Y、Z原子序数依次增大且最外层电子数之和为15,X与Z可形成XZ、XZ2型分子, Y与M气态化合物标准状况下密度约0.76g/L。N的原子半径为短周期元素中最大。回答下列问题:
(1)M、Z和N的元素符号分别为_______ 、_________ 、_______ 。
(2)X、Y、Z、M四种元素的原子半径由大到小的顺序为______________________ 。
(3)由上述元素组成、既含有共价键又含有离子键的化合物,其中含有极性共价键或含有非极性共价键,各举一例用电子式表示为_______ 、 ________ 。
(4)X和Y组成的离子XY-对环境有害,可在NaClO的碱性溶液中转化为碳酸盐和氮气,相应的离子方程式为__________________________ 。
(1)M、Z和N的元素符号分别为
(2)X、Y、Z、M四种元素的原子半径由大到小的顺序为
(3)由上述元素组成、既含有共价键又含有离子键的化合物,其中含有极性共价键或含有非极性共价键,各举一例用电子式表示为
(4)X和Y组成的离子XY-对环境有害,可在NaClO的碱性溶液中转化为碳酸盐和氮气,相应的离子方程式为
您最近一年使用:0次



