11-12高二下·内蒙古包头·期中
名校
1 . 不能说明X的电负性比Y的大的是()
| A.与H2化合时X单质比Y单质容易 |
| B.X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 |
| C.X原子的最外层电子数比Y原子的最外层电子数多 |
| D.X单质可以把Y从其氢化物中置换出来 |
您最近一年使用:0次
2016-12-09更新
|
1717次组卷
|
31卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第2课时
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第2课时(已下线)2011-2012学年内蒙古包头三十三中高二下学期期中考试化学试卷(已下线)2014年高二鲁科版选修3化学规范训练 1.3原子结构与元素性质练习卷2016-2017学年黑龙江哈三中高二下学期4月月考(验收)考试化学试卷福建省福州市八县(市)协作校2016-2017学年高二下学期期中考试化学试题人教版2017-2018学年高二化学选修三同步训练:第一章 原子结构与性质2【全国百强校】辽宁省葫芦岛市第一高级中学2017-2018学年高二下学期期中考试化学试题新疆阿勒泰地区第二高级中学2018-2019学年高二下学期期末(A卷)化学试题黑龙江省哈尔滨市第三中学校2019-2020学年高二上学期期末考试化学试题云南省元阳县第三中学2019-2020学年高二上学期期末考试化学试题山东省烟台第二中学2019-2020学年高二上学期12月月考化学试题人教化学选修3第一章第二节课时3黑龙江省哈尔滨市第三中学2019-2020学年高二上学期第一模块(期末)考试化学试题第3节 原子结构与元素性质——A学习区 夯实基础(鲁科版选修3)江西省都昌县第三中学2019-2020学年高二下学期4月考试化学试题江西省都昌县第一中学2019-2020学年高二下学期期中线上考试化学试题宁夏自治区银川市北方民族大学附属中学2019-2020学年度(下)高二月考试卷四川省越西中学2019-2020学年高二5月月考化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质 课时2 元素周期律——原子半径、电离能、电负性的递变规律(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质江苏省南京市2019-2020学年高二下学期期末考试化学试卷A卷江苏省扬州中学2020-2021学年高二下学期期中考试化学试题湖北省十堰市2016-2017学年高二下学期期末调研考试化学试题(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第38练 原子结构与元素的性质-2023年高考化学一轮复习小题多维练(全国通用)专题1~2 综合检测(提升卷)新疆博尔塔拉蒙古自治州蒙古中学2020-2021学年高二下学期期中考试化学试题 河北省石家庄市第23中学2022-2023学年高二上学期第一次月考化学试题河北省邯郸市永年区第二中学2022-2023学年高二上学期12月月考化学试题江苏省盐城市东台创新高级中学2021-2022学年高二2月份月检测化学试题(已下线)题型82 电负性的比较
名校
解题方法
2 . 如图为周期表中部分元素某种性质(X值)随原子序数变化的关系。___ (填元素符号)。
(2)同主族内不同元素的X值变化的特点是___ ;同周期内,随着原子序数的增大,X值的变化总趋势是___ 。周期表中X值的这种变化特点体现了元素性质的___ 变化规律。
(3)X值较小的元素集中在元素周期表的___ (填序号,下同)。
a.左下角 b.右上角 c.分界线附近
(4)下列说法正确的是___ 。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱

(2)同主族内不同元素的X值变化的特点是
(3)X值较小的元素集中在元素周期表的
a.左下角 b.右上角 c.分界线附近
(4)下列说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
您最近一年使用:0次
2020-04-09更新
|
489次组卷
|
7卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1第1章 原子结构 易错疑难集训(二)——A学习区 夯实基础(鲁科版选修3)(已下线)易错25 电离能和电负性-备战2021年高考化学一轮复习易错题(已下线)第一单元 原子结构(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)安徽省 淮北师范大学附属实验中学2022-2023学年高二下学期第一次月考化学试题山东省平邑县第一中学2022-2023学年高二下学期第一次月考化学试题广东省湛江市某校2023-2024学年高二下学期第一次月考化学试题
名校
解题方法
3 . 研究人员利用3,3-二氟环丁基胺,成功设计并合成出了首例无铅、多极轴的二维有机—无机杂化钙钛矿铁电体{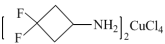 }。该材料表现出了优异的铁电性能、出色的多极轴特性和独特的热致变色性质,有望应用于新一代的多功能智能器件中。请回答下列问题:
}。该材料表现出了优异的铁电性能、出色的多极轴特性和独特的热致变色性质,有望应用于新一代的多功能智能器件中。请回答下列问题:
(1)基态 原子的电子排布式为
原子的电子排布式为_______ 。
(2)3,3-二氟环丁基胺(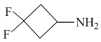 )中所含元素的电负性由强到弱的顺序为
)中所含元素的电负性由强到弱的顺序为_______ (用元素符号表示)。
(3)沸点:
_______ (填“>”或“<”) ,解释其原因:
,解释其原因:_______ 。
(4) 配合物中碳原子的杂化类型是
配合物中碳原子的杂化类型是_______ ,所含化学键的类型为_______ 。
(5)单质铁的晶体在不同温度下有两种堆积方式,分别为面心立方最密堆积和体心立方堆积。则在面心立方晶胞和体心立方晶胞中含有的铁原子的个数之比为_______ 。
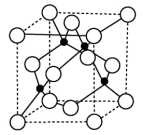
(6)晶体具有自范性及各向异性等特点,造成晶体某些物理性质的各向异性最本质的原因是_______ ;铜与氯形成的晶体的晶胞如图所示,该晶体的化学式为_______ ,已知晶胞边长为 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为_______  。
。
 }。该材料表现出了优异的铁电性能、出色的多极轴特性和独特的热致变色性质,有望应用于新一代的多功能智能器件中。请回答下列问题:
}。该材料表现出了优异的铁电性能、出色的多极轴特性和独特的热致变色性质,有望应用于新一代的多功能智能器件中。请回答下列问题:(1)基态
 原子的电子排布式为
原子的电子排布式为(2)3,3-二氟环丁基胺(
 )中所含元素的电负性由强到弱的顺序为
)中所含元素的电负性由强到弱的顺序为(3)沸点:

 ,解释其原因:
,解释其原因:(4)
 配合物中碳原子的杂化类型是
配合物中碳原子的杂化类型是(5)单质铁的晶体在不同温度下有两种堆积方式,分别为面心立方最密堆积和体心立方堆积。则在面心立方晶胞和体心立方晶胞中含有的铁原子的个数之比为
(6)晶体具有自范性及各向异性等特点,造成晶体某些物理性质的各向异性最本质的原因是
 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。
。
您最近一年使用:0次
2021-09-09更新
|
212次组卷
|
3卷引用:河北省邢台市2021-2022学年高三上学期入学考试化学试题
4 . 甲醛检测试剂盒常用来检测室内空气中甲醛,其原理是甲醛与MBTH反应生成物质A,物质A再发生一系列反应,最终生成蓝绿色化合物,有关转化如图。下列说法正确的是


| A.上述有机物涉及的元素中氮元素的电负性最强 |
| B.甲醛分子结构为平面三角形 |
| C.物质A中的C、N、S一定位于同一个平面内 |
| D.1molMBTH中σ键的数目为22NA |
您最近一年使用:0次
5 . 有机物M(如图所示)是合成某新型绿色农药的中间体,下列说法正确的是
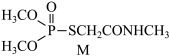
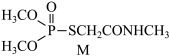
A.中子数为8的碳原子: | B.电负性: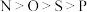 |
C.碳原子的杂化方式为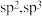 | D.简单离子半径: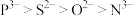 |
您最近一年使用:0次
2023-04-24更新
|
121次组卷
|
3卷引用:河北省邢台市重点高中联考2022-2023学年高二下学期6月月考化学试题
6 . 前四周期原子序数依次增大的元素a、b、c、d中,a和b的价电子层中未成对电子均只有1个。并且a—和b+的电子数相差8;c和d与b位于同一周期,c和d的价电子层中的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:
(1)a元素在元素周期表中的位置是___________ ,属于___________ 区。
(2)基态b原子中。电子占据最高能层的符号是___________ , 基态b+占据的最高能级共有___________ 个原子轨道。
(3)d元素基态原子的简化电子排布式为___________ 。
(4)a、b、c、d四种元素中,电负性最大的为___________ (填元素符号)。
(5)a、b、d三种元素的第一电离能由大到小的顺序为___________ (填元素符号)。
(6)Mn和c两种元素的部分电离能数据如表所示:
比较两元素的I2、 I3可知,气态Mn2+再失去一个电子比气态c2+再失去一个电子更难,原因是___________ 。
(1)a元素在元素周期表中的位置是
(2)基态b原子中。电子占据最高能层的符号是
(3)d元素基态原子的简化电子排布式为
(4)a、b、c、d四种元素中,电负性最大的为
(5)a、b、d三种元素的第一电离能由大到小的顺序为
(6)Mn和c两种元素的部分电离能数据如表所示:
| 元素 | 电离能/(kJ·mol-1) | ||
| I1 | I2 | I3 | |
| c元素 | 759 | 1561 | 2957 |
| Mn元素 | 717 | 1509 | 3248 |
比较两元素的I2、 I3可知,气态Mn2+再失去一个电子比气态c2+再失去一个电子更难,原因是
您最近一年使用:0次
7 . 重水是含有较多 和
和 的水,重水对工农业生成有很大危害,其中含有
的水,重水对工农业生成有很大危害,其中含有 和
和 的重水叫暂时硬水,含有
的重水叫暂时硬水,含有 、
、 、
、 和
和 等的重水叫永久硬水,回答下面问题:
等的重水叫永久硬水,回答下面问题:
(1)画出Ca原子的原子结构示意图___________ ,硫元素在元素周期表的位置___________ ,属于___________ 区。
(2)写出基态N原子的电子排布式___________ ,画出基态O原子的价电子排布图___________ 。基态N原子的第一电离能比O原子的要大的原因是___________ 。
(3)若将基态镁原子最高能级的电子排布图表示为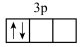 ,则它违背的电子排布规律是
,则它违背的电子排布规律是___________ 、___________ ,基态硫原子核外电子所处最高能级轨道的形状为___________ 。
(4)EDTA是硬水软化常用的化学试剂,与镁离子结合为
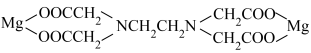
其中C、N、O、Mg四种元素的电负性由大到小的顺序是___________ ,原子半径最大的是___________ (填元素符号,下同),四种元素中基态原子核外单电子数最多的是___________ 。
(5)钙元素与铬元素、铜元素位于同一周期,写出铬、铜基态原子的价电子排布式___________ 、___________ 。
 和
和 的水,重水对工农业生成有很大危害,其中含有
的水,重水对工农业生成有很大危害,其中含有 和
和 的重水叫暂时硬水,含有
的重水叫暂时硬水,含有 、
、 、
、 和
和 等的重水叫永久硬水,回答下面问题:
等的重水叫永久硬水,回答下面问题:(1)画出Ca原子的原子结构示意图
(2)写出基态N原子的电子排布式
(3)若将基态镁原子最高能级的电子排布图表示为
 ,则它违背的电子排布规律是
,则它违背的电子排布规律是(4)EDTA是硬水软化常用的化学试剂,与镁离子结合为
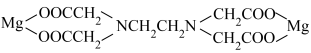
其中C、N、O、Mg四种元素的电负性由大到小的顺序是
(5)钙元素与铬元素、铜元素位于同一周期,写出铬、铜基态原子的价电子排布式
您最近一年使用:0次
名校
8 . A、B、C、D、E 五种元素在周期表中的相对位置如图所示,下列说法正确的是
A | B | ||||
C | D | E |
| A.C的简单离子是它所在周期元素中离子半径最小的离子 |
| B.D和E两元素的氧化物对应水化物的酸性E>D |
| C.B是周期表中电负性最强的元素 |
| D.该五种元素中第一电离能由大到小进行排序为:B>A>E>D>C |
您最近一年使用:0次
名校
9 . 下列各组元素性质的递变情况错误的是
| A.Li、Be、B原子的最外层电子数依次增多 |
| B.P、S、Cl元素的最高化合价依次升高 |
| C.N、O、F电负性依次增大 |
| D.Na、K、Rb第一电离能逐渐增大 |
您最近一年使用:0次
2018-02-10更新
|
682次组卷
|
12卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第2课时
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第2课时河北省邢台市第八中学2018-2019学年高二下学期期末考试化学试题人教版2017-2018学年高二化学选修三同步训练:第一章 原子结构与性质2(已下线)2018年11月26日 《每日一题》一轮复习-元素性质的递变规律福建省平和县第一中学2018-2019学年高二下学期期末考试化学试题(已下线)2019年11月25日 《每日一题》2020年高考化学一轮复习——元素性质的递变规律陕西省宝鸡市金台区2020-2021学年高二下学期期中考试化学试题陕西省宝鸡市渭滨区2020-2021学年高二下学期期末考试化学试题河南省南阳市六校2021-2022学年高二下学期第一次联考化学试题(B)广东省广州市真光中学2021-2022学年高二下学期3月月考化学试题河北省保定市崇德实验中学2020-2021学年度高二下学期期中考试化学试题(已下线)2022年天津市普通高中学业水平等级性考试化学试题变式题(选择题1-4)
解题方法
10 . 下列关于配合物 的说法中正确的是
的说法中正确的是
 的说法中正确的是
的说法中正确的是A.在 中, 中, 给出孤电子对, 给出孤电子对, 提供空轨道 提供空轨道 |
B. 组成元素中电负性最大的元素是氮元素 组成元素中电负性最大的元素是氮元素 |
| C.阴离子的空间结构是平面正方形 |
D. 的空间构型为正四面体形 的空间构型为正四面体形 |
您最近一年使用:0次



