名校
解题方法
1 . C、Si在元素周期表中属于同主族元素,其常见的氧化物分别为CO2、SiO2。请回答下列问题:
(1)锗与碳、硅同主族,写出锗原子基态时的核外电子排布式:____________ 。
(2)C、O、Si三种元素的电负性由大到小的顺序为____________ (用元素符号表示)。
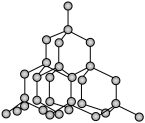
(3)二氧化硅结构跟硅晶体结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察下图中硅晶体的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目为____________ ;晶体硅中硅原子与共价键的数目比为____________ 。
(4)下图是二氧化碳的晶胞模型,从晶体类型来看,CO2属于_______ 晶体。图中显示出的二氧化碳分子数有________ 个,实际上一个二氧化碳晶胞中含有_______ 个二氧化碳分子。标准状况下2.24 L的CO2分子中含有的π键的数目为______ 。
(5)在二氧化碳晶胞中,最近的两个二氧化碳分子间的距离为a nm,NA为阿伏加 德罗常数的值,则晶体密度为____________ g·cm-3。
(1)锗与碳、硅同主族,写出锗原子基态时的核外电子排布式:
(2)C、O、Si三种元素的电负性由大到小的顺序为
(3)二氧化硅结构跟硅晶体结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察下图中硅晶体的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目为
(4)下图是二氧化碳的晶胞模型,从晶体类型来看,CO2属于
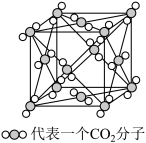
(5)在二氧化碳晶胞中,最近的两个二氧化碳分子间的距离为a nm,NA为阿伏加 德罗常数的值,则晶体密度为
您最近一年使用:0次
2020-09-22更新
|
342次组卷
|
3卷引用:辽宁省朝阳市建平县2021届高三9月联考化学试题
解题方法
2 .  、
、 、
、 、
、 、
、 是元素周期表中前四周期的元素,各周期至少含有一种元素,且原子序数依次增大。
是元素周期表中前四周期的元素,各周期至少含有一种元素,且原子序数依次增大。 、
、 、
、 三种元素原子的最外层电子数相同,
三种元素原子的最外层电子数相同, 与
与 能够形成原子之比为
能够形成原子之比为 的化合物
的化合物 ,
, 是前四周期基态原子含有未成对电子数目最多的元素,
是前四周期基态原子含有未成对电子数目最多的元素, 与
与 形成的晶体
形成的晶体 结构如图所示。试用元素符号回答下列问题:
结构如图所示。试用元素符号回答下列问题:
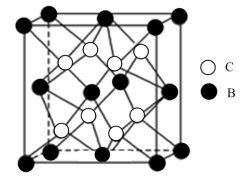
(1) 、
、 、
、 三种元素的电负性由大到小的顺序为
三种元素的电负性由大到小的顺序为_______ 。
(2) 与
与 两种元素能够形成两种常见的化合物,则在这两种化合物分子中,原子的杂化方式分别为
两种元素能够形成两种常见的化合物,则在这两种化合物分子中,原子的杂化方式分别为______ 和______ ,且这两种分子____ (填选项)。
A 都是极性分子 B 都是非极性分子 C 其中一种是极性分子另一种是非极性分子
(3) 元素处于周期表的
元素处于周期表的____ 区,其单质晶体堆积模型的名称为_____ 。
(4) 元素的基态原子价层电子排布图为
元素的基态原子价层电子排布图为______ 。
(5)已知 能溶于某浓度的硝酸中,得到蓝色溶液的同时,会逸出一种与
能溶于某浓度的硝酸中,得到蓝色溶液的同时,会逸出一种与 互为等电子体的纯净气体,则该反应的化学方程式为
互为等电子体的纯净气体,则该反应的化学方程式为_____ 。经研究证实,所得溶液呈蓝色,是因为溶液中含有由 、
、 、
、 三种元素形成的一种配位离子,试写出该离子的结构式
三种元素形成的一种配位离子,试写出该离子的结构式______ 。
(6)由晶体 的晶胞可知,
的晶胞可知, 离子呈简单立方堆积模型,形成立方体空隙,则
离子呈简单立方堆积模型,形成立方体空隙,则 离子对这些立方体空隙的填充率为
离子对这些立方体空隙的填充率为_____  。
。
 、
、 、
、 、
、 、
、 是元素周期表中前四周期的元素,各周期至少含有一种元素,且原子序数依次增大。
是元素周期表中前四周期的元素,各周期至少含有一种元素,且原子序数依次增大。 、
、 、
、 三种元素原子的最外层电子数相同,
三种元素原子的最外层电子数相同, 与
与 能够形成原子之比为
能够形成原子之比为 的化合物
的化合物 ,
, 是前四周期基态原子含有未成对电子数目最多的元素,
是前四周期基态原子含有未成对电子数目最多的元素, 与
与 形成的晶体
形成的晶体 结构如图所示。试用元素符号回答下列问题:
结构如图所示。试用元素符号回答下列问题:
(1)
 、
、 、
、 三种元素的电负性由大到小的顺序为
三种元素的电负性由大到小的顺序为(2)
 与
与 两种元素能够形成两种常见的化合物,则在这两种化合物分子中,原子的杂化方式分别为
两种元素能够形成两种常见的化合物,则在这两种化合物分子中,原子的杂化方式分别为A 都是极性分子 B 都是非极性分子 C 其中一种是极性分子另一种是非极性分子
(3)
 元素处于周期表的
元素处于周期表的(4)
 元素的基态原子价层电子排布图为
元素的基态原子价层电子排布图为(5)已知
 能溶于某浓度的硝酸中,得到蓝色溶液的同时,会逸出一种与
能溶于某浓度的硝酸中,得到蓝色溶液的同时,会逸出一种与 互为等电子体的纯净气体,则该反应的化学方程式为
互为等电子体的纯净气体,则该反应的化学方程式为 、
、 、
、 三种元素形成的一种配位离子,试写出该离子的结构式
三种元素形成的一种配位离子,试写出该离子的结构式(6)由晶体
 的晶胞可知,
的晶胞可知, 离子呈简单立方堆积模型,形成立方体空隙,则
离子呈简单立方堆积模型,形成立方体空隙,则 离子对这些立方体空隙的填充率为
离子对这些立方体空隙的填充率为 。
。
您最近一年使用:0次
名校
解题方法
3 . 碳是地球上组成生命的最基本的元素之一。根据要求回答下列问题:
(1)碳原子的价电子排布式______________ ,核外有_________ 种不同运动状态的电子。
(2)碳可以形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。
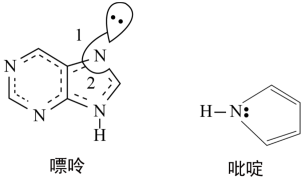
①嘌呤中所有元素的电负性由大到小的顺序__________________ 。
②嘌呤中轨道之间的夹角∠1比∠2大,解释原因__________________ 。
③吡啶结构中N原子的杂化方式__________________ 。
④分子中的大π键可用符号 表示,m代表形成大π键的原子数,n代表参与形成大π键的电子数。则吡啶结构中的大π键表示为
表示,m代表形成大π键的原子数,n代表参与形成大π键的电子数。则吡啶结构中的大π键表示为__________ 。
(3)碳元素能形成CO、CO2、H2CO3等多种无机化合物。
①二氧化碳的晶体叫做干冰,每个二氧化碳分子周围通常有__________ 个紧邻的分子。
②在CO转化成CO2的反应过程中,下列说法正确的是__________ 。
A.分子中孤电子对数不变 B.分子的极性发生变化
C.原子间成键方式发生改变 D.分子晶体的熔沸点升高
③H2CO3与H3PO4均有1个非羟基氧,H3PO4为中强酸,H2CO3为弱酸的原因_________ 。
(4)2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。T-碳的结构是将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代形成碳的一种新型三维立方晶体结构,如下图。已知T碳晶胞参数为a pm,阿伏伽德罗常数为NA,则T碳的密度的表达式为__________ g/cm3。(写出表达式即可)

(1)碳原子的价电子排布式
(2)碳可以形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。

①嘌呤中所有元素的电负性由大到小的顺序
②嘌呤中轨道之间的夹角∠1比∠2大,解释原因
③吡啶结构中N原子的杂化方式
④分子中的大π键可用符号
 表示,m代表形成大π键的原子数,n代表参与形成大π键的电子数。则吡啶结构中的大π键表示为
表示,m代表形成大π键的原子数,n代表参与形成大π键的电子数。则吡啶结构中的大π键表示为(3)碳元素能形成CO、CO2、H2CO3等多种无机化合物。
①二氧化碳的晶体叫做干冰,每个二氧化碳分子周围通常有
②在CO转化成CO2的反应过程中,下列说法正确的是
A.分子中孤电子对数不变 B.分子的极性发生变化
C.原子间成键方式发生改变 D.分子晶体的熔沸点升高
③H2CO3与H3PO4均有1个非羟基氧,H3PO4为中强酸,H2CO3为弱酸的原因
(4)2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。T-碳的结构是将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代形成碳的一种新型三维立方晶体结构,如下图。已知T碳晶胞参数为a pm,阿伏伽德罗常数为NA,则T碳的密度的表达式为

您最近一年使用:0次
2018-04-14更新
|
364次组卷
|
2卷引用:辽宁省大连市2018年高三第一次模拟考试理科综合试卷化学试题



