1 . Fe、Co、Ni、Cu均为第四周期元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Fe原子的核外电子中,两种自旋状态的电子数之比为___________ 。在空气中FeO稳定性小于 ,从电子排布的角度分析,其主要原因是
,从电子排布的角度分析,其主要原因是___________ 。
(2) 可形成
可形成 ,其中en代表
,其中en代表 。该化合物分子中,VSEPR模型为四面体的非金属原子共有
。该化合物分子中,VSEPR模型为四面体的非金属原子共有___________ 个;C、N、B的电负性由小到大的顺序为___________ 。
(3)基态 的核外电子排布式为
的核外电子排布式为___________ ; 常温下为无色液体,写出两种与CO互为等电子体离子的化学式
常温下为无色液体,写出两种与CO互为等电子体离子的化学式___________ 、___________ 。
(4)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为___________ ;该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点、B点原子的分数坐标分别为 、
、 ,则c点原子的分数坐标为
,则c点原子的分数坐标为___________ ;晶胞中C、D间距离d=___________ pm。
(1)基态Fe原子的核外电子中,两种自旋状态的电子数之比为
 ,从电子排布的角度分析,其主要原因是
,从电子排布的角度分析,其主要原因是(2)
 可形成
可形成 ,其中en代表
,其中en代表 。该化合物分子中,VSEPR模型为四面体的非金属原子共有
。该化合物分子中,VSEPR模型为四面体的非金属原子共有(3)基态
 的核外电子排布式为
的核外电子排布式为 常温下为无色液体,写出两种与CO互为等电子体离子的化学式
常温下为无色液体,写出两种与CO互为等电子体离子的化学式(4)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为
 、
、 ,则c点原子的分数坐标为
,则c点原子的分数坐标为
您最近一年使用:0次
解题方法
2 . 铜是人类广泛使用的一种金属,含铜物质在生产生活中有着广泛应用。回答下列问题:
(1)基态Cu原子的价电子排布式为_______ , 原子核外的电子有_______ 种空间运动状态。
(2)配合物Cu(NH3)2OOCCH3中,铜显+1价,则其中碳原子的杂化轨道类型是_______ ,NH3分子的价层电子对互斥模型是_______ ,C、N、O、H的电负性由大到小的顺序为_______ 。
(3)Cu+与CN-形成的阴离子为[Cu(CN)3]2- ,该阴离子中σ键与π键数目之比为_______ 。
(4)铜能与拟卤素(SCN)2反应。拟卤素(SCN)2对应的酸有两种,理论上异硫氰酸(H-N=C=S)的沸点高于硫氰酸(H-S-C≡N),其原因为_______ 。
(5)某立方磷青铜晶体的晶胞结构如图所示。
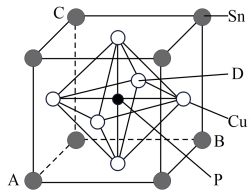
①原子分数坐标可表示晶胞内部各原子的相对位置,图中各原子分数坐标:A为(0,0,0),B为(1,1,0),C为(0,1,1),则D原子的分数坐标为_______ 。
②若晶体密度为ρg·cm-3 ,最近的Cu原子核间距为_______ (用含ρ、NA的代数式表示)pm。
(1)基态Cu原子的价电子排布式为
(2)配合物Cu(NH3)2OOCCH3中,铜显+1价,则其中碳原子的杂化轨道类型是
(3)Cu+与CN-形成的阴离子为[Cu(CN)3]2- ,该阴离子中σ键与π键数目之比为
(4)铜能与拟卤素(SCN)2反应。拟卤素(SCN)2对应的酸有两种,理论上异硫氰酸(H-N=C=S)的沸点高于硫氰酸(H-S-C≡N),其原因为
(5)某立方磷青铜晶体的晶胞结构如图所示。

①原子分数坐标可表示晶胞内部各原子的相对位置,图中各原子分数坐标:A为(0,0,0),B为(1,1,0),C为(0,1,1),则D原子的分数坐标为
②若晶体密度为ρg·cm-3 ,最近的Cu原子核间距为
您最近一年使用:0次
名校
解题方法
3 . 主族元素N、F、Si、As、Se、Cl等的某些化合物对工农业生产意义重大,回答下列问题:
(1)Si3N4陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于_______ 晶体;SiCl4中Si采取的杂化类型为_______ 。
(2)O、F、Cl电负性由大到小的顺序为_______ ;OF2分子的空间构型为_______ ;OF2的熔、沸点低于Cl2O,原因是_______ 。
(3)Se元素基态原子的原子核外电子排布式为_______ ;As的第一电离能比Se的第一电离能大的原因为_______ 。
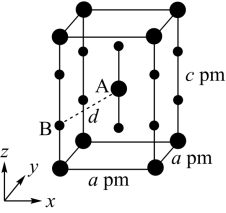
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______ 个XeF2分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,
, ,
, )。已知Xe-F键长为rpm,则B点原子的分数坐标为
)。已知Xe-F键长为rpm,则B点原子的分数坐标为_______ ;晶胞中A、B间距离d=_______ pm。
(1)Si3N4陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于
(2)O、F、Cl电负性由大到小的顺序为
(3)Se元素基态原子的原子核外电子排布式为
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
 ,
, ,
, )。已知Xe-F键长为rpm,则B点原子的分数坐标为
)。已知Xe-F键长为rpm,则B点原子的分数坐标为
您最近一年使用:0次
2022-05-02更新
|
860次组卷
|
7卷引用:陕西省汉中市2022届高三教学质量第二次检测考试理科综合能力测试化学试题
陕西省汉中市2022届高三教学质量第二次检测考试理科综合能力测试化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)(已下线)专题18物质结构与性质(选修)-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题17物质结构与性质(综合题)-2022年高考真题+模拟题汇编(全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)四川省绵阳南山中学2022-2023学年高三上学期入学考试理综化学试题山东省枣庄市第三中学2022-2023学年高三上学期期中考试化学试题
名校
解题方法
4 . 镁、铝、铁、铜及其化合物在生产生活中具有广泛的应用。
(1)基态铝原子核外电子占据的最高能级符号为____ ,该能级原子轨道数为____ ,电子云轮廓图为_____ ;基态铁原子价层电子未成对电子数为_____ 。
(2)第一电离能镁_____ 铝(填>、<、=)
(3)CuSO4·5H2O俗名胆矾矾,可用于配制农药和游泳池消毒,其组成可表示为[Cu(H2O)4]SO4·H2O。晶体中含有的化学键类型为_______
a.离子键 b.共价键 c.配位键 d.氢键 e.金属键
(4)FeSO4·7H2O俗称绿矾,在空气中加热分解可能得到Fe2O3、H2O、SO2、SO3等,其中CuO的熔点为1026℃。
①H2O分子中氧原子的杂化类型是______ ,分子的立体构型是_____ 。组成绿矾的元素中电负性最大的元素是______ ,
②CuO的晶体类型是_____ 。
③SO2与SO3中,属于非极性分子的是______ ,SO2在溶剂水与溶剂CCl4中,相同温度能溶解更多SO2的溶剂是________
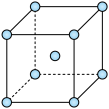
④铁的晶胞结构如图,若晶胞参数为acm,阿伏加德罗常数值为NA,则晶体的密度为___________ g/cm3。
(1)基态铝原子核外电子占据的最高能级符号为
(2)第一电离能镁
(3)CuSO4·5H2O俗名胆矾矾,可用于配制农药和游泳池消毒,其组成可表示为[Cu(H2O)4]SO4·H2O。晶体中含有的化学键类型为
a.离子键 b.共价键 c.配位键 d.氢键 e.金属键
(4)FeSO4·7H2O俗称绿矾,在空气中加热分解可能得到Fe2O3、H2O、SO2、SO3等,其中CuO的熔点为1026℃。
①H2O分子中氧原子的杂化类型是
②CuO的晶体类型是
③SO2与SO3中,属于非极性分子的是
④铁的晶胞结构如图,若晶胞参数为acm,阿伏加德罗常数值为NA,则晶体的密度为

您最近一年使用:0次
名校
解题方法
5 . 2013年绵阳科博会场馆,大量的照明材料或屏幕都使用了发光的二极管(LED)。目前市售LED铝片,材质基本以GaAs(砷化镓)、AlGaInP(氮化铟镓)为主。已知砷化镓的晶胞结构如图。试回答:

(1)镓的基态原子的外围电子排布式是_______________ 。
(2)镓与钾、钙元素的第一电离能从大到小依次为_________________________ ,与其在同一周期的砷、硒和溴的电负性从大到小依次为_______________ 。(填元素符号)
(3)此晶胞中所含的砷原子(白色球)个数为_______ ,与同一个镓原子相连的砷原子构成的立体构型为___________ ,镓采取的杂化方式为________________ 。
(4)与镓同主族的元素硼形成的最高价氧化物对应水化物化学式为_____________________ ,其结构式为_____________ ,硼酸是_______ 元酸。
(5)若砷和镓两元素的相对原子质量分别为a,b,GaAs晶体结构图中相距最近的两个原子的距离为dnm,晶胞参数为________ cm,NA表示阿伏伽德罗常数,则该晶体的密度为________ g/cm3。

(1)镓的基态原子的外围电子排布式是
(2)镓与钾、钙元素的第一电离能从大到小依次为
(3)此晶胞中所含的砷原子(白色球)个数为
(4)与镓同主族的元素硼形成的最高价氧化物对应水化物化学式为
(5)若砷和镓两元素的相对原子质量分别为a,b,GaAs晶体结构图中相距最近的两个原子的距离为dnm,晶胞参数为
您最近一年使用:0次



