名校
解题方法
1 . 氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。按要求回答下列问题:
(1)氢化钠( )是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为
)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为___________ 。
(2)钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态钛的价层电子排布式为___________ 。
(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(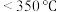 )而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
)而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成,则涉及的元素H、B、C、N、O电负性最大的是
进行合成,则涉及的元素H、B、C、N、O电负性最大的是___________ ,键角:
___________  (填“
(填“ ”或“
”或“ ”)。
”)。
(4)咔唑(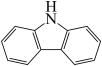 )是一种新型有机液体储氢材料,它的沸点比(
)是一种新型有机液体储氢材料,它的沸点比(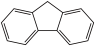 )的高,其主要原因是
)的高,其主要原因是___________ 。
(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
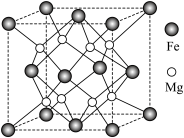
①距离 原子最近的
原子最近的 原子个数是
原子个数是___________ 。
②铁镁合金的化学式为___________ 。
③若该晶胞的晶胞边长为dnm,阿伏加德罗常数为NA,则该合金的密度为___________  。
。
④若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下 的体积约为
的体积约为___________ L。
(1)氢化钠(
 )是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为
)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为(2)钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态钛的价层电子排布式为
(3)
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(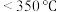 )而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
)而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成,则涉及的元素H、B、C、N、O电负性最大的是
进行合成,则涉及的元素H、B、C、N、O电负性最大的是
 (填“
(填“ ”或“
”或“ ”)。
”)。(4)咔唑(
 )是一种新型有机液体储氢材料,它的沸点比(
)是一种新型有机液体储氢材料,它的沸点比( )的高,其主要原因是
)的高,其主要原因是(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离
 原子最近的
原子最近的 原子个数是
原子个数是②铁镁合金的化学式为
③若该晶胞的晶胞边长为dnm,阿伏加德罗常数为NA,则该合金的密度为
 。
。④若该晶体储氢时,
 分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下 的体积约为
的体积约为
您最近一年使用:0次
2023-05-25更新
|
342次组卷
|
3卷引用:宁夏石嘴山市第三中学2023-2024学年高三上学期第二次月考 化学试题
解题方法
2 . 2019 年诺贝尔化学奖授予三位开发锂离子电池的科学家。TiS2、LiCoO2和 LiMnO2等都是他们研究锂离子电池的载体。回答下列问题:
(1)基态 Ti 原子的价层电子排布图为____ 。
(2)在第四周期 d 区元素中,与 Ti 原子未成对电子数相同的元素名称________ 。
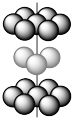
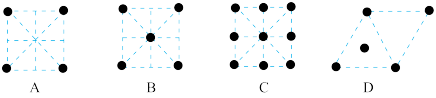
(3)金属钛的原子堆积方式如图所示,则金属钛晶胞俯视图为______ 。
(4)已知第三电离能数据:I3(Mn)=3246 kJ·mol-1,I3(Fe)=2957 kJ·mol-1。锰的第三电离能大于铁的第三电离能,其主要原因是______ 。
(5)据报道,在 MnO2的催化下,甲醛可被氧化成 CO2,在处理含 HCHO 的废水或空气方面有广泛应用。HCHO中键角________ CO2中键角(填“大于”“小于”或“等于”)。
(6)Co3+、Co2+能与 NH3、H2O、SCN-等配体组成配合物。
①1 mol[ Co(NH3)6]3+含______ mol σ键。
②配位原子提供孤电子对与电负性有关,电负性越大,对孤电子对吸引力越大。SCN-的结构式为[S=C=N] -,SCN-与金属离子形成的配离子中配位原子是_______ (填元素符号)。
(7)工业上,采用电解熔融氯化锂制备锂,钠还原 TiCl4(g)制备钛。已知:LiCl、TiCl4的熔点分别为 605℃、-24℃,它们的熔点相差很大,其主要原因是________ 。
(8)钛的化合物晶胞如图所示。
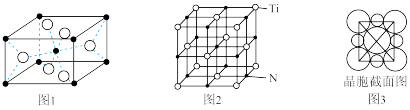
二氧化钛晶胞如图 1 所示,钛原子配位数为______ 。氮化钛的晶胞如图 2 所示, 图 3 是氮化钛的晶胞截面图(相邻原子两两相切)。已知:NA是阿伏加 德罗常数的值,氮化钛晶体密度为 d g·cm-3。氮化钛晶胞中 N 原子半径为________ pm。
(1)基态 Ti 原子的价层电子排布图为
(2)在第四周期 d 区元素中,与 Ti 原子未成对电子数相同的元素名称
(3)金属钛的原子堆积方式如图所示,则金属钛晶胞俯视图为


(4)已知第三电离能数据:I3(Mn)=3246 kJ·mol-1,I3(Fe)=2957 kJ·mol-1。锰的第三电离能大于铁的第三电离能,其主要原因是
(5)据报道,在 MnO2的催化下,甲醛可被氧化成 CO2,在处理含 HCHO 的废水或空气方面有广泛应用。HCHO中键角
(6)Co3+、Co2+能与 NH3、H2O、SCN-等配体组成配合物。
①1 mol[ Co(NH3)6]3+含
②配位原子提供孤电子对与电负性有关,电负性越大,对孤电子对吸引力越大。SCN-的结构式为[S=C=N] -,SCN-与金属离子形成的配离子中配位原子是
(7)工业上,采用电解熔融氯化锂制备锂,钠还原 TiCl4(g)制备钛。已知:LiCl、TiCl4的熔点分别为 605℃、-24℃,它们的熔点相差很大,其主要原因是
(8)钛的化合物晶胞如图所示。

二氧化钛晶胞如图 1 所示,钛原子配位数为
您最近一年使用:0次
名校
解题方法
3 . 碳、 氮、磷、砷和硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。锂、钠、铝、铁等金属在日常生活、工业生产中也占有举足轻重的地位,请回答下列问题:
(1)基态As原子的电子排布式为[Ar]______________________ ;
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B—N—B之间的夹角是___________________ (填角度)。
(3)砷化硼(BAs)是ⅢA一VA族半导体材料的重要成员之一,其晶体结构与金刚石相似。
①BAs晶体中,每个As与____________ 个B相连,As的杂化形式为_______________ ;
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有____________ (填字母)。
A.离子键 B.金属键 C.极性键 D.氢键 E.配位键 F.σ键 G.π键
(4)铁的另一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于________________________________ (填晶体类型)。
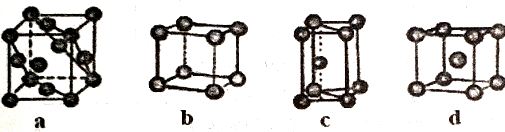
(5)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为___________ (填字母)。
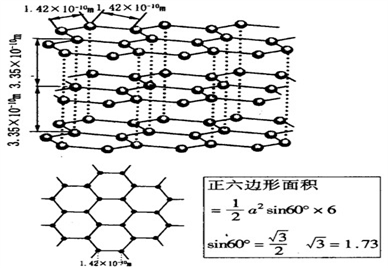
(6)石墨晶体的结构如下图,石墨的密度为________________________________ (只列式不化简不计算)
(1)基态As原子的电子排布式为[Ar]
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B—N—B之间的夹角是
(3)砷化硼(BAs)是ⅢA一VA族半导体材料的重要成员之一,其晶体结构与金刚石相似。
①BAs晶体中,每个As与
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有
A.离子键 B.金属键 C.极性键 D.氢键 E.配位键 F.σ键 G.π键
(4)铁的另一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于
(5)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为

(6)石墨晶体的结构如下图,石墨的密度为

您最近一年使用:0次



