解题方法
1 . 铁元素在人体健康和新材料研发中有重要的应用。
I.在血液中,以 为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送
为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送 ,下图为载氧后的血红蛋白分子示意图:
,下图为载氧后的血红蛋白分子示意图:_________ 。
(2)载氧时,血红蛋白分子中 脱去配位的
脱去配位的 并与
并与 配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与
配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与 配位能力最强的是
配位能力最强的是_________ (填字母)。
a. b.
b. c.CO
c.CO
(3)一种最简单的卟啉环结构如图:_________ 。
②比较C和N的电负性大小,并从原子结构角度说明理由:_________ 。
③该卟啉分子在酸性环境中配位能力会减弱,原因是_________ 。
Ⅱ. 可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为a pm。
可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为a pm。 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
(4)该晶体的密度是_________  。
。
(5)距离F最近的Cs的个数为_________ 。
I.在血液中,以
 为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送
为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送 ,下图为载氧后的血红蛋白分子示意图:
,下图为载氧后的血红蛋白分子示意图: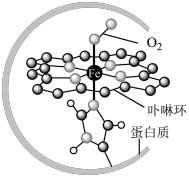
(2)载氧时,血红蛋白分子中
 脱去配位的
脱去配位的 并与
并与 配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与
配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与 配位能力最强的是
配位能力最强的是a.
 b.
b. c.CO
c.CO (3)一种最简单的卟啉环结构如图:
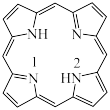
②比较C和N的电负性大小,并从原子结构角度说明理由:
③该卟啉分子在酸性环境中配位能力会减弱,原因是
Ⅱ.
 可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为a pm。
可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为a pm。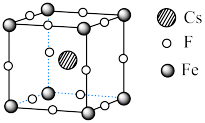
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。(4)该晶体的密度是
 。
。(5)距离F最近的Cs的个数为
您最近一年使用:0次
解题方法
2 . 含硼物质在生产生活中有着广泛应用。回答下列问题:
(1)基态硼原子的价电子轨道表示式是___________ ,最高能量的原子轨道的空间形状是___________ 。
(2)BN可以水解成硼酸(H3BO3)和NH3,B、N、O中,第一电离能最大的元素是___________ 。人工合成的一种BN晶体硬度已超过金刚石,是一种超硬材料,常用作刀具材料和磨料。可预测该BN晶体属于___________ 晶体。用___________ 法可以测得该晶体的结构,其中B的化合价为___________ ,请解释原因:___________ 。
(3)N-甲基咪唑的结构为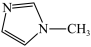 ,它的某种衍生物与NaBF4形成的离子化合物
,它的某种衍生物与NaBF4形成的离子化合物 是离子液体。离子液体是在室温和接近室温时呈液态的盐类物质,由于其具有良好的化学稳定性,较低的熔点和良好的溶解性,应用越来越广泛。
是离子液体。离子液体是在室温和接近室温时呈液态的盐类物质,由于其具有良好的化学稳定性,较低的熔点和良好的溶解性,应用越来越广泛。
①0.3 mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ热量,其热化学方程式为___________ ;
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一、以NaBH4为硼源、某配合物为氨源可用于制备氨硼烷。为测定该配合物的结构,取2.32 g配合物进行如下实验:用重量法分析金属元素,测得镍元素的质量为0.59 g;在碱性条件下加热蒸出NH3,用滴定法测出其物质的量为0.06 mol;滴加过量硝酸银溶液,有白色沉淀生成,加热,沉淀没有增加;用摩尔法分析含量,测得氯元素质量为0.71 g。
I.该配合物中镍离子的基态电子排布式为___________ 。
Ⅱ.该配合物的结构简式为___________ 。
(1)基态硼原子的价电子轨道表示式是
(2)BN可以水解成硼酸(H3BO3)和NH3,B、N、O中,第一电离能最大的元素是
(3)N-甲基咪唑的结构为
 ,它的某种衍生物与NaBF4形成的离子化合物
,它的某种衍生物与NaBF4形成的离子化合物 是离子液体。离子液体是在室温和接近室温时呈液态的盐类物质,由于其具有良好的化学稳定性,较低的熔点和良好的溶解性,应用越来越广泛。
是离子液体。离子液体是在室温和接近室温时呈液态的盐类物质,由于其具有良好的化学稳定性,较低的熔点和良好的溶解性,应用越来越广泛。①1mol离子化合物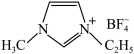 中,阿伏加德罗常数的值为NA,则根据价电子对互斥(VSEPR)理论,杂化方式为sp3的原子共有
中,阿伏加德罗常数的值为NA,则根据价电子对互斥(VSEPR)理论,杂化方式为sp3的原子共有 的电子式为
的电子式为
②离子化合物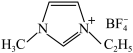 熔点低的原因是
熔点低的原因是
①0.3 mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ热量,其热化学方程式为
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一、以NaBH4为硼源、某配合物为氨源可用于制备氨硼烷。为测定该配合物的结构,取2.32 g配合物进行如下实验:用重量法分析金属元素,测得镍元素的质量为0.59 g;在碱性条件下加热蒸出NH3,用滴定法测出其物质的量为0.06 mol;滴加过量硝酸银溶液,有白色沉淀生成,加热,沉淀没有增加;用摩尔法分析含量,测得氯元素质量为0.71 g。
I.该配合物中镍离子的基态电子排布式为
Ⅱ.该配合物的结构简式为
您最近一年使用:0次
名校
解题方法
3 . 甲硅烷 可用于制备多种新型无机非金属材料。
可用于制备多种新型无机非金属材料。
(1) 原子与
原子与 原子结合时,
原子结合时, 表现为正价,则电负性:
表现为正价,则电负性:
___________ H(填“>”“<”或“=”), 分子的空间结构为
分子的空间结构为___________ 。
(2)利用 与
与 反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。

①碳化硅晶体中每个 原子周围距离最近的
原子周围距离最近的 原子数目为
原子数目为________ , 的晶体类型是
的晶体类型是_______ 。
②基态 原子的价层电子轨道表达式为
原子的价层电子轨道表达式为___________ 。
(3)利用 与
与 可制得氮化硅(
可制得氮化硅( )材料。
)材料。
①热稳定性:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
② 中
中 的键角
的键角___________  中
中 的键角(填“>”“<”或“=”),其键角差异的原因是
的键角(填“>”“<”或“=”),其键角差异的原因是___________ 。
 可用于制备多种新型无机非金属材料。
可用于制备多种新型无机非金属材料。(1)
 原子与
原子与 原子结合时,
原子结合时, 表现为正价,则电负性:
表现为正价,则电负性:
 分子的空间结构为
分子的空间结构为(2)利用
 与
与 反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
①碳化硅晶体中每个
 原子周围距离最近的
原子周围距离最近的 原子数目为
原子数目为 的晶体类型是
的晶体类型是②基态
 原子的价层电子轨道表达式为
原子的价层电子轨道表达式为(3)利用
 与
与 可制得氮化硅(
可制得氮化硅( )材料。
)材料。①热稳定性:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②
 中
中 的键角
的键角 中
中 的键角(填“>”“<”或“=”),其键角差异的原因是
的键角(填“>”“<”或“=”),其键角差异的原因是
您最近一年使用:0次
名校
解题方法
4 . 镍是一种银白色金属,具有良好的机械强度和延展性,常用来制造货币等,镀在其他金属上可以防止生锈。回答下列问题:
(1)基态 原子核外电子的运动状态有
原子核外电子的运动状态有_______ 种,价层电子轨道表示式(电子排布图)为_______ ;
(2)镍不溶于水,在稀酸中可缓慢溶解,生成 。用丁二酮肟
。用丁二酮肟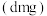 鉴定
鉴定 的存在时生成鲜红色的沉淀,
的存在时生成鲜红色的沉淀,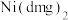 的结构如图所示。
的结构如图所示。
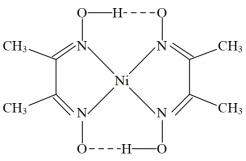
①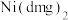 中所含的作用力有
中所含的作用力有_______ (填字母序号)。
A.极性键 B.非极性键 C.离子键 D.配位键 E.氢键
②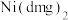 中所含非金属元素电负性由大到小的顺序是
中所含非金属元素电负性由大到小的顺序是_______ ,N原子的杂化方式为_______ 。
③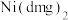 中
中 与N成键,而非和O成键的原因可能是
与N成键,而非和O成键的原因可能是_______ 。
(3)某铜镍合金立方晶胞结构如图所示:

①元素铜和镍的第二电离能分别为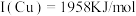 、
、 的原因是
的原因是_______ 。
②该晶体的化学式为_______ ,铜原子距离最近的 有
有_______ 个,已知该晶体的密度为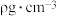 ,晶胞边长
,晶胞边长
_______ nm(用 表示阿伏加德罗常数的值,列出计算式即可,相对原子质量:
表示阿伏加德罗常数的值,列出计算式即可,相对原子质量: )。
)。
(1)基态
 原子核外电子的运动状态有
原子核外电子的运动状态有(2)镍不溶于水,在稀酸中可缓慢溶解,生成
 。用丁二酮肟
。用丁二酮肟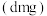 鉴定
鉴定 的存在时生成鲜红色的沉淀,
的存在时生成鲜红色的沉淀,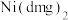 的结构如图所示。
的结构如图所示。
①
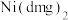 中所含的作用力有
中所含的作用力有A.极性键 B.非极性键 C.离子键 D.配位键 E.氢键
②
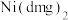 中所含非金属元素电负性由大到小的顺序是
中所含非金属元素电负性由大到小的顺序是③
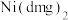 中
中 与N成键,而非和O成键的原因可能是
与N成键,而非和O成键的原因可能是(3)某铜镍合金立方晶胞结构如图所示:

①元素铜和镍的第二电离能分别为
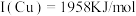 、
、 的原因是
的原因是②该晶体的化学式为
 有
有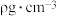 ,晶胞边长
,晶胞边长
 表示阿伏加德罗常数的值,列出计算式即可,相对原子质量:
表示阿伏加德罗常数的值,列出计算式即可,相对原子质量: )。
)。
您最近一年使用:0次



