名校
解题方法
1 . 乙炔是有机合成工业的一种重要原料。工业上曾用焦炭制备电石 (CaC2),再与水反应制备乙炔。
(1)焦炭、金刚石和C60都是碳的单质。已知金刚石中碳碳键的键长为154.45pm,C60中碳碳键的键长为140~145pm ,二者比较熔点高的是_______ ,理由是_______ 。
(2)乙炔与氢氰酸反应可得丙烯腈 ,丙烯腈分子中碳原子轨道杂化类型是
,丙烯腈分子中碳原子轨道杂化类型是_______ ,该分子中 键与
键与 键个数比为
键个数比为_______ 。
(3)将乙炔通入 溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为
溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为_______ ; 的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:
的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:_______ 。
(4)CaC2中C 与O
与O 互为等电子体,O
互为等电子体,O 的电子式为
的电子式为_______ 。
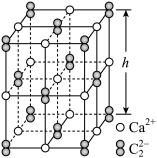
(5)CaC2晶体的晶胞结构与NaCl晶体相似,但CaC2晶体中哑铃形C 的存在,使晶胞沿一个方向拉长,晶胞呈长方体(如图)。每个Ca2+周围距离相等且最近的C
的存在,使晶胞沿一个方向拉长,晶胞呈长方体(如图)。每个Ca2+周围距离相等且最近的C 有
有_______ 个;已知CaC2晶体密度为 ,晶胞中两个C
,晶胞中两个C 的最近距离为acm,阿伏加德罗常数值为NA,则CaC2晶胞中棱长h=
的最近距离为acm,阿伏加德罗常数值为NA,则CaC2晶胞中棱长h=_______ cm。
(6)钾和铜都是第四周期元素,且原子的最外层电子数相同,铜的熔沸点远大于钾的原因是_______ 。
(7)CuSO4·5H2O结构示意图如下,CuSO4·5H2O中存在的相互作用有_______ (填序号,下同),加热该蓝色胆矾晶体得到白色硫酸铜固体破坏的相互作用有_______ 。

A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键
(1)焦炭、金刚石和C60都是碳的单质。已知金刚石中碳碳键的键长为154.45pm,C60中碳碳键的键长为140~145pm ,二者比较熔点高的是
(2)乙炔与氢氰酸反应可得丙烯腈
 ,丙烯腈分子中碳原子轨道杂化类型是
,丙烯腈分子中碳原子轨道杂化类型是 键与
键与 键个数比为
键个数比为(3)将乙炔通入
 溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为
溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为 的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:
的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:(4)CaC2中C
 与O
与O 互为等电子体,O
互为等电子体,O 的电子式为
的电子式为(5)CaC2晶体的晶胞结构与NaCl晶体相似,但CaC2晶体中哑铃形C
 的存在,使晶胞沿一个方向拉长,晶胞呈长方体(如图)。每个Ca2+周围距离相等且最近的C
的存在,使晶胞沿一个方向拉长,晶胞呈长方体(如图)。每个Ca2+周围距离相等且最近的C 有
有 ,晶胞中两个C
,晶胞中两个C 的最近距离为acm,阿伏加德罗常数值为NA,则CaC2晶胞中棱长h=
的最近距离为acm,阿伏加德罗常数值为NA,则CaC2晶胞中棱长h=
(6)钾和铜都是第四周期元素,且原子的最外层电子数相同,铜的熔沸点远大于钾的原因是
(7)CuSO4·5H2O结构示意图如下,CuSO4·5H2O中存在的相互作用有

A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键
您最近一年使用:0次
名校
解题方法
2 . HCHO与[Zn(CN)4]2—在水溶液中发生反应:4HCHO+[Zn(CN)4]2—+4H++4H2O=[Zn(H2O)4]2-+4HOCH2CN,下列说法正确的是
| A.甲醛(HCHO)的键角约为120°,分子之间存在氢键 |
| B.HCN的空间构型为直线形,中心原子的杂化方式为sp |
| C.与Zn2+的配位能力:CN—<H2O |
| D.Zn2+与CN—-生成的配离子[Zn(CN)4]2-中,σ键和π键的数目之比为2:1 |
您最近一年使用:0次
2021-12-30更新
|
457次组卷
|
2卷引用:山东省威海乳山市2021-2022学年高二上学期期中考试化学试题
3 . 酸性溶液中过氧化氢能使Cr2O 转化成蓝色的过氧化铬(CrO5,分子结构为
转化成蓝色的过氧化铬(CrO5,分子结构为 ),该反应可用来检验Cr2O
),该反应可用来检验Cr2O 的存在,其反应的离子方程式为4H2O2+Cr2O
的存在,其反应的离子方程式为4H2O2+Cr2O +2H+=2CrO5+5H2O。下列说法正确的是
+2H+=2CrO5+5H2O。下列说法正确的是
 转化成蓝色的过氧化铬(CrO5,分子结构为
转化成蓝色的过氧化铬(CrO5,分子结构为 ),该反应可用来检验Cr2O
),该反应可用来检验Cr2O 的存在,其反应的离子方程式为4H2O2+Cr2O
的存在,其反应的离子方程式为4H2O2+Cr2O +2H+=2CrO5+5H2O。下列说法正确的是
+2H+=2CrO5+5H2O。下列说法正确的是| A.过氧化铬中铬元素的化合价为+5 | B.1 mol CrO5分子中含有σ键数为6NA |
| C.CrO5分子中既有极性键又有非极性键 | D.该反应中H2O2表现了还原性 |
您最近一年使用:0次
2021-09-15更新
|
1205次组卷
|
14卷引用:山东省泰安肥城市2021-2022学年高三上学期第一次摸底考试化学试题
山东省泰安肥城市2021-2022学年高三上学期第一次摸底考试化学试题山东省滨州市博兴县第二中学2021-2022学年高三上学期第一次月考化学试题山东省济宁市嘉祥县第一中学2022届高三10月月考化学试题河南省郑州市维纲中学2022届高三9月月考化学试题辽宁省沈阳市郊联体2022届高三下学期4月份线上考试化学试题湖南省岳阳县第一中学2022届高三下学期期中考试化学试题(已下线)三轮冲刺卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)(已下线)三轮冲刺卷2-【赢在高考黄金20卷】备战2022年高考化学模拟卷(辽宁专用)广东省汕头市金山中学2023届高三下学期一模化学试题(已下线)专题06 物质结构与性质福建省厦门外国语学校2022-2023学年高二下学期期中考试化学试题江苏省建湖高级中学2023-2024学年高三上学期暑期学情检测(一)化学试题福建省厦门第一中学2023-2024学年高二下学期第一次月考化学试题广东省东山中学2023-2024学年高三上学期期末考试化学试题
解题方法
4 . 2021年5月15日,天问一号探测器成功着陆于火星。据了解火星上存在大量的含氮化合物,科学家推测火星生命可能主要以氮、碳、硅、铜为基体构成。请回答下列问题:
(1)邻氨基吡啶( )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由小到大的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由小到大的顺序为___________ (填元素符号)。基态N原子核外电子的运动状态有___________ 种,设NA为阿伏加德罗常数的值,1 mol 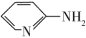 中含有σ键的数目为
中含有σ键的数目为___________ 。
(2)SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为___________ 。SiCl4可发生水解反应,机理如下:

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为___________ (填标号)。SiCl4的熔沸点___________ (填“高于”或“低于”)CCl4,原因是___________ 。
(3)一种鸟嘌呤和吡咯的结构如图。
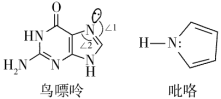
①鸟嘌呤中轨道之间的夹角∠1___________ ∠2(填“>”或“<”)
②分子中的大π键可以用符号π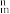 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为___________ 。
(4)火星岩石中存在大量的氮化镓,氮化镓为六方晶胞,结构如图所示。

若该晶体密度为d g·cm-3,晶胞参数a=b≠c(单位:nm),a、b夹角为120°,阿伏加德罗常数的值为NA,则晶胞参数c=___________ nm(写出代数式)。
(1)邻氨基吡啶(
 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由小到大的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由小到大的顺序为 中含有σ键的数目为
中含有σ键的数目为(2)SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(3)一种鸟嘌呤和吡咯的结构如图。

①鸟嘌呤中轨道之间的夹角∠1
②分子中的大π键可以用符号π
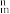 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为(4)火星岩石中存在大量的氮化镓,氮化镓为六方晶胞,结构如图所示。

若该晶体密度为d g·cm-3,晶胞参数a=b≠c(单位:nm),a、b夹角为120°,阿伏加德罗常数的值为NA,则晶胞参数c=
您最近一年使用:0次
5 . 茶文化是中国人民对世界饮食文化的一大贡献,茶叶中含有少量的咖啡因(结构简式如图)。下列关于咖啡因的说法错误的是
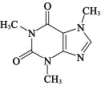

| A.咖啡因的组成元素均位于元素周期表p区 |
| B.咖啡因分子中C、N 均有 sp2、sp3两种杂化方式 |
| C.咖啡因与足量 H2加成的产物含有 4 个手性碳原子 |
| D.咖啡因分子间存在氢键 |
您最近一年使用:0次
解题方法
6 . 锂单质及化合物用途广泛,涉及电池、陶瓷、玻璃、润滑剂、制冷液、核工业等领域。
(1)锂离子电池的电解液有LiBF4,等,碳酸亚乙酯(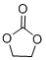 )用作该电解液的添加剂。
)用作该电解液的添加剂。
①LiBF4中阴离子的空间构型为_______ ,LiBF4中不存在______ (填序号)。
A.离子键 B.极性共价键 C.配位键 D.氢键
②碳酸亚乙酯分子中σ键与π键数目之比为______ 。酯密度一般比水小,难溶于水,而碳酸亚乙酯能溶于水的主要原因是______ 。
(2)碱金属在空气中燃烧时,只有锂生成普通氧化物 。
。 是离子晶体,其晶格能可通过下图的
是离子晶体,其晶格能可通过下图的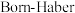 循环计算得到。
循环计算得到。
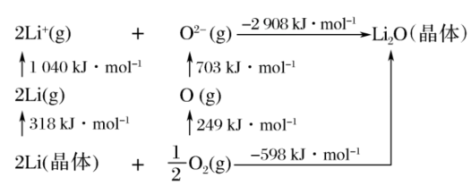
①由图中数据可知O=O键键能为___________  ,
, 晶格能为
晶格能为___________  。
。
② 和
和 的熔点如下表所示:
的熔点如下表所示:
熔点差异的原因是___________ 。
(1)锂离子电池的电解液有LiBF4,等,碳酸亚乙酯(
 )用作该电解液的添加剂。
)用作该电解液的添加剂。①LiBF4中阴离子的空间构型为
A.离子键 B.极性共价键 C.配位键 D.氢键
②碳酸亚乙酯分子中σ键与π键数目之比为
(2)碱金属在空气中燃烧时,只有锂生成普通氧化物
 。
。 是离子晶体,其晶格能可通过下图的
是离子晶体,其晶格能可通过下图的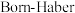 循环计算得到。
循环计算得到。
①由图中数据可知O=O键键能为
 ,
, 晶格能为
晶格能为 。
。②
 和
和 的熔点如下表所示:
的熔点如下表所示:| 氧化物 |  |  |
| 熔点/℃ | 1570 | 2800 |
熔点差异的原因是
您最近一年使用:0次
7 . 法匹拉韦是治疗新冠肺炎的一种药物,其结构简式如图所示。下列说法不正确的是
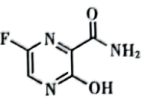

A.该分子的化学式为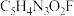 |
B.该分子中 键的键能小于 键的键能小于 键的键能 键的键能 |
C.该分子中σ键与π键数目之比为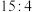 |
D.该分子中N、O、F的电负性的大小顺序为 |
您最近一年使用:0次
解题方法
8 . 卤族元素的单质和化合物在生产生活中有重要用途。
(1)某浓度的HF溶液中,氟化氢主要以(HF)2缔合形式存在。使氟化氢分子缔合的作用力是___________ ;气态氟化氢分子的热稳定性大于氯化氢的原因是___________ 。
(2)氯元素有多种含氧酸根离子。 中氯原子的杂化类型为
中氯原子的杂化类型为___________ , 的空间结构为
的空间结构为___________ 。
(3)几种卤化锌的熔点见表:
则x___________ (填“大于”或“小于”)283,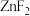 熔点远高于
熔点远高于 ,原因为
,原因为___________ 。
(4)2-碘酰基苯甲酸是典型的高价碘试剂,在有机合成中用作氧化剂,结构如图:

其分子中 键个数为
键个数为___________ ,基态碘原子的价电子轨道式为___________ 。
(1)某浓度的HF溶液中,氟化氢主要以(HF)2缔合形式存在。使氟化氢分子缔合的作用力是
(2)氯元素有多种含氧酸根离子。
 中氯原子的杂化类型为
中氯原子的杂化类型为 的空间结构为
的空间结构为(3)几种卤化锌的熔点见表:
| 物质 | 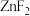 |  |  |
| 熔点/℃ | 872 | 283 | x |
则x
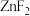 熔点远高于
熔点远高于 ,原因为
,原因为(4)2-碘酰基苯甲酸是典型的高价碘试剂,在有机合成中用作氧化剂,结构如图:

其分子中
 键个数为
键个数为
您最近一年使用:0次
名校
9 . 《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄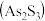 经常用来修改错字,其结构如图所示。下列说法不正确的是
经常用来修改错字,其结构如图所示。下列说法不正确的是
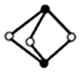
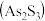 经常用来修改错字,其结构如图所示。下列说法不正确的是
经常用来修改错字,其结构如图所示。下列说法不正确的是
A.As、S原子的杂化方式均为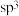 |
B.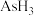 的沸点比 的沸点比 的低 的低 |
| C.与As同周期且基态原子核外未成对电子数目相同的元素只有V |
D.已知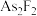 分子中各原子均满足8电子结构,分子中 分子中各原子均满足8电子结构,分子中 键和 键和 键的个数比为3:1 键的个数比为3:1 |
您最近一年使用:0次
2021-05-11更新
|
177次组卷
|
8卷引用:热点2 化学与传统文化-2021年高考化学【热点·重点·难点】专练(山东专用)
(已下线)热点2 化学与传统文化-2021年高考化学【热点·重点·难点】专练(山东专用)山东省济宁市2020届高三第三次模拟化学试题山东省邹城市第一中学2020届高三下学期第5次模拟考试化学试题(已下线)热点2 化学与传统文化-2021年高考化学专练【热点·重点·难点】(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练湖北省黄石市有色第一中学2020-2021学年高二下学期期中考试化学试题内蒙古自治区赤峰市赤峰二中2020-2021学年高二下学期第二次月考化学试题河北省唐山市开滦第二中学2019-2020学年高二下学期期末考试化学试题
名校
解题方法
10 . 国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、过氧乙酸(CH3COOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法错误的是
| A.CH3CH2OH能与水互溶主要原因是CH3CH2OH和水分子间能形成氢键 |
| B.NaClO通过氧化灭活病毒,乙醚与1—丁醇互为同分异构体 |
| C.1mol过氧乙酸分子中含有8NA个σ键 |
| D.氯仿(三氯甲烷)分子结构为正四面体,可由甲烷与氯气在光照的条件下发生取代反应制得 |
您最近一年使用:0次



