解题方法
1 . 《自然》报道了我国科学家利用催化剂通过化学链合成氨。回答下列问题:
(1)NH3可用于制备NaN3、NH₄NO₃,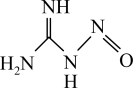 (亚硝基胍)等含氮化合物,基态N的核外电子排布为
(亚硝基胍)等含氮化合物,基态N的核外电子排布为___________ ; NH₄NO₃中 NH 中中心原子的杂化轨道类型为
中中心原子的杂化轨道类型为___________ NO 的空间结构为
的空间结构为___________ ; 亚硝基胍分子中σ键与π键的数目比为___________ 。
(2)N、P位于同一主族,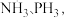 分子结构如图所示:
分子结构如图所示:___________ ,
②NH₃比PH₃的沸点高, 其主要原因是___________ 。
③磷化镓的晶胞结构如下图所示,A点坐标为(0,0,0),B点坐标为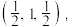 则C点坐标为
则C点坐标为___________ ;
(1)NH3可用于制备NaN3、NH₄NO₃,
 (亚硝基胍)等含氮化合物,基态N的核外电子排布为
(亚硝基胍)等含氮化合物,基态N的核外电子排布为 中中心原子的杂化轨道类型为
中中心原子的杂化轨道类型为 的空间结构为
的空间结构为(2)N、P位于同一主族,
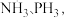 分子结构如图所示:
分子结构如图所示:
②NH₃比PH₃的沸点高, 其主要原因是
③磷化镓的晶胞结构如下图所示,A点坐标为(0,0,0),B点坐标为
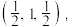 则C点坐标为
则C点坐标为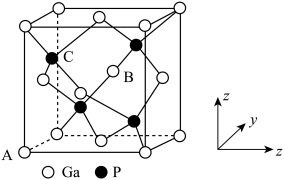
您最近一年使用:0次
解题方法
2 . 偶氨苯作为光开关,可对外部刺激作出响应。其结构简式如图所示。下列分析错误的是
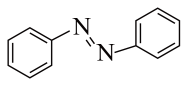
| A.根据“相似相溶”原理判断该物质可能与苯互溶 |
| B.分子中所有原子可能处于同一平面上 |
| C.1mol偶氮苯含2mol极性共价键 |
D.分子中C和N原子均采用 杂化方式 杂化方式 |
您最近一年使用:0次
解题方法
3 . 咪唑( )是生产抗真菌药物的主要原料之一,下列说法错误的是
)是生产抗真菌药物的主要原料之一,下列说法错误的是
| A.咪唑分子为极性分子 | B.分子中C-N键的极性小于N-H键的极性 |
C.分子中 键与 键与 键个数比为9∶2 键个数比为9∶2 | D.咪唑中两个N原子均为 杂化 杂化 |
您最近一年使用:0次
解题方法
4 . 我国自主研发的用氟硼铍酸钾(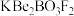 )晶体制造深紫外固体激光器技术领先世界。回答下列问题:
)晶体制造深紫外固体激光器技术领先世界。回答下列问题:
(1)基态K原子核外有_____ 种不同运动状态的电子,能量最低的空轨道的符号是_____ 。
(2)在1000℃时,氯化铍以 形式存在,该分子的空间构型为
形式存在,该分子的空间构型为_____ ;在500~600℃气相中,氯化铍则以二聚体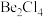 的形式存在,画出
的形式存在,画出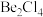 的结构:
的结构:_____ (标出配位键)。
(3)在第二周期中第一电离能介于B和O两种元素之间的元素有_____ (填元素符号)。
(4) 分子中的
分子中的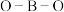 的键角大于
的键角大于 中的
中的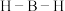 的键角,判断依据是
的键角,判断依据是_____ (从中心原子杂化方式的角度来解释)。
(5)一定条件下,实验测得的HF的相对分子质量总是大于理论值,原因是_____ 。
(6)六方氮化硼在高温高压下,可以转化为立方氮化硼,二者晶体结构如图所示: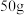 六方氮化硼晶体中含有六元环的数目为
六方氮化硼晶体中含有六元环的数目为_____  (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
②立方氮化硼晶体中,设晶胞中最近的B、N原子之间的距离为apm,晶体的密度为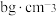 。则阿伏加德罗常数为
。则阿伏加德罗常数为_____  。(列式即可,用含a、b的代数式表示)
。(列式即可,用含a、b的代数式表示)
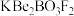 )晶体制造深紫外固体激光器技术领先世界。回答下列问题:
)晶体制造深紫外固体激光器技术领先世界。回答下列问题:(1)基态K原子核外有
(2)在1000℃时,氯化铍以
 形式存在,该分子的空间构型为
形式存在,该分子的空间构型为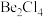 的形式存在,画出
的形式存在,画出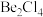 的结构:
的结构:(3)在第二周期中第一电离能介于B和O两种元素之间的元素有
(4)
 分子中的
分子中的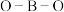 的键角大于
的键角大于 中的
中的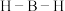 的键角,判断依据是
的键角,判断依据是(5)一定条件下,实验测得的HF的相对分子质量总是大于理论值,原因是
(6)六方氮化硼在高温高压下,可以转化为立方氮化硼,二者晶体结构如图所示:

 六方氮化硼晶体中含有六元环的数目为
六方氮化硼晶体中含有六元环的数目为 (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。②立方氮化硼晶体中,设晶胞中最近的B、N原子之间的距离为apm,晶体的密度为
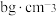 。则阿伏加德罗常数为
。则阿伏加德罗常数为 。(列式即可,用含a、b的代数式表示)
。(列式即可,用含a、b的代数式表示)
您最近一年使用:0次
5 . 化合物M·6H₂O 可用作洗涤粉, M的结构如下, 其中X、Y、Z、W 是原子序数依次增大的短周期主族元素,下列说法不正确的是
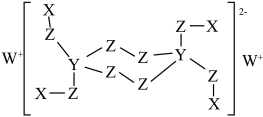

| A.Y的基态原子核外电子排布中有1个未成对电子 |
| B.X、Y、Z、W元素中电负性最大的是Z |
| C.Z、W形成的化合物中不可能含有共价键 |
| D.X、Z形成的X₂Z 分子的空间构型是 V 形 |
您最近一年使用:0次
6 . 氮和硒(Se)都是重要元素,在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉是一种抗癌新药,其结构式如图:___________ ,价层有___________ 种不同能量的电子
②比较 、
、 、
、 三种氢化物:沸点由高到低依次为
三种氢化物:沸点由高到低依次为___________ ,稳定性由强到弱依次为___________ 。
③比较键角大小:气态 分子
分子___________ 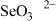 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是
___________ 。
(2)① 是有机合成中常用的还原剂,其阴离子
是有机合成中常用的还原剂,其阴离子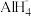 空间结构为
空间结构为___________ , 中存在的化学键
中存在的化学键___________ (填标号)。
A.离子键 B. 键 C.极性键 D.氢键
键 C.极性键 D.氢键
② 中阴离子的空间结构为
中阴离子的空间结构为___________ ;
(1)乙烷硒啉是一种抗癌新药,其结构式如图:
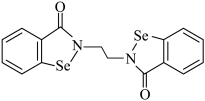
②比较
 、
、 、
、 三种氢化物:沸点由高到低依次为
三种氢化物:沸点由高到低依次为③比较键角大小:气态
 分子
分子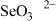 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是(2)①
 是有机合成中常用的还原剂,其阴离子
是有机合成中常用的还原剂,其阴离子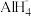 空间结构为
空间结构为 中存在的化学键
中存在的化学键A.离子键 B.
 键 C.极性键 D.氢键
键 C.极性键 D.氢键②
 中阴离子的空间结构为
中阴离子的空间结构为③1mol 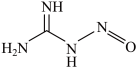 中含
中含 键
键
您最近一年使用:0次
解题方法
7 . 下列关于 、
、 、
、 三种微粒的说法不正确
三种微粒的说法不正确
 、
、 、
、 三种微粒的说法不正确
三种微粒的说法不正确| A.三种微粒所含有的电子数相等 | B.三种微粒中氮原子的杂化方式相同 |
| C.三种微粒的VSEPR模型相同 | D.键角大小关系: |
您最近一年使用:0次
8 . 碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构为 。下列有关该分子的说法错误的是
。下列有关该分子的说法错误的是
A.分子式为 | B.分子中碳原子的杂化方式为 、 、 |
| C.分子中既有极性键也有非极性键 | D.该分子为手性分子 |
您最近一年使用:0次
解题方法
9 . 下列说法正确的是
| A.水很稳定是因为水中含有大量的氢键 |
| B.邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点高 |
C. 和 和 空间结构不同,价层电子对数也不同 空间结构不同,价层电子对数也不同 |
| D.氨气极易溶于水,原因之一是氨分子与水分子之间形成了氢键。 |
您最近一年使用:0次
解题方法
10 . 下列判断正确的是
A. 为平面三角形 为平面三角形 | B. 为平面三角形 为平面三角形 | C. 为直线形 为直线形 | D. 为三角锥形 为三角锥形 |
您最近一年使用:0次



