解题方法
1 . 下列符号表征或说法正确的是
A. 电离: 电离: | B. 位于元素周期表p区 位于元素周期表p区 |
C. 空间结构:平面三角形 空间结构:平面三角形 | D. 电子式: 电子式: |
您最近一年使用:0次
名校
解题方法
2 . 我国力争在2030年前实现“碳达峰”。2060年前实现“碳中和”的目标,因此二氧化碳的固定及转化成了重要的研究课题。
Ⅰ.在 催化作用下
催化作用下 和
和 反应生成甲醇:
反应生成甲醇: ;
;
Ⅱ.新型 水介质电池放电时,温室气体
水介质电池放电时,温室气体 被转化为储能物质
被转化为储能物质 。
。
请回答下列问题:
(1)基态Cu原子的外围电子排布式为___________ ,基态O原子核外有___________ 种不同运动状态的电子。
(2)Ⅰ中涉及的 、
、 、
、 、
、 ,属于非极性分子的是
,属于非极性分子的是___________ (填化学式)。
(3) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为___________ ,分子中含有的 键和
键和 键数目之比为
键数目之比为___________ 。
(4) 反应中,
反应中, 的立体构型为
的立体构型为___________ , 的沸点高于
的沸点高于 的原因是
的原因是___________ 。
(5)氧化锌(ZnO),俗称锌白,是一种常用的化学添加剂,广泛地应用于塑料、硅酸盐制品、合成橡胶等产品的制作中。一种ZnO的立方晶胞如图所示。
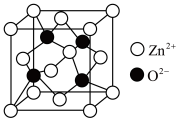
① 周围距离最近且等距的
周围距离最近且等距的 数目为
数目为___________ 。
②设晶胞边长为anm, 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为___________  。
。
Ⅰ.在
 催化作用下
催化作用下 和
和 反应生成甲醇:
反应生成甲醇: ;
;Ⅱ.新型
 水介质电池放电时,温室气体
水介质电池放电时,温室气体 被转化为储能物质
被转化为储能物质 。
。请回答下列问题:
(1)基态Cu原子的外围电子排布式为
(2)Ⅰ中涉及的
 、
、 、
、 、
、 ,属于非极性分子的是
,属于非极性分子的是(3)
 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为 键和
键和 键数目之比为
键数目之比为(4)
 反应中,
反应中, 的立体构型为
的立体构型为 的沸点高于
的沸点高于 的原因是
的原因是(5)氧化锌(ZnO),俗称锌白,是一种常用的化学添加剂,广泛地应用于塑料、硅酸盐制品、合成橡胶等产品的制作中。一种ZnO的立方晶胞如图所示。

①
 周围距离最近且等距的
周围距离最近且等距的 数目为
数目为②设晶胞边长为anm,
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 。
。
您最近一年使用:0次
2023-07-30更新
|
899次组卷
|
4卷引用:内蒙古名校联盟2022-2023学年高二下学期期末考试化学试题
解题方法
3 . 铜及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)在元素周期表的分区中,铜属于_______ 区,与铜处于同一周期且最外层电子数相同的元素的基态原子共有_______ 种。
(2)过渡金属与O形成羰基配合物时,每个CO分子向中心原子提供2个电子,最终使中心原子的电子总数与同周期的稀有气体原子相同,称为有效原子序数规则。根据此规则推断,镍与CO形成的羰基配合物Ni(CO)x中,x=_______ 。
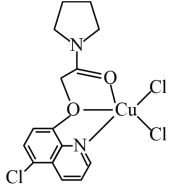
(3)CuCl2可与某有机多齿配体形成具有较强荧光性能的配合物,其结构简式如图所示。该配合物分子中N原子的杂化类型为_______ ,1mol 该有机配体与Cu( II )形成的配位键为_______ mol。
(4)铜催化烯烃硝化反应时会产生 。键角:
。键角:
_______  (填“<” 或“=”或“>”),其原因是
(填“<” 或“=”或“>”),其原因是_______ 。
(5)近期我国科学家合成了一种电化学性能优异的铜硒化合物,其晶胞结构如图所示。该铜硒化合物的化学式为_______ ,其中Cu 元素以Cu+和Cu2+存在,则_______ (填“①”或“②”)为Cu2+,该晶体的密度_______ g/cm3 (用含a和c的式子表示,设阿伏伽德罗常数为NA)。

(1)在元素周期表的分区中,铜属于
(2)过渡金属与O形成羰基配合物时,每个CO分子向中心原子提供2个电子,最终使中心原子的电子总数与同周期的稀有气体原子相同,称为有效原子序数规则。根据此规则推断,镍与CO形成的羰基配合物Ni(CO)x中,x=
(3)CuCl2可与某有机多齿配体形成具有较强荧光性能的配合物,其结构简式如图所示。该配合物分子中N原子的杂化类型为

(4)铜催化烯烃硝化反应时会产生
 。键角:
。键角:
 (填“<” 或“=”或“>”),其原因是
(填“<” 或“=”或“>”),其原因是(5)近期我国科学家合成了一种电化学性能优异的铜硒化合物,其晶胞结构如图所示。该铜硒化合物的化学式为

您最近一年使用:0次
4 . 铜及其化合物在生产生活中有着广泛的应用。请回答:
(1)已知Cu第一电离能I1(Cu)=746 kJ·mol-1,Zn第一电离能I1(Zn)=906 kJ·mol-1;则第二电离能大小关系为I2(Cu)___________ I2(Zn)(填“>”、“=”或“<”)。。
(2)在碱性条件下CuSO4与双缩脲[HN(CONH2)2]生成紫色的配位化合物,该原理可用于检验蛋白质。该配位化合物的阴离子结构如图所示:
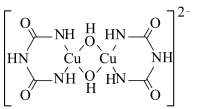
①该阴离子中所有元素的电负性从大到小的顺序为___________ 。
②该阴离子中氧原子的杂化方式为___________ ;
③lmol该阴离子含有σ键的数目为___________ ;
④该配合物中心铜离子的外围电子排布图为___________ ;
(3)磁性形状记忆材料Cu-Mn-Al合金的晶胞如图a所示(Mn、Al位于Cu形成的立方体体心位置),图b是沿立方格子对角面取得的截图,Cu在沿立方格子对角面取得截图中的相对位置如图c所示。

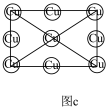
①该合金随温度升高,电导率_______ (填“升高”或“降低”或“不变”) ,原因为________ ;
②在图c中画出上图b切面上的Al和Mn的相对位置___________ (不考虑各原子的大小)。
(1)已知Cu第一电离能I1(Cu)=746 kJ·mol-1,Zn第一电离能I1(Zn)=906 kJ·mol-1;则第二电离能大小关系为I2(Cu)
(2)在碱性条件下CuSO4与双缩脲[HN(CONH2)2]生成紫色的配位化合物,该原理可用于检验蛋白质。该配位化合物的阴离子结构如图所示:

①该阴离子中所有元素的电负性从大到小的顺序为
②该阴离子中氧原子的杂化方式为
③lmol该阴离子含有σ键的数目为
④该配合物中心铜离子的外围电子排布图为
(3)磁性形状记忆材料Cu-Mn-Al合金的晶胞如图a所示(Mn、Al位于Cu形成的立方体体心位置),图b是沿立方格子对角面取得的截图,Cu在沿立方格子对角面取得截图中的相对位置如图c所示。


①该合金随温度升高,电导率
②在图c中画出上图b切面上的Al和Mn的相对位置
您最近一年使用:0次
名校
解题方法
5 . 现有前四周期的6种元素的部分信息如下表所示:
根据上述元素信息,回答下列问题。
(1)基态F原子的简化电子排布式为___________ ,该元素在元素周期表中的位置是___________ ,属于___________ 区,此区元素的价电子层结构特点是___________ ;
(2)E原子的价电子轨道表示式为___________ ;请画出BD2物质的电子式___________
(3)比较下列物质的键角大小(填“>”或“<”、“=”)并说明原因:CA3___________ EA3;原因___________ ;
(4)1mol [F(CA3)4]2+ 中含有___________ 个 键,若该离子中两个CA3被
键,若该离子中两个CA3被 取代能得到两种不同结构的离子,则[F(CA3)4]2+的立体构型为
取代能得到两种不同结构的离子,则[F(CA3)4]2+的立体构型为___________ ,所含化学键类型为___________
a.共价键 b.离子键 c.配位键 d. 键 e.
键 e. 键
键
| 元素 | 元素部分信息 |
| A | A的阴离子核外电子云呈球形 |
| B | 元素原子最外层电子数是次外层的2倍 |
| C | 原子的最高能级上有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的气态氢化物中最大 |
| D | 基态原子核外有3个能级填充了电子,能量最高能级的电子数等于前两个能级的电子数之和 |
| E | 与C同族,次外层有8个电子 |
| F | 一种核素的质量数为65,中子数为36 |
(1)基态F原子的简化电子排布式为
(2)E原子的价电子轨道表示式为
(3)比较下列物质的键角大小(填“>”或“<”、“=”)并说明原因:CA3
(4)1mol [F(CA3)4]2+ 中含有
 键,若该离子中两个CA3被
键,若该离子中两个CA3被 取代能得到两种不同结构的离子,则[F(CA3)4]2+的立体构型为
取代能得到两种不同结构的离子,则[F(CA3)4]2+的立体构型为a.共价键 b.离子键 c.配位键 d.
 键 e.
键 e. 键
键
您最近一年使用:0次
名校
6 . 下列说法正确的有个
①价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
②所有σ键强度都大于π键
③杂化轨道只用于形成共价键
④只要分子的空间结构为平面三角形,中心原子均为sp2杂化
⑤NH3与H3O+的VSEPR构型均为四面体形,二者空间结构一致
⑥p能级能量一定比s能级的能量高
①价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
②所有σ键强度都大于π键
③杂化轨道只用于形成共价键
④只要分子的空间结构为平面三角形,中心原子均为sp2杂化
⑤NH3与H3O+的VSEPR构型均为四面体形,二者空间结构一致
⑥p能级能量一定比s能级的能量高
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
名校
7 . NA为阿伏加德罗常数的值。下列说法错误的是
| A.23g CH3CH2OH中sp3杂化的原子数为NA |
| B.0.5molXeF4中氙的价层电子对数为3NA |
| C.62 g白磷中含有P-P键的数目为3NA |
| D.12g石墨烯(单层石墨)中含有六元环的个数为0.5NA |
您最近一年使用:0次
2023-05-09更新
|
165次组卷
|
2卷引用:内蒙古呼和浩特市剑桥中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
8 . 2022年春晚中舞蹈诗剧《只此青绿》生动还原了北宋名画《千里江山图》,画之所以色彩艳丽,璀璨夺目,与所使用矿物颜料有关。回答下列问题:
(1)石青,又名蓝矿石,化学式为Cu3(CO3)2(OH)2,基态Cu2+核外电子的空间运动状态有_____ 种,CO 的空间构型为
的空间构型为_____ 。原子中电子有两种相反的自旋状态,分别用+ 和-
和- 表示,称为电子的自旋磁量子数,则Cu2+中电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则Cu2+中电子自旋磁量子数的代数和为_____ 。
(2)亚铁氰化钾,化学式为K4[Fe(CN)6],呈黄色结晶性粉末。[Fe(CN)6]4-中配体CN-的配位原子是_____ (填元素符号),与CN-互为等电子体的分子______ ,[Fe(CN)6]4-中σ键和π键的数目之比为_____ 。
(3)Cu2S呈黑色或灰黑色,已知:晶胞中S2-的位置如图1所示,Cu+位于S2-所构成的四面体中心,晶胞的侧视图如图2所示。
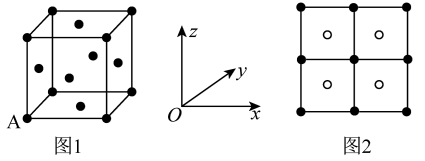
Cu+填充了晶胞中四面体空隙的百分率是_____ ,S2-配位数为______ 。已知图1中A原子的原子分数坐标为(0,0,0),则与A原子距离最近的Cu+的原子分数坐标为______ 。若晶胞参数为anm,晶体的密度为dg/cm3,则阿伏加德罗常数的值为______ (用含a和d的代数式表示)。
(1)石青,又名蓝矿石,化学式为Cu3(CO3)2(OH)2,基态Cu2+核外电子的空间运动状态有
 的空间构型为
的空间构型为 和-
和- 表示,称为电子的自旋磁量子数,则Cu2+中电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则Cu2+中电子自旋磁量子数的代数和为(2)亚铁氰化钾,化学式为K4[Fe(CN)6],呈黄色结晶性粉末。[Fe(CN)6]4-中配体CN-的配位原子是
(3)Cu2S呈黑色或灰黑色,已知:晶胞中S2-的位置如图1所示,Cu+位于S2-所构成的四面体中心,晶胞的侧视图如图2所示。

Cu+填充了晶胞中四面体空隙的百分率是
您最近一年使用:0次
2023-05-03更新
|
162次组卷
|
2卷引用:内蒙古赤峰市2022-2023学年高三上学期期末模拟考试化学试题
名校
9 . X、Y、Z、V、W五种短周期元素,原子序数依次增大,其中Z的原子半径最大,Z的单质在W的单质中燃烧产生黄色火焰,生成ZW型化合物;五种元素可以组成一种有机盐(如图所示)。下列说法正确的是
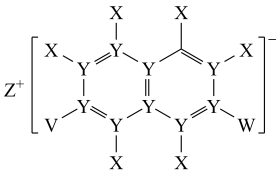

| A.Y与W形成的分子空间结构为三角锥 |
| B.V单质微溶于Y与V组成的二元化合物 |
| C.原子半径的大小关系为:Z>V>W |
| D.热稳定性:X与V组成的二元化合物>X与W组成的二元化合物 |
您最近一年使用:0次
2023-03-22更新
|
417次组卷
|
4卷引用:内蒙古阿拉善盟2023届高三第一次模拟考试理科综合化学试题
内蒙古阿拉善盟2023届高三第一次模拟考试理科综合化学试题宁夏中卫市2022届高三下学期二模理综化学试题(已下线)专题07 突破原子结构和元素周期表(律)(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)河北省张家口市宣化第一中学2022-2023学年高二下学期5月期中化学试题
解题方法
10 . 某些过渡金属(如钛、铜)及其化合物,以其高导电性和丰富的物理化学性质在材料领域大放异彩。
(1)钛比钢轻、比铝硬。基态钛原子的价层电子排布式为_______ :钛原子核外电子占据的轨道数_______ 。
(2)铜的下列状态中,失去最外层一个电子所需能量最小的是_______。
(3)二氧化钛是良好的光催化剂,可催化转化多种有毒物质,如:可将水中的 转化为
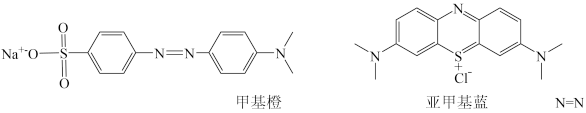
转化为 ,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
① 的空间构型是
的空间构型是_______ 。
②甲基橙、亚甲基蓝中C原子的杂化类型有_______ ,
③常温下,CO2、HCHO在水中溶解度之比大约是1:500,其主要原因是_______ 。
(4)黄铜矿炼铜过程中会产生SO2,与SO2互为等电子体的分子和阴离子分别为_______ (各写一种即可)。
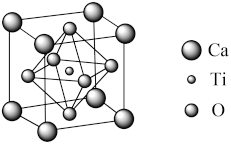
(5)钙钛矿型太阳能电池近年越来越受到科学界的关注,其效率提升速度超越过去任何一类电池。某种钙钛矿晶胞如图所示,则钙原子的配位数是_______ ,若阿伏加德罗常数的值为NA,晶胞中钙原子与氧原子的最近距离为a pm。则该晶胞的密度为_______ g/cm3.(列出计算式)
(1)钛比钢轻、比铝硬。基态钛原子的价层电子排布式为
(2)铜的下列状态中,失去最外层一个电子所需能量最小的是_______。
| A.[Ar]3dl04pl | B.[Ar]3d10 | C.[Ar]3d94s1 | D.[Ar]3d104s1 |
 转化为
转化为 ,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
①
 的空间构型是
的空间构型是②甲基橙、亚甲基蓝中C原子的杂化类型有
③常温下,CO2、HCHO在水中溶解度之比大约是1:500,其主要原因是
(4)黄铜矿炼铜过程中会产生SO2,与SO2互为等电子体的分子和阴离子分别为
(5)钙钛矿型太阳能电池近年越来越受到科学界的关注,其效率提升速度超越过去任何一类电池。某种钙钛矿晶胞如图所示,则钙原子的配位数是

您最近一年使用:0次
2023-03-16更新
|
778次组卷
|
4卷引用:内蒙古自治区包头市2024届高三二模理科综合-化学试题
内蒙古自治区包头市2024届高三二模理科综合-化学试题河南省平许济洛四市2023届高三下学期第二次质量检测理科综合化学试题(已下线)狂飙卷 04-【热题狂飙】2023年高考化学样卷(全国卷专用)陕西省铜川市2023届高三下学期第二次模拟考试理综化学试题



