解题方法
1 . 黄铁矿是制取硫酸的主要原料,其主要成分为FeS2,其中铁元素显+2价,FeS2晶体的晶胞形状为立方体,晶胞结构如图所示。

(1)基态Fe2+的价电子排布式是___________ 。
(2)制取硫酸过程中会产生SO3,SO3分子的空间构型为___________ 。
(3)晶胞中与每个S 距离最近且相等的Fe2+有
距离最近且相等的Fe2+有___________ 个。
(4)FeS2晶体的晶胞边长为anm,FeS2的摩尔质量为120g·mol-1,阿伏加德罗常数的值为NA,该FeS2晶体的密度ρ=___________ g·cm-3(1nm=10-7cm,用含a、NA的代数式表示)

(1)基态Fe2+的价电子排布式是
(2)制取硫酸过程中会产生SO3,SO3分子的空间构型为
(3)晶胞中与每个S
 距离最近且相等的Fe2+有
距离最近且相等的Fe2+有(4)FeS2晶体的晶胞边长为anm,FeS2的摩尔质量为120g·mol-1,阿伏加德罗常数的值为NA,该FeS2晶体的密度ρ=
您最近一年使用:0次
2 . 离子液体具有较好的化学稳定性、较低的熔点及对无机物、有机化合物等不同物质良好溶解性等优点,在有机合成领域用途广泛。一种离子液体的结构简式如下图。
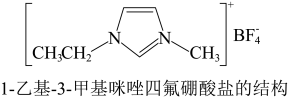
下列说法错误 的是

下列说法
| A.阳离子中C原子有sp2、sp3两种杂化方式 |
| B.阴离子呈平面正方形,存在共价键和配位键 |
| C.该离子液体能与H2O形成氢键 |
| D.熔点低的可能原因是离子体积增大、距离增大、作用力减弱 |
您最近一年使用:0次



