解题方法
1 . 废水中 会带来环境污染问题,用微生物法和铁炭法均可将
会带来环境污染问题,用微生物法和铁炭法均可将 还原脱除。
还原脱除。
(1)微生物法脱硫
富含有机物的弱酸性废水在微生物作用下产生CH3COOH、H2等物质,可将废水中 还原为H2S,同时用N2或CO2将H2S从水中吹出,再用碱液吸收。
还原为H2S,同时用N2或CO2将H2S从水中吹出,再用碱液吸收。
① 的空间构型为
的空间构型为_______ 。
②CH3COOH与 在SBR细菌作用下生成CO2和H2S的离子方程式为
在SBR细菌作用下生成CO2和H2S的离子方程式为_______ 。
③将H2S从水中吹出时,用CO2比N2效果更好,其原因是_______ 。
(2)铁炭法脱硫
铁炭混合物(铁屑与活性炭的混合物)在酸性废水中产生原子态H,可将废水中的 转化为硫化物沉淀除去。
转化为硫化物沉淀除去。
①废水中 转化为硫化物而除去,该硫化物的化学式为
转化为硫化物而除去,该硫化物的化学式为_______ 。
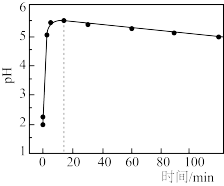
②为提高铁炭混合物处理效果常通入少量空气,反应过程中废水pH随时间变化如图所示。反应进行15 min后溶液pH缓慢下降的原因可能是_______ 。
(3)处理后废水中 含量测定
含量测定
准确量取50.00 mL水样于锥形瓶中,加入10.00 mL 0.0500 mol·L-1BaCl2溶液,充分反应后,滴加氨水调节溶液pH= 10,用0.0100 mol·L-1 EDTA (Na2H2Y) 溶液滴定至终点,滴定反应为:Ba2++H2Y2- =BaY2-+2H+,平行滴定3次,平均消耗EDTA溶液27.50 mL。计算处理后水样中 含量
含量_______ 。(用mg·L-1表示,写出计算过程)。
 会带来环境污染问题,用微生物法和铁炭法均可将
会带来环境污染问题,用微生物法和铁炭法均可将 还原脱除。
还原脱除。(1)微生物法脱硫
富含有机物的弱酸性废水在微生物作用下产生CH3COOH、H2等物质,可将废水中
 还原为H2S,同时用N2或CO2将H2S从水中吹出,再用碱液吸收。
还原为H2S,同时用N2或CO2将H2S从水中吹出,再用碱液吸收。①
 的空间构型为
的空间构型为②CH3COOH与
 在SBR细菌作用下生成CO2和H2S的离子方程式为
在SBR细菌作用下生成CO2和H2S的离子方程式为③将H2S从水中吹出时,用CO2比N2效果更好,其原因是
(2)铁炭法脱硫
铁炭混合物(铁屑与活性炭的混合物)在酸性废水中产生原子态H,可将废水中的
 转化为硫化物沉淀除去。
转化为硫化物沉淀除去。①废水中
 转化为硫化物而除去,该硫化物的化学式为
转化为硫化物而除去,该硫化物的化学式为②为提高铁炭混合物处理效果常通入少量空气,反应过程中废水pH随时间变化如图所示。反应进行15 min后溶液pH缓慢下降的原因可能是

(3)处理后废水中
 含量测定
含量测定准确量取50.00 mL水样于锥形瓶中,加入10.00 mL 0.0500 mol·L-1BaCl2溶液,充分反应后,滴加氨水调节溶液pH= 10,用0.0100 mol·L-1 EDTA (Na2H2Y) 溶液滴定至终点,滴定反应为:Ba2++H2Y2- =BaY2-+2H+,平行滴定3次,平均消耗EDTA溶液27.50 mL。计算处理后水样中
 含量
含量
您最近一年使用:0次
2022-05-07更新
|
951次组卷
|
6卷引用:江苏省苏锡常镇四市2022届高三下学期教学情况调研(二)化学试题
江苏省苏锡常镇四市2022届高三下学期教学情况调研(二)化学试题江苏省苏锡常镇四市2021-2022学年高三下学期5月教学情况调研(二)化学试题 (已下线)2022年江苏卷高考真题变式题14-17(已下线)2022年北京高考真题变式题1-14(已下线)江苏省2022年普通高中学业水平选择性考试变式题(结构与性质)(已下线)2022年北京高考真题化学试题变式题(结构与性质)
名校
解题方法
2 . 2022年春晚节目《只此青绿》取材于宋代名画《千里江山图》,该画描绘了山清水秀的美丽景色,历经千年色彩依然,其中青色来自蓝铜矿颜料[主要成分为Cu3(CO3)2(OH)2]。请回答下列问题:
(1)基态铜原子价电子排布式为_______ 。从原子结构角度分析,第二电离能I2(Fe)与I2(Cu)的关系是I2(Fe)_______ I2(Cu) (填“>”“<”或“=”),并解释有关原因_______ 。
(2) 的空间构型为
的空间构型为_______ 。
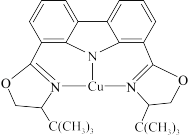
(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素电负性由大到小的顺序是_______ (填元素符号),该配合物中采用sp2杂化的碳原子与sp3杂化的碳原子个数比为_______ 。
(4)黄铜矿是主要的炼铜原料,晶胞结构如下图1所示,晶胞中S原子的投影位置如图2所示。
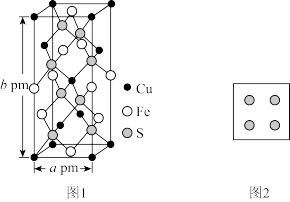
①Fe3+周围距离最近的S2-的个数为_______ 。
②该晶胞上下底面均为正方形,侧面与底面垂直,晶胞参数如图所示,晶胞的密度为ρ g/cm3,则阿伏加德罗常数(NA)为_______ mol-1(用a、b、ρ表示,并化成最简)。
(1)基态铜原子价电子排布式为
(2)
 的空间构型为
的空间构型为(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素电负性由大到小的顺序是

(4)黄铜矿是主要的炼铜原料,晶胞结构如下图1所示,晶胞中S原子的投影位置如图2所示。

①Fe3+周围距离最近的S2-的个数为
②该晶胞上下底面均为正方形,侧面与底面垂直,晶胞参数如图所示,晶胞的密度为ρ g/cm3,则阿伏加德罗常数(NA)为
您最近一年使用:0次
2022-05-04更新
|
733次组卷
|
4卷引用:安徽省淮北市2022届高三第二次模拟考试理科综合化学试题
安徽省淮北市2022届高三第二次模拟考试理科综合化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)山东省菏泽市单县第二中学2021-2022学年高二下学期慧光班段考化学试题四川省南充高级中学2021-2022学年高二下学期期中考试化学试题
解题方法
3 . 砷化镓(GaAs)、碲化镉(CdTe)等太阳能电池适合光电转换,可以直接把光能转化成电能。回答下列问题:
(1)元素As与N同族,预测As的氢化物分子的立体结构为____ ,其基态原子最外层p轨道电子的自旋状态____ (填“相同”或“相反”)。
(2)元素Cd与Zn是同一副族的相邻元素,Cd的价层电子排布为4d105s2,Cd2+的价层电子排布为___ 。
(3)经X射线衍射实验证明在碲酸(H6TeO6)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为____ 。
(4)Te、Se都是第ⅥA族的元素,SeF6与SF6具有相似的结构,则熔沸点SeF6___ SF6(填“>”或“<”或“=");二硒键和二硫键是重要的光响应动态共价键,其光响应原理可用如图表示,已知光的波长与其能量成反比,则图中实现光响应的波长:λ1____ λ2(填“>”或“<”或“="),其原因是____ 。

(5)CdTe的晶胞属立方晶系,晶胞参数如图1所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。如原子M的坐标为(0,0,0),则原子N的坐标为____ 。

该晶胞沿其面对角线方向上的投影如图2所示,则代表Te原子的位置是____ (填序号),晶胞中原子6和11之间的距离为____ pm(用含a的代数式表示)。
(1)元素As与N同族,预测As的氢化物分子的立体结构为
(2)元素Cd与Zn是同一副族的相邻元素,Cd的价层电子排布为4d105s2,Cd2+的价层电子排布为
(3)经X射线衍射实验证明在碲酸(H6TeO6)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为
(4)Te、Se都是第ⅥA族的元素,SeF6与SF6具有相似的结构,则熔沸点SeF6

(5)CdTe的晶胞属立方晶系,晶胞参数如图1所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。如原子M的坐标为(0,0,0),则原子N的坐标为

该晶胞沿其面对角线方向上的投影如图2所示,则代表Te原子的位置是
您最近一年使用:0次
解题方法
4 . M、P、Q三种元素的相关信息如表:
(1)MO3是常见的M的氧化物,液态MO3有单分子MO3和三聚体(MO3)3两种形式;固态MO3主要以三聚体(MO3)3和无限长链(MO3)n两种形式存在。单分子MO3的空间构型为____ 。
②环状(MO3)3和链状(MO3)n的结构如图所示,环状(MO3)3中M原子的杂化轨道类型为____ ,链状(MO3)n中发生杂化的氧原子有____ 个(用含“n”的式于表示)。常温下,单分子MO3是液体,而链状(MO3)n是固体的原因是____ 。

(2)RH3BH3是目前最具潜力的储氢材料之一。
①RH3BH3能溶于水,其主要原因是____ 。
②RH3BH3分子中与R相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键,用“R—H…H—B”表示.以下物质之间可能形成双氢键的是____ (填序号)。
A.LiH和HCN B.C6H6和CHCl3 C.C2H4和C2H2 D.B2H6和NH3
(3)含元素Q、钇(Y)、氧(O)的某正交相晶胞[YaQbOc]结构如图所示。

a:b:c=____ ,已知1号O原子空间坐标为(0,0, ),2号O原子空间坐标为(
),2号O原子空间坐标为( ,
, +m,
+m, +n),则3号Fe原子的空间坐标为
+n),则3号Fe原子的空间坐标为____ 。若晶胞参数分别为apm、bpm和cpm,阿伏加德罗常数的值用NA表示,则该晶体的密度为____ g•cm-3(列表达式)。
| 元素 | 相关信息 |
| M | 基态原子的价电子排布式为3s23p4 |
| R | 空气中含量最多的元素 |
| Q | 常见金属元素,基态原子的M层有4个未成对的电子 |
②环状(MO3)3和链状(MO3)n的结构如图所示,环状(MO3)3中M原子的杂化轨道类型为

(2)RH3BH3是目前最具潜力的储氢材料之一。
①RH3BH3能溶于水,其主要原因是
②RH3BH3分子中与R相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键,用“R—H…H—B”表示.以下物质之间可能形成双氢键的是
A.LiH和HCN B.C6H6和CHCl3 C.C2H4和C2H2 D.B2H6和NH3
(3)含元素Q、钇(Y)、氧(O)的某正交相晶胞[YaQbOc]结构如图所示。

a:b:c=
 ),2号O原子空间坐标为(
),2号O原子空间坐标为( ,
, +m,
+m, +n),则3号Fe原子的空间坐标为
+n),则3号Fe原子的空间坐标为
您最近一年使用:0次
名校
解题方法
5 . Ⅰ.用硼镁矿(主要成分为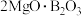 ,含
,含 、
、 、铁的氧化物等杂质)生产硼酸(H3BO3)并回收硫酸镁的工艺流程如图:
、铁的氧化物等杂质)生产硼酸(H3BO3)并回收硫酸镁的工艺流程如图:
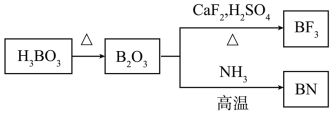
(1)“酸浸”过程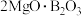 发生的主要化学反应方程式为
发生的主要化学反应方程式为_______ 。为避免“酸浸”产生大量气泡使物料溢出,应采取的措施为_______ 。
(2)“除杂”时向滤液中加入 和试剂a,
和试剂a, 的作用为
的作用为_______ (用离子方程式表示)。试剂a为_______ 。
(3)硫酸镁的溶解度随温度变化曲线如图所示。为从“母液”中充分回收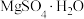 ,应保持“母液”在
,应保持“母液”在_______ ℃以上蒸发浓缩结晶、_______ ,再用乙醇洗涤后干燥。_______ 。
(5)在 中,F-B-F的键角是
中,F-B-F的键角是_______ , 和过NaF作用可生成
和过NaF作用可生成 ,
, 的空间结构为
的空间结构为_______ 。 的电子式为
的电子式为_______ 。
 ,含
,含 、
、 、铁的氧化物等杂质)生产硼酸(H3BO3)并回收硫酸镁的工艺流程如图:
、铁的氧化物等杂质)生产硼酸(H3BO3)并回收硫酸镁的工艺流程如图: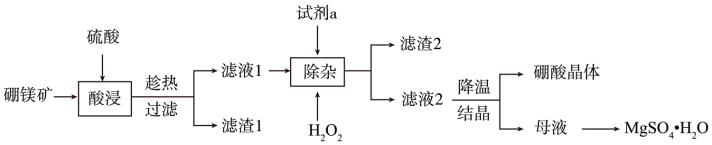
(1)“酸浸”过程
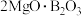 发生的主要化学反应方程式为
发生的主要化学反应方程式为(2)“除杂”时向滤液中加入
 和试剂a,
和试剂a, 的作用为
的作用为(3)硫酸镁的溶解度随温度变化曲线如图所示。为从“母液”中充分回收
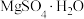 ,应保持“母液”在
,应保持“母液”在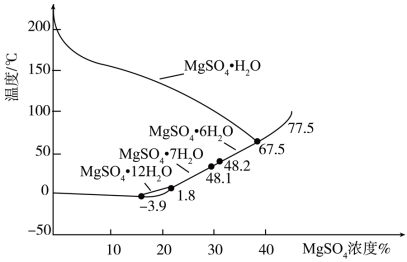
(5)在
 中,F-B-F的键角是
中,F-B-F的键角是 和过NaF作用可生成
和过NaF作用可生成 ,
, 的空间结构为
的空间结构为 的电子式为
的电子式为
您最近一年使用:0次
2022-05-03更新
|
286次组卷
|
2卷引用:广东省广州市第六中学2021-2022学年高二下学期期中测试化学试题
解题方法
6 . 我国科学家研究了具有高稳定性的二维硼烯氧化物(BmOn)的超导电性。回答下列问题:
(1)第一电离能介于B、N之间的第二周期元素为_______ (填元素符号)。
(2)①已知二维硼烯氧化物的部分结构如图所示,则该氧化物的化学式为_____ ,其中硼原子的杂化轨道类型为_____ 。

②键长和键角的数值可通过晶体的X射线衍射实验获得。经过该实验测定,二维硼烯氧化物中B-B键的键长大于B-O键的键长,其原因是_______ 。
(3)硼烷又称硼氢化合物,随着硼原子数的增加,硼烷由气态经液态至固态,其原因_______ 。
(4)LiBH4 -LiI复合材料在低温下表现出较高的离子电导率。BH 离子中H的化合价为-1,其原因可能是
离子中H的化合价为-1,其原因可能是 _______ ,BH 可以被PS
可以被PS 离子部分取代,PS
离子部分取代,PS 离子的空间结构为
离子的空间结构为_______ 。
(5)Fe3O4是电子导体,其导电率显著高于Fe2O3,这归因于Fe2+和Fe3+中心之间的电子交换。如图甲所示, Fe3O4晶体中,O2-围成正四面体空隙(如:1、3、6、7围成)和正八面体空隙(如:3、6、7、8、9、12围成),Fe3O4中有一半的Fe3+填充在正四面体空隙中, Fe2+和另一半 Fe3+填充在正八面体空隙中。则没有填充阳离子的正四面体空隙数与没有填充阳离子的正八面体空隙数之比为_______ 。FeO 、Fe2O3都具有与Fe3O4相似的立方堆积结构,氧化亚铁晶体的晶胞如图乙所示,已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶体中,与Fe2+紧邻且等距离的Fe2+数目为_______ ;Fe2+与O2-的最短核间距为_______ cm(列出计算式)。

(1)第一电离能介于B、N之间的第二周期元素为
(2)①已知二维硼烯氧化物的部分结构如图所示,则该氧化物的化学式为

②键长和键角的数值可通过晶体的X射线衍射实验获得。经过该实验测定,二维硼烯氧化物中B-B键的键长大于B-O键的键长,其原因是
(3)硼烷又称硼氢化合物,随着硼原子数的增加,硼烷由气态经液态至固态,其原因
(4)LiBH4 -LiI复合材料在低温下表现出较高的离子电导率。BH
 离子中H的化合价为-1,其原因可能是
离子中H的化合价为-1,其原因可能是  可以被PS
可以被PS 离子部分取代,PS
离子部分取代,PS 离子的空间结构为
离子的空间结构为(5)Fe3O4是电子导体,其导电率显著高于Fe2O3,这归因于Fe2+和Fe3+中心之间的电子交换。如图甲所示, Fe3O4晶体中,O2-围成正四面体空隙(如:1、3、6、7围成)和正八面体空隙(如:3、6、7、8、9、12围成),Fe3O4中有一半的Fe3+填充在正四面体空隙中, Fe2+和另一半 Fe3+填充在正八面体空隙中。则没有填充阳离子的正四面体空隙数与没有填充阳离子的正八面体空隙数之比为

您最近一年使用:0次
名校
解题方法
7 . 主族元素N、F、Si、As、Se、Cl等的某些化合物对工农业生产意义重大,回答下列问题:
(1)Si3N4陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于_______ 晶体;SiCl4中Si采取的杂化类型为_______ 。
(2)O、F、Cl电负性由大到小的顺序为_______ ;OF2分子的空间构型为_______ ;OF2的熔、沸点低于Cl2O,原因是_______ 。
(3)Se元素基态原子的原子核外电子排布式为_______ ;As的第一电离能比Se的第一电离能大的原因为_______ 。
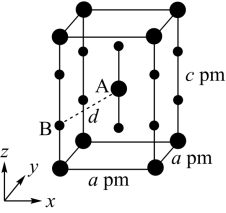
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______ 个XeF2分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,
, ,
, )。已知Xe-F键长为rpm,则B点原子的分数坐标为
)。已知Xe-F键长为rpm,则B点原子的分数坐标为_______ ;晶胞中A、B间距离d=_______ pm。
(1)Si3N4陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于
(2)O、F、Cl电负性由大到小的顺序为
(3)Se元素基态原子的原子核外电子排布式为
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
 ,
, ,
, )。已知Xe-F键长为rpm,则B点原子的分数坐标为
)。已知Xe-F键长为rpm,则B点原子的分数坐标为
您最近一年使用:0次
2022-05-02更新
|
860次组卷
|
7卷引用:陕西省汉中市2022届高三教学质量第二次检测考试理科综合能力测试化学试题
陕西省汉中市2022届高三教学质量第二次检测考试理科综合能力测试化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)(已下线)专题18物质结构与性质(选修)-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题17物质结构与性质(综合题)-2022年高考真题+模拟题汇编(全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)四川省绵阳南山中学2022-2023学年高三上学期入学考试理综化学试题山东省枣庄市第三中学2022-2023学年高三上学期期中考试化学试题
解题方法
8 . 在元素周期表中,铜副族(IB族)包括铜、银、金等元素,在生产、生活和科研中都有着广泛用途和重要的研究价值。
(1)Ag元素在元素周期表分区中属于_______ 区,基态Ag原子的价电子排布式为_______ 。
(2)硫代硫酸银(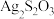 )是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠(
)是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠( )溶液生成
)溶液生成 等络阴离子。
等络阴离子。
①依据 理论推测
理论推测 的空间构型为
的空间构型为_______ ,中心原子S的杂化方式为_______ 。
②在 中配位原子是S原子而非O原子,其原因是
中配位原子是S原子而非O原子,其原因是_______ 。
(3)碘化银常用于做人工增雨剂。其中碘元素形成的最高价氧化物对应水化物有 (偏高碘酸,不稳定)和
(偏高碘酸,不稳定)和 (正高碘酸)等多种形式,它们的酸性
(正高碘酸)等多种形式,它们的酸性
_______  (填“弱于”、“等于”或“强于”)。而
(填“弱于”、“等于”或“强于”)。而 、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是
、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是_______ 。
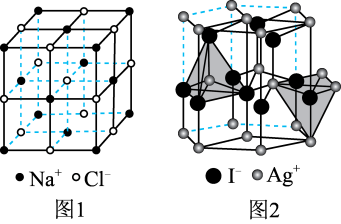
(4)在离子晶体中,当 (阳离子)∶r(阴离子)
(阳离子)∶r(阴离子) 时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知
时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知 ,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为
,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为_______ ,造成AgI晶体结构不同于NaCl晶体结构的原因不可能是_______ (填标号)。
a.几何因素 b.电荷因素 c.键性因素
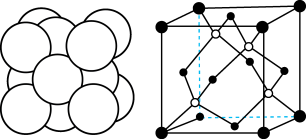
(5)Cu与Au的某种合金可形成面心立方最密堆积的晶体(密度为 ),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为
),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为_______ ;若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_______ (储氢能力 )
)
(1)Ag元素在元素周期表分区中属于
(2)硫代硫酸银(
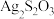 )是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠(
)是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠( )溶液生成
)溶液生成 等络阴离子。
等络阴离子。①依据
 理论推测
理论推测 的空间构型为
的空间构型为②在
 中配位原子是S原子而非O原子,其原因是
中配位原子是S原子而非O原子,其原因是(3)碘化银常用于做人工增雨剂。其中碘元素形成的最高价氧化物对应水化物有
 (偏高碘酸,不稳定)和
(偏高碘酸,不稳定)和 (正高碘酸)等多种形式,它们的酸性
(正高碘酸)等多种形式,它们的酸性
 (填“弱于”、“等于”或“强于”)。而
(填“弱于”、“等于”或“强于”)。而 、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是
、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是(4)在离子晶体中,当
 (阳离子)∶r(阴离子)
(阳离子)∶r(阴离子) 时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知
时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知 ,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为
,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为a.几何因素 b.电荷因素 c.键性因素

(5)Cu与Au的某种合金可形成面心立方最密堆积的晶体(密度为
 ),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为
),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为 )
)
您最近一年使用:0次
2022-04-25更新
|
1252次组卷
|
4卷引用:内蒙古包头市2022届高三第二次模拟考试理综试卷化学试题
内蒙古包头市2022届高三第二次模拟考试理综试卷化学试题(已下线)押全国卷理综第35题 物质结构与性质-备战2022年高考化学临考题号押题(课标全国卷)(已下线)【直抵名校】01-备战2022年高考化学名校进阶模拟卷(通用版)河南省南阳市2021-2022学年高二下学期期末考试化学试题
解题方法
9 . 回答下列问题:
(1)已知:
分析表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的各自原因是_______ 。
②结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时_______ (填化学式)先液化。
(2)SO2与CO2分子的空间结构分别是_______ 和_______ ,相同条件下两者在水中的溶解度较大的是_______ (填化学式),理由是_______ 。
(3)肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4晶体内不存在_______ (填字母)。
a.离子键 b.共价键 c.配位键 d.范德华力
(4)有机物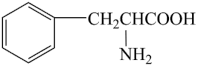 中含有
中含有_______ 个手性碳原子。
(5)“金山银山不如绿水青山”,汽车尾气治理是我国一项重要的任务。经过化学工作者的努力,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
已知:N2(g)+O2(g) 2NO(g) ΔH=+180.5kJ·mol-1
2NO(g) ΔH=+180.5kJ·mol-1
若1mol N2(g)、lmol O2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1mol NO(g)分子中化学键断裂时需吸收的能量为_______ kJ。
(1)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点/K | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度/K | 873 | 773 | 1073 | 713.2 |
①CH4和SiH4比较,NH3和PH3比较,沸点高低的各自原因是
②结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时
(2)SO2与CO2分子的空间结构分别是
(3)肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4晶体内不存在
a.离子键 b.共价键 c.配位键 d.范德华力
(4)有机物
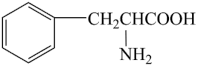 中含有
中含有(5)“金山银山不如绿水青山”,汽车尾气治理是我国一项重要的任务。经过化学工作者的努力,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
已知:N2(g)+O2(g)
 2NO(g) ΔH=+180.5kJ·mol-1
2NO(g) ΔH=+180.5kJ·mol-1若1mol N2(g)、lmol O2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1mol NO(g)分子中化学键断裂时需吸收的能量为
您最近一年使用:0次
解题方法
10 . 物质的结构决定物质的性质。请回答下列问题:
(1)下列有关物质结构与性质的说法中错误的有_______ (填标号)。
A.酸性强弱:三氟乙酸>三氯乙酸>乙酸
B.C2H4分子中的H原子与C原子之间形成s-sp2σ键
C.价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
D.H2S和NH3均是价层电子对数为4的极性分子,且H2S分子的键角较小
E.冰属于分子晶体,其中的氢键可以表示为O- H …O,具有“分子密堆积”特征
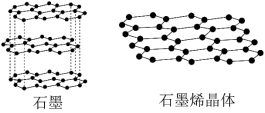
(2)石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体(见下图)。从石墨中剥离出石墨烯需要破坏的作用力是_______ ,12g石墨烯中由碳原子连接成的六元环的物质的量约为_______ mol。
(3)冠醚是由多个二元醇分子之间失水形成的环状化合物,它们能与碱金属离子作用并随着环的大小不同而与不同金属离子作用。由于烯烃难溶于水,故被KMnO4水溶液氧化的效果较差。
①烯烃难溶于水的原因是_______ 。
②若在烯烃中溶人某冠醚,与KMnO4发生如下所示的变化后,氧化效果明显提升。加入该冠醚后,烯烃的氧化效果明显提升的原因是_______ 。
KMnO4+

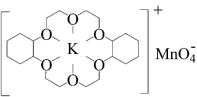
(4)多原子分子中各原子若在同一平面内,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”。下列物质中存在“离域π键”的是_______(填标号)。
(5)硅的含氧化合物都以硅氧四面体(SiO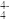 )作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为
)作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为_______ 。在无限长链的硅酸根离子中硅原子与氧原子个数比为_______ 。
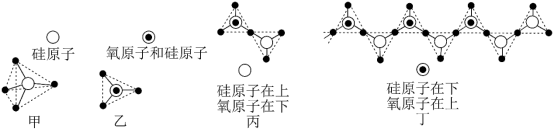
(1)下列有关物质结构与性质的说法中错误的有
A.酸性强弱:三氟乙酸>三氯乙酸>乙酸
B.C2H4分子中的H原子与C原子之间形成s-sp2σ键
C.价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
D.H2S和NH3均是价层电子对数为4的极性分子,且H2S分子的键角较小
E.冰属于分子晶体,其中的氢键可以表示为O- H …O,具有“分子密堆积”特征
(2)石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体(见下图)。从石墨中剥离出石墨烯需要破坏的作用力是

(3)冠醚是由多个二元醇分子之间失水形成的环状化合物,它们能与碱金属离子作用并随着环的大小不同而与不同金属离子作用。由于烯烃难溶于水,故被KMnO4水溶液氧化的效果较差。
①烯烃难溶于水的原因是
②若在烯烃中溶人某冠醚,与KMnO4发生如下所示的变化后,氧化效果明显提升。加入该冠醚后,烯烃的氧化效果明显提升的原因是
KMnO4+



(4)多原子分子中各原子若在同一平面内,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”。下列物质中存在“离域π键”的是_______(填标号)。
| A.苯 | B.三氧化硫 | C.四氯化碳 | D.环己烷 |
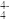 )作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为
)作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为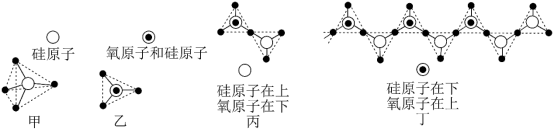
您最近一年使用:0次



