解题方法
1 . 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH2=CH2)与四氟乙烯(CF2=CF2)的共聚物(ETFE)制成。回答下列问题:
(1)画出基态碳原子的价层电子排布图___________ 。
(2)图A、B、C分别表示基态C、N、O和F原子的原子半径、第一电离能和电负性的变化趋势(纵坐标的标度不同)。
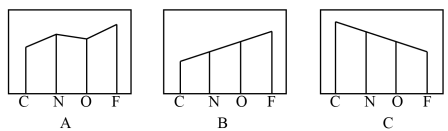
表示原子半径的变化图是___________ (填序号,下同),表示电负性的变化图是___________ 。表示第一电离能的变化图是___________ ,判断第一电离能变化图的根据是___________ 。
(3) 和
和 分子中C原子的杂化轨道类型分别为
分子中C原子的杂化轨道类型分别为___________ 和___________ 。
(4)甲烷与氯气光照发生取代反应能生成多种有机物,其中一氯甲烷(CH3Cl)的价层电子对互斥模型是___________ 形,从分子构型上分析二氯甲烷(CH2Cl2)存在___________ 种分子。
(5)Cu、Al等金属具有良好的导电性,从金属键的角度分析,原因是___________ 。
(6) 的一种晶体与NaCl晶体的结构相似,该
的一种晶体与NaCl晶体的结构相似,该 晶体的一个晶胞中
晶体的一个晶胞中 的数目为
的数目为___________ ,与 相邻的最近的
相邻的最近的 个数
个数___________ 。若晶胞参数为apm,阿伏加德罗常数的值为 ,
, 的摩尔质量为Mg/mol,则该晶体的密度为
的摩尔质量为Mg/mol,则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
(1)画出基态碳原子的价层电子排布图
(2)图A、B、C分别表示基态C、N、O和F原子的原子半径、第一电离能和电负性的变化趋势(纵坐标的标度不同)。

表示原子半径的变化图是
(3)
 和
和 分子中C原子的杂化轨道类型分别为
分子中C原子的杂化轨道类型分别为(4)甲烷与氯气光照发生取代反应能生成多种有机物,其中一氯甲烷(CH3Cl)的价层电子对互斥模型是
(5)Cu、Al等金属具有良好的导电性,从金属键的角度分析,原因是
(6)
 的一种晶体与NaCl晶体的结构相似,该
的一种晶体与NaCl晶体的结构相似,该 晶体的一个晶胞中
晶体的一个晶胞中 的数目为
的数目为 相邻的最近的
相邻的最近的 个数
个数 ,
, 的摩尔质量为Mg/mol,则该晶体的密度为
的摩尔质量为Mg/mol,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
名校
2 . Ⅰ.(多选)对于钠的卤化物(NaX)和硅的卤化物(SiX4),下列叙述正确的是( )
A.SiX4难水解B.SiX4是共价化合物
C.NaX易水解D.NaX的熔点一般高于SiX4
Ⅱ.碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:

回答下列问题:
(1)金刚石、石墨、C60和碳纳米管等都是碳元素的单质形式,它们互为________ 。
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________ 、________ 。
(3)C60属于________ 晶体,石墨属于________ 晶体。
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C-C键的键长为154 pm。其原因是金刚石中只存在C—C间的________ 共价键,而石墨层内的C—C间不仅存在________ 共价键,还有________ 键。
(5)金刚石晶胞含有________ 个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=________ a,列式表示碳原子在晶胞中的空间占有率________ (不要求计算结果)。
A.SiX4难水解B.SiX4是共价化合物
C.NaX易水解D.NaX的熔点一般高于SiX4
Ⅱ.碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:

回答下列问题:
(1)金刚石、石墨、C60和碳纳米管等都是碳元素的单质形式,它们互为
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为
(3)C60属于
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C-C键的键长为154 pm。其原因是金刚石中只存在C—C间的
(5)金刚石晶胞含有
您最近一年使用:0次



