解题方法
1 . 硅及其化合物在生活、生产和科技等方面应用广泛。工业制备高纯硅的主要过程如下:
石英砂(主要成分 )
)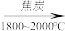 粗硅
粗硅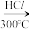

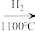 高纯硅
高纯硅
(1) 位于元素周期表第
位于元素周期表第_____ 周期,第_____ 族。
(2)由硅原子核形成的三种微粒,电子排布式分别为:a.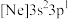 、b.
、b.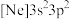 、c.
、c.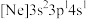 ,有关这些微粒的叙述,正确的是_____(填标号)。
,有关这些微粒的叙述,正确的是_____(填标号)。
(3)石英砂与焦炭反应制备粗硅的化学方程式为_____ 。粗硅与 反应过程中会有副产物
反应过程中会有副产物 生成,
生成, 中
中 的杂化轨道类型为
的杂化轨道类型为_____ 。 的键角
的键角_____ (填“大于”、“小于”或“等于”) 的键角。
的键角。
(4) 以空间结构为
以空间结构为_____ 。 和
和 会剧烈反应,写出该反应的化学方程式
会剧烈反应,写出该反应的化学方程式_____ (已知:电负性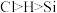 )。
)。
石英砂(主要成分
 )
)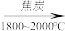 粗硅
粗硅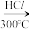

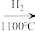 高纯硅
高纯硅(1)
 位于元素周期表第
位于元素周期表第(2)由硅原子核形成的三种微粒,电子排布式分别为:a.
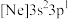 、b.
、b.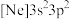 、c.
、c.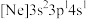 ,有关这些微粒的叙述,正确的是_____(填标号)。
,有关这些微粒的叙述,正确的是_____(填标号)。A.微粒半径: |
| B.电子排布属于基态原子(或离子)的是:a、b |
C.电离一个电子所需最低能量: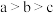 |
D.得电子能力: |
 反应过程中会有副产物
反应过程中会有副产物 生成,
生成, 中
中 的杂化轨道类型为
的杂化轨道类型为 的键角
的键角 的键角。
的键角。(4)
 以空间结构为
以空间结构为 和
和 会剧烈反应,写出该反应的化学方程式
会剧烈反应,写出该反应的化学方程式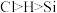 )。
)。
您最近一年使用:0次
2024-04-29更新
|
40次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
解题方法
2 . C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)基态Si原子中存在___________ 种不同能量的电子。
(2)基态Ge原子核外有___________ 种不同空间运动状态的电子。
(3)Si为重要的半导体材料,硅与NaOH溶液反应生成Na2SiO3溶液,该溶液中四种元素电负性由小到大的顺序为___________ 。硅酸盐中的硅酸根离子通常以[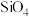 ]四面体(如图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,写出其化学式:
]四面体(如图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,写出其化学式:___________ 。

(4)实验中常用K3[Fe(CN)6]检验Fe2+,K3[Fe(CN)6]中Fe3+的配位数为___________ ,其中碳原子的杂化轨道类型为___________ 。1 mol K3[Fe(CN)6]中含有σ键与π键的数目之比为___________ 。
(5)灰锡的晶体结构(如图3所示)与金刚石相似,其中A处原子的原子分数坐标为(0,0,0),则B处原子的原子分数坐标为___________ 。

(1)基态Si原子中存在
(2)基态Ge原子核外有
(3)Si为重要的半导体材料,硅与NaOH溶液反应生成Na2SiO3溶液,该溶液中四种元素电负性由小到大的顺序为
 ]四面体(如图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,写出其化学式:
]四面体(如图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,写出其化学式:
(4)实验中常用K3[Fe(CN)6]检验Fe2+,K3[Fe(CN)6]中Fe3+的配位数为
(5)灰锡的晶体结构(如图3所示)与金刚石相似,其中A处原子的原子分数坐标为(0,0,0),则B处原子的原子分数坐标为

您最近一年使用:0次
名校
解题方法
3 . 铁氧体是一种磁性材料,具有广泛的应用。
(1)基态铁原子的核外电子排布式为____ 。
(2)工业制备铁氧体常使用水解法,制备时常加入尿素[CO(NH2)2]、醋酸钠等碱性物质。尿素分子中四种不同元素的电负性由大至小的顺序是____ ;醋酸钠中碳原子的杂化类型是____ 。
(3)工业制备铁氧体也可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4)等弱碱。比较表中氨(NH3)、联氨(N2H4)的熔沸点,解释其高低的主要原因____ 。
(4)如图是从铁氧体离子晶体Fe3O4中,取出的能体现其晶体结构的一个立方体,则晶体中的氧离子是否构成了面心立方最密堆积____ (填“是”或“否”),该立方体是不是Fe3O4的晶胞____ (填“是”或“否”),立方体中三价铁离子处于氧离子围成的____ 空隙(填空间结构)。
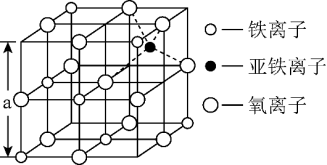
(5)解释该Fe3O4晶体能导电的原因____ ,根据如图计算Fe3O4晶体的密度____ g•cm-3。(图中a=0.42nm,只需要列出计算式。)
(1)基态铁原子的核外电子排布式为
(2)工业制备铁氧体常使用水解法,制备时常加入尿素[CO(NH2)2]、醋酸钠等碱性物质。尿素分子中四种不同元素的电负性由大至小的顺序是
(3)工业制备铁氧体也可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4)等弱碱。比较表中氨(NH3)、联氨(N2H4)的熔沸点,解释其高低的主要原因
| N2H4 | NH3 | |
| 熔点/℃ | 2 | -77.8 |
| 沸点/℃ | 113.5 | -33.5 |

(5)解释该Fe3O4晶体能导电的原因
您最近一年使用:0次
2022-03-18更新
|
176次组卷
|
5卷引用:2017届湖北省黄冈市高三3月质量检测理科综合化学试卷
解题方法
4 . 前四周期元素及其化合物在生产、生活中应用广泛。回答下列问题:
(1)下列状态的N原子或离子在跃迁时,用光谱仪可捕捉到发射光谱的是_______ 。
a. b.
b. c.
c.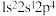 d.
d.
(2)基态铜原子的价电子排布式为_______ 。
(3) 的几何构型为
的几何构型为_______ ,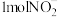 中含有的价层电子对数目为
中含有的价层电子对数目为_______ 。
(4)已知下图均与第三周期的主族元素有关。
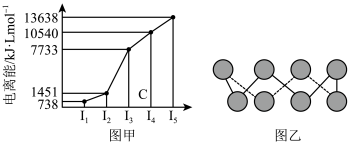
①图甲表示第一至第五电离能数据,则该元素的原子有_______ 种不同运动状态的电子。
②图乙中为某单质的一种同素异形体,分子中的各原子最外层均达到8电子稳定结构,则该元素的原子的杂化轨道类型为_______ ,其易溶于 的原因是
的原因是_______ 。
(5)氨气极易溶于水,溶于水的氨分子大部分与水分子形成氢键,生成一水合氨,关于一水合氨的结构有如下两种可能,正确的是b,理由是_______ 。

(1)下列状态的N原子或离子在跃迁时,用光谱仪可捕捉到发射光谱的是
a.
 b.
b. c.
c.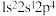 d.
d.
(2)基态铜原子的价电子排布式为
(3)
 的几何构型为
的几何构型为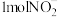 中含有的价层电子对数目为
中含有的价层电子对数目为(4)已知下图均与第三周期的主族元素有关。

①图甲表示第一至第五电离能数据,则该元素的原子有
②图乙中为某单质的一种同素异形体,分子中的各原子最外层均达到8电子稳定结构,则该元素的原子的杂化轨道类型为
 的原因是
的原因是(5)氨气极易溶于水,溶于水的氨分子大部分与水分子形成氢键,生成一水合氨,关于一水合氨的结构有如下两种可能,正确的是b,理由是

您最近一年使用:0次
解题方法
5 . 据报道,我国化学研究人员用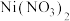 和
和 等合成了一个镍的一维链状配位聚合物(如图),对镍配合物在磁性、电化学性质等方面的研究提出了理论指导。
等合成了一个镍的一维链状配位聚合物(如图),对镍配合物在磁性、电化学性质等方面的研究提出了理论指导。

请回答下列问题:
(1)基态 原子的基态电子排布式为
原子的基态电子排布式为___________ , 在元素周期表中的位置是
在元素周期表中的位置是___________ 。
(2)C、N、O三种元素第一电离能最大的是___________ (填元素符号),C在形成化合物时,其键型以共价键为主,其原因是___________ 。
(3)镍的一维链状配位聚合物中,碳原子的杂化方式为___________ 。已知: 的沸点为117.9℃,
的沸点为117.9℃,  的沸点为32℃。
的沸点为32℃。 的沸点高于
的沸点高于 的沸点的主要原因是
的沸点的主要原因是___________ 。
(4)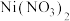 的阴离子为
的阴离子为 ,中心原子N原子的
,中心原子N原子的 键电子对数为
键电子对数为___________ 。阴离子 的空间构型是
的空间构型是___________ 。
(5)氧化镍的晶胞结构如图所示。若 为阿伏加德罗常数的值,晶胞中最近的
为阿伏加德罗常数的值,晶胞中最近的 之间的距离为
之间的距离为 ,则氧化镍的密度为
,则氧化镍的密度为___________  。
。

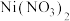 和
和 等合成了一个镍的一维链状配位聚合物(如图),对镍配合物在磁性、电化学性质等方面的研究提出了理论指导。
等合成了一个镍的一维链状配位聚合物(如图),对镍配合物在磁性、电化学性质等方面的研究提出了理论指导。
请回答下列问题:
(1)基态
 原子的基态电子排布式为
原子的基态电子排布式为 在元素周期表中的位置是
在元素周期表中的位置是(2)C、N、O三种元素第一电离能最大的是
(3)镍的一维链状配位聚合物中,碳原子的杂化方式为
 的沸点为117.9℃,
的沸点为117.9℃,  的沸点为32℃。
的沸点为32℃。 的沸点高于
的沸点高于 的沸点的主要原因是
的沸点的主要原因是(4)
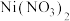 的阴离子为
的阴离子为 ,中心原子N原子的
,中心原子N原子的 键电子对数为
键电子对数为 的空间构型是
的空间构型是(5)氧化镍的晶胞结构如图所示。若
 为阿伏加德罗常数的值,晶胞中最近的
为阿伏加德罗常数的值,晶胞中最近的 之间的距离为
之间的距离为 ,则氧化镍的密度为
,则氧化镍的密度为 。
。
您最近一年使用:0次
名校
解题方法
6 . 我国科学家制备了一种高性能Bi@氮掺杂碳纳米笼。其合成过程如图:

回答下列问题:
(1)Bi(NO3)3·5H2O中各元素电负性从大到小的顺序为___ 。
(2)元素Bi位于第6周期VA族,其基态原子的价电子排布式为____ 。
(3)常温下,1,3,5—苯三甲酸在水中溶解度比苯甲酸大的原因为__ 。
(4) 中氮原子的杂化类型有
中氮原子的杂化类型有__ 。
(5)Bi@氮掺杂碳纳米笼作为钾离子电池负极材料,充电时存在Bi到钾铋合金的两步转变,其晶胞结构转变如图所示:

①合金M中离钾原子最近的钾原子有__ 个。
②合金N的化学式为____ 。

回答下列问题:
(1)Bi(NO3)3·5H2O中各元素电负性从大到小的顺序为
(2)元素Bi位于第6周期VA族,其基态原子的价电子排布式为
(3)常温下,1,3,5—苯三甲酸在水中溶解度比苯甲酸大的原因为
(4)
 中氮原子的杂化类型有
中氮原子的杂化类型有(5)Bi@氮掺杂碳纳米笼作为钾离子电池负极材料,充电时存在Bi到钾铋合金的两步转变,其晶胞结构转变如图所示:

①合金M中离钾原子最近的钾原子有
②合金N的化学式为
您最近一年使用:0次
2021-05-01更新
|
68次组卷
|
2卷引用:湖北省黄冈市示范高中蕲春四中2020-2021学年高二下学期5月月考化学试题
名校
解题方法
7 . 硫、钒化合物在药物化学及催化化学等领域应用广泛。回答下列问题:
(1)基态钒原子的价层电子排布图为_______ ,钒有+2、+3、+4、+5等多种化合价,其中最稳定的化合价是_______ , 的空间构型为
的空间构型为_______ 。
(2)2-巯基烟酸氧钒配合物(图甲)是副作用小的有效调节血糖的新型药物:
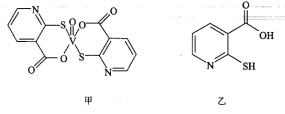
该药物中N原子的杂化方式是_______ ;2-巯基烟酸(图乙)水溶性优于2-巯基烟酸氧钒配合物(图甲)的原因是_______ 。
(3)某六方硫钒化合物晶体的晶胞如图丙所示,该晶胞的化学式为_______ 。图丁为该晶胞的俯视图,该晶胞的密度为_______  (列出计算式即可)。
(列出计算式即可)。

(1)基态钒原子的价层电子排布图为
 的空间构型为
的空间构型为(2)2-巯基烟酸氧钒配合物(图甲)是副作用小的有效调节血糖的新型药物:

该药物中N原子的杂化方式是
(3)某六方硫钒化合物晶体的晶胞如图丙所示,该晶胞的化学式为
 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
2021-03-22更新
|
329次组卷
|
3卷引用:湖北省罗田县第一中学2020-2021学年高二下学期第一次月考化学试题
解题方法
8 . 均由两种短周期元素组成的A、B、C、D四种化合物分子都含有18个电子,四种化合物分子中所含原子的数目依次为2、3、4、6。A和C分子中各元素原子的个数比均为1:1,B和D分子中各元素原子的个数比均为1:2。D可作为火箭推进剂的燃料。请回答下列问题。
(1)A与HF相比,其沸点较低,原因是____ 。
(2)B分子的立体构型为____ 形,该分子属于____ (填“极性”或“非极性”)分子。
(3)A、B两种化合物分子的非氢元素原子的最高价氧化物对应的水化物的酸性强弱顺序为____ (用化学式表示),设A分子的非氢元素原子为X,B分子的中心原子为Y,比较下列物质的酸性强弱:HXO_____ HXO3____ HXO4(填“>”“<”或“=”,下同);H2YO3____ H2YO4。
(4)D分子中心原子的杂化方式是____ ,由该原子组成的单质分子中包含____ 个π键,与该单质分子互为等电子体的常见分子的分子式为___ 。
(1)A与HF相比,其沸点较低,原因是
(2)B分子的立体构型为
(3)A、B两种化合物分子的非氢元素原子的最高价氧化物对应的水化物的酸性强弱顺序为
(4)D分子中心原子的杂化方式是
您最近一年使用:0次
名校
解题方法
9 . 过渡元素铜的配合物在物质制备、尖端技术、医药科学、催化反应、材料化学等领域有着广泛的应用。请回答下列问题:
(1)科学家推测胆矾(CuSO4·5H2O)的结构示意图可简单表示如下图:

用配合物的形式表示胆矾的化学式为______ ; 的空间构型为
的空间构型为______ ,其中硫原子的轨道杂化方式为______ 。
(2)Cu能与(SCN)2反应生成Cu(SCN)2。1 mol(SCN)2中含有的π键数目为______ ;(SCN)2对应的酸有两种,分别为硫氰酸 和异硫氰酸
和异硫氰酸 ,其中异硫氰酸的沸点较高,原因是
,其中异硫氰酸的沸点较高,原因是______ 。
(3)向硫酸铜溶液中,加入NaCl固体,溶液由蓝色变为黄绿色,则溶液中铜元素的主要存在形式是______ (写微粒符号);向上述溶液中继续滴加浓氨水,先有蓝色沉淀生成,继续滴加浓氨水后,沉淀溶解,溶液变为深蓝色。沉淀溶解的原因是______ (用离子方程式表示)。
(4)Cu单独与氨水、过氧化氢都不反应,但能与氨水和过氧化氢的混合溶液反应,发生的化学方程式为______ 。
(1)科学家推测胆矾(CuSO4·5H2O)的结构示意图可简单表示如下图:

用配合物的形式表示胆矾的化学式为
 的空间构型为
的空间构型为(2)Cu能与(SCN)2反应生成Cu(SCN)2。1 mol(SCN)2中含有的π键数目为
 和异硫氰酸
和异硫氰酸 ,其中异硫氰酸的沸点较高,原因是
,其中异硫氰酸的沸点较高,原因是(3)向硫酸铜溶液中,加入NaCl固体,溶液由蓝色变为黄绿色,则溶液中铜元素的主要存在形式是
(4)Cu单独与氨水、过氧化氢都不反应,但能与氨水和过氧化氢的混合溶液反应,发生的化学方程式为
您最近一年使用:0次
2021-01-29更新
|
269次组卷
|
3卷引用:湖北省黄冈市黄梅县育才高级中学2023-2024学年高二下学期3月月考化学试题
解题方法
10 . 一种Ru络合物与g-C3N4复合光催化剂将CO,还原为HCOOH的原理图如图。
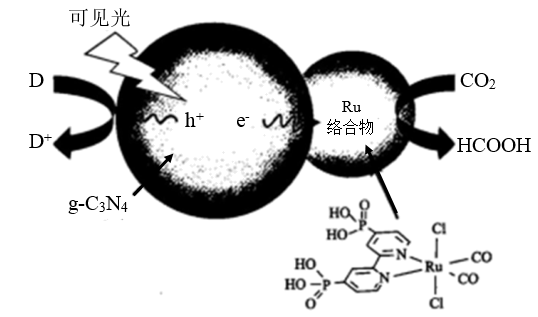
(1)基态碳原子的价电子排布图为___________ 。
(2)1molHCOOH中含有的σ键数目为___________ ,HCOOH的沸点比CO2高的原因为___________ 。
(3)Ru络合物中第二周期元素的第一电离能由大到小的顺序为___________ 。
(4)Ru络合物中与Ru配位的原子有N、___________ 。
(5)一类石墨的聚合物半导体g-C3N4,其单层平面结构如图1,晶胞结构如图2。
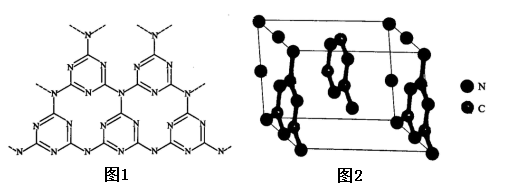
①g-C3N4中氮原子的杂化类型是______________ 。
②根据图2,在图1中用平行四边形画出一个最小重复单元。______________
③已知该晶胞的体积为Vcm3,中间层原子均在晶胞内部。设阿伏加 德罗常数的值为NA,则g-C3N4的密度为______________ g.cm-3。

(1)基态碳原子的价电子排布图为
(2)1molHCOOH中含有的σ键数目为
(3)Ru络合物中第二周期元素的第一电离能由大到小的顺序为
(4)Ru络合物中与Ru配位的原子有N、
(5)一类石墨的聚合物半导体g-C3N4,其单层平面结构如图1,晶胞结构如图2。

①g-C3N4中氮原子的杂化类型是
②根据图2,在图1中用平行四边形画出一个最小重复单元。
③已知该晶胞的体积为Vcm3,中间层原子均在晶胞内部。设阿伏加 德罗常数的值为NA,则g-C3N4的密度为
您最近一年使用:0次



