名校
1 . 对下列一些实验事实的理论解释,错误的是
| 选项 | 实验事实 | 理论解释 |
| A | P原子的第一电离能大于S原子 | 磷原子的半径比硫原子的半径大 |
| B | 乙烯的化学性质比乙烷活泼 | 乙烯分子结构中存在π键 |
| C | 向加入过量氨水的硫酸铜溶液中加入乙醇,将析出深蓝色晶体 | 乙醇的加入降低了[Cu(NH3)4]SO4·H2O的溶解度 |
| D | HCl气体极易溶于水 | HCl和H2O均为极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 冠醚能与阳离子作用,将阳离子以及对应的阴离子都带入有机溶剂,例如 水溶液对烯烃的氧化效果较差,在烯烃中溶入冠醚,可使氧化反应迅速发生,原理如图。
水溶液对烯烃的氧化效果较差,在烯烃中溶入冠醚,可使氧化反应迅速发生,原理如图。
 水溶液对烯烃的氧化效果较差,在烯烃中溶入冠醚,可使氧化反应迅速发生,原理如图。
水溶液对烯烃的氧化效果较差,在烯烃中溶入冠醚,可使氧化反应迅速发生,原理如图。
| A.冠醚属于超分子 |
B.冠醚与 结合后将 结合后将 带入烯烃中, 带入烯烃中, 与烯烃充分接触而迅速反应 与烯烃充分接触而迅速反应 |
C. 通过配位键与冠醚相结合 通过配位键与冠醚相结合 |
| D.冠醚中C、O原子间的化学键为σ键 |
您最近一年使用:0次
2024-02-08更新
|
574次组卷
|
5卷引用:吉林省长春吉大附中实验学校2023-2024学年高二上学期1月期末化学试题
吉林省长春吉大附中实验学校2023-2024学年高二上学期1月期末化学试题(已下线)3.4 配合物与超分子-随堂练习辽宁省沈阳市东北育才学校高中部2023-2024学年高二下学期第1次月考化学试题内蒙古师范大学锦山实验中学2023-2024学年高二下学期一调考试化学试题(已下线)清单03 晶体结构与性质(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
名校
解题方法
3 . 下列实验事实的理论解释不正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 磷原子的第一电离能大于硫原子 | 磷原子3p能级半充满 |
| B |  分子在水中有一定溶解度 分子在水中有一定溶解度 |  与水分子极性上相似 与水分子极性上相似 |
| C | 浓 溶液显绿色,加水稀释过程中变蓝 溶液显绿色,加水稀释过程中变蓝 |  与 与 、 、 均能形成配合物 均能形成配合物 |
| D | 石墨比金刚石熔点高 | 金刚石碳碳键键能更小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-08更新
|
105次组卷
|
2卷引用:吉林省长春吉大附中实验学校2023-2024学年高二上学期1月期末化学试题
解题方法
4 . 下列说法正确的是
A.第一电离能: |
B. 的键角比 的键角比 大 大 |
C. 分子构型为平面型 分子构型为平面型 |
D.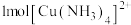 中 中 键的数目为12mol 键的数目为12mol |
您最近一年使用:0次
2024-02-04更新
|
328次组卷
|
2卷引用:江苏省南京师范大学苏州实验学校2023-2024学年高三上学期零模考试热身练化学试题
名校
5 . 铁、铜、锌是形成许多金属材料和有机材料的重要组成元素。回答下列问题:
(1)金属铜在元素周期表_______ 区。
(2)铜和锌同周期且相邻,现有几种铜、锌元素的相应状态,①锌: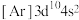 、②锌:
、②锌: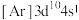 、③铜:
、③铜: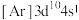 、④铜:
、④铜: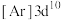 ,失去1个电子需要的能量由大到小排序是
,失去1个电子需要的能量由大到小排序是_______ 。
(3)向 溶液中滴加氨水可以得到
溶液中滴加氨水可以得到 型离子化合物,其阳离子结构如图所示。
型离子化合物,其阳离子结构如图所示。_______ 。
A.该阳离子中存在的化学键有极性共价键、配位键和氢键
B.溶液中的阴离子为正四面体结构
C.电负性大小:
D.往该溶液中继续加95%乙醇,并用玻璃棒摩擦试管壁,析出深蓝色晶体
②该化合物加热时首先失去的组分是 ,原因是
,原因是_______ 。
(4)铁及其化合物在生产、生活中有重要应用。
①改性 是一种优良的磁性材料,该
是一种优良的磁性材料,该 晶胞的
晶胞的 的结构如图所示,研究发现结构中的
的结构如图所示,研究发现结构中的 只可能出现在图中某一“▲”所示位置上,请确定
只可能出现在图中某一“▲”所示位置上,请确定 所在晶胞的位置
所在晶胞的位置_______ (填a或b或c)。 。铁-氰骨架组成小立方体,Fe粒子在顶点,
。铁-氰骨架组成小立方体,Fe粒子在顶点, 在棱上,两端均与Fe相连,立方体中心空隙可容纳
在棱上,两端均与Fe相连,立方体中心空隙可容纳 ,如图所示(
,如图所示( 在图中省略)。普鲁士蓝中
在图中省略)。普鲁士蓝中 与
与 个数之比为
个数之比为_______ ;该晶胞的化学式为_______ 。
(1)金属铜在元素周期表
(2)铜和锌同周期且相邻,现有几种铜、锌元素的相应状态,①锌:
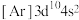 、②锌:
、②锌: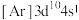 、③铜:
、③铜: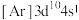 、④铜:
、④铜: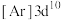 ,失去1个电子需要的能量由大到小排序是
,失去1个电子需要的能量由大到小排序是(3)向
 溶液中滴加氨水可以得到
溶液中滴加氨水可以得到 型离子化合物,其阳离子结构如图所示。
型离子化合物,其阳离子结构如图所示。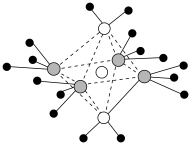
A.该阳离子中存在的化学键有极性共价键、配位键和氢键
B.溶液中的阴离子为正四面体结构
C.电负性大小:

D.往该溶液中继续加95%乙醇,并用玻璃棒摩擦试管壁,析出深蓝色晶体

②该化合物加热时首先失去的组分是
 ,原因是
,原因是(4)铁及其化合物在生产、生活中有重要应用。
①改性
 是一种优良的磁性材料,该
是一种优良的磁性材料,该 晶胞的
晶胞的 的结构如图所示,研究发现结构中的
的结构如图所示,研究发现结构中的 只可能出现在图中某一“▲”所示位置上,请确定
只可能出现在图中某一“▲”所示位置上,请确定 所在晶胞的位置
所在晶胞的位置
 。铁-氰骨架组成小立方体,Fe粒子在顶点,
。铁-氰骨架组成小立方体,Fe粒子在顶点, 在棱上,两端均与Fe相连,立方体中心空隙可容纳
在棱上,两端均与Fe相连,立方体中心空隙可容纳 ,如图所示(
,如图所示( 在图中省略)。普鲁士蓝中
在图中省略)。普鲁士蓝中 与
与 个数之比为
个数之比为
您最近一年使用:0次
名校
解题方法
6 . 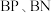 晶体结构与金刚石相似,是硬度大、耐磨、耐高温的材料,
晶体结构与金刚石相似,是硬度大、耐磨、耐高温的材料,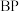 合成途径之一为
合成途径之一为 ,下列说法错误的是
,下列说法错误的是
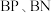 晶体结构与金刚石相似,是硬度大、耐磨、耐高温的材料,
晶体结构与金刚石相似,是硬度大、耐磨、耐高温的材料,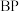 合成途径之一为
合成途径之一为 ,下列说法错误的是
,下列说法错误的是A. 与 与 的空间结构均为平面三角形 的空间结构均为平面三角形 | B.沸点: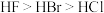 |
C.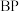 与 与 中既有共价键又有配位链 中既有共价键又有配位链 | D.基态硼原子的电子排布图: |
您最近一年使用:0次
2024-02-02更新
|
200次组卷
|
3卷引用:河北省2023-2024学年高三上学期质量监测期末联考化学试题
名校
解题方法
7 . 碳和硫的化合物种类繁多,应用广泛。例如CS2是一种优良的溶剂,也是用于制造黏胶纤维、玻璃的重要原材料。回答下列问题。
I.CCl4曾广泛用作溶剂、灭火剂。
(1)基态氯原子价层电子的空间运动状态有___________ 种。基态碳原子的价电子排布是否可以表示为 ,
,___________ (填“是”或“否”),原因为___________ 。
(2)CCl4在500℃以上时可以与水反应,产生有毒的光气(COCl2)。SiCl4常温遇水水解作用很激烈,产生浑浊和气体。造成两者水解差异的因素有___________ (填标号)。
a.Si的原子半径更大 b.Si-Cl键的键能更大
c.Si-Cl键的极性更大 d.Si有更多的价层轨道
光气分子中Cl-C-Cl的键角___________ (填“大于”、“小于”或“等于”)甲醛分子中H-C-H的键角,原因为___________ 。
Ⅱ.硫代硫酸盐可用于矿石提取银、鞣制皮革等。
(3)硫代硫酸根( )中心原子的杂化方式为
)中心原子的杂化方式为___________ 。硫代硫酸盐用于矿石提取银时形成 ,该配合物中提供孤电子对的原子为
,该配合物中提供孤电子对的原子为___________ (填标号),原因为___________ 。
a.端基硫原子 b.中心硫原子 c.氧原子
(4)某硫代硫酸盐的晶胞结构如图。Mn+的n=___________ 。原子b的分数坐标为(0,0,0),则原子a的分数坐标为___________ 。
I.CCl4曾广泛用作溶剂、灭火剂。
(1)基态氯原子价层电子的空间运动状态有
 ,
,(2)CCl4在500℃以上时可以与水反应,产生有毒的光气(COCl2)。SiCl4常温遇水水解作用很激烈,产生浑浊和气体。造成两者水解差异的因素有
a.Si的原子半径更大 b.Si-Cl键的键能更大
c.Si-Cl键的极性更大 d.Si有更多的价层轨道
光气分子中Cl-C-Cl的键角
Ⅱ.硫代硫酸盐可用于矿石提取银、鞣制皮革等。
(3)硫代硫酸根(
 )中心原子的杂化方式为
)中心原子的杂化方式为 ,该配合物中提供孤电子对的原子为
,该配合物中提供孤电子对的原子为a.端基硫原子 b.中心硫原子 c.氧原子
(4)某硫代硫酸盐的晶胞结构如图。Mn+的n=

您最近一年使用:0次
2024-02-02更新
|
468次组卷
|
4卷引用:山东省青岛市黄岛区2023-2024学年高三上学期期末考试化学试题
名校
解题方法
8 . 下列有关物质结构与性质的说法中,错误的是
A.在 中的溶解性: 中的溶解性: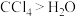 |
B.沸点: |
C.酸性: |
D.利用超分子特征,“杯酚”可将 和 和 分离 分离 |
您最近一年使用:0次
2024-02-02更新
|
218次组卷
|
3卷引用:四川省德阳市高中2023-2024学年学年高二上学期期末教学质量检测考试化学试题
四川省德阳市高中2023-2024学年学年高二上学期期末教学质量检测考试化学试题吉林省长春外国语学校2023-2024学年高二下学期开学化学试题(已下线)猜想03 晶体结构与性质 【考题猜想】(8大题型)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
名校
9 . 乙酰乙酸乙酯存在酮式与烯醇式的互变异构,其中烯醇式可与 结合产生紫色,其结构如图所示,下列有关该配离子的说法正确的是
结合产生紫色,其结构如图所示,下列有关该配离子的说法正确的是
 结合产生紫色,其结构如图所示,下列有关该配离子的说法正确的是
结合产生紫色,其结构如图所示,下列有关该配离子的说法正确的是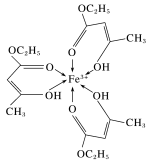
A. 有23种空间运动状态的电子 有23种空间运动状态的电子 |
| B.该配离子中含有6个配体 |
C.该配离子中碳原子的杂化类型有 、 、 杂化 杂化 |
| D.该配离子中含有的化学键有离子键、极性键、非极性键、配位键 |
您最近一年使用:0次
2024-02-01更新
|
441次组卷
|
6卷引用:山东省德州市2023-2024学年高二上学期期末考试化学试题
山东省德州市2023-2024学年高二上学期期末考试化学试题(已下线)热点09 配合物和超分子(已下线)3.4.1 配合物与超分子(提高)河南省信阳高级中学2023-2024学年高二下学期开学化学试题山东省临沂市第二十四中学2023-2024学年高二下学期3月学科素养水平监测化学试题山东省德州市2023-2024学年高二上学期期末考试化学试题
名校
解题方法
10 . 同一周期主族元素W、Z、X、Y原子序数依次增大,X原子的最外层电子数是W原子的次外层电子数的3倍,由四种元素原子形成的阴离子结构如图,下列说法正确的是
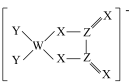
| A.Z位于元素周期表第2周期ⅥA族 | B.以W为中心原子形成的VSEPR模型为平面三角形 |
| C.该阴离子中含有配位键 | D.最高价氧化物对应水化物的酸性:Y>Z>W |
您最近一年使用:0次
2024-02-01更新
|
232次组卷
|
3卷引用:山东省德州市2023-2024学年高二上学期期末考试化学试题



