名校
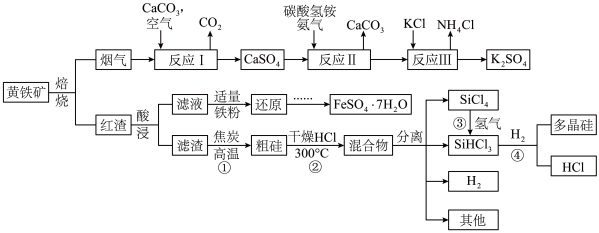
1 . 近日,武汉市第十二中学的“化学妙妙屋”社团以黄铁矿FeS2(杂质为石英)为原料,设计了如下工艺流程:
(1)在空气中焙烧黄铁矿的化学方程式为:___________ 。
(2)检验反应Ⅱ所得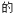 滤液中所含阴离子的方法是
滤液中所含阴离子的方法是___________ 。
(3)向红渣酸浸得到的滤液中加入适量铁粉还原,再由还原后的滤液制得FeSO4·7H2O的操作为:___________ 、___________ 、过滤、洗涤、干燥。
(4)反应③氢化SiCl4过程中所需的高纯度H2可通过电解精制的饱和食盐水制得,电解过程中同时生成一种黄绿色的气体和一种易溶、易电离的碱,电解反应的离子方程式是___________ 。粗盐水精制过程中,为有效除去 、
、 、
、 等杂质,要按
等杂质,要按___________ 顺序(填标号)加入下列溶液,过滤后再向滤液中加___________ 调节pH。
a.NaOH b.Na2CO3 c.BaCl2
(1)在空气中焙烧黄铁矿的化学方程式为:
(2)检验反应Ⅱ所得
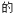 滤液中所含阴离子的方法是
滤液中所含阴离子的方法是(3)向红渣酸浸得到的滤液中加入适量铁粉还原,再由还原后的滤液制得FeSO4·7H2O的操作为:
(4)反应③氢化SiCl4过程中所需的高纯度H2可通过电解精制的饱和食盐水制得,电解过程中同时生成一种黄绿色的气体和一种易溶、易电离的碱,电解反应的离子方程式是
 、
、 、
、 等杂质,要按
等杂质,要按a.NaOH b.Na2CO3 c.BaCl2
您最近一年使用:0次
名校
解题方法
2 . V2O5(五氧化二钒)可作化学工业中的催化剂。为回收利用含钒催化剂,研制了一种利用废催化剂(含有V2O5、VOSO4、不溶性硅酸盐)回收V2O5的新工艺流程如下:
②部分含钒物质常温下在水中的溶解性如表所示:
③ +2OH-
+2OH-
 +H2O
+H2O
回答下列问题:
(1)在滤渣1中加入Na2SO3和过量H2SO4溶液发生反应生成VOSO4的化学方程式为___________ 。
(2)在第Ⅱ步中需要加入氨水,请结合 +2OH-
+2OH-
 +H2O,用平衡移动原理解释加入氨水的作用为
+H2O,用平衡移动原理解释加入氨水的作用为___________ 。
(3)需在流动空气中加热NH4VO3的原因可能是___________ 。
(4)将0.250g产品溶于强碱溶液中,加热煮沸,调节pH为8~8.5,向反应后的溶液中加入硫酸酸化的KI溶液(过量),溶液中的还原产物为V3+离子,滴加指示剂,用0.250mol/LNa2S2O3溶液滴定,达到终点时消耗Na2S2O3标准溶液20.00mL,则该产品的纯度为___________ (保留4位有效数字)。(已知:I2+2 Na2S2O3= Na2S4O6+2NaI,写出计算过程)

②部分含钒物质常温下在水中的溶解性如表所示:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
 +2OH-
+2OH-
 +H2O
+H2O回答下列问题:
(1)在滤渣1中加入Na2SO3和过量H2SO4溶液发生反应生成VOSO4的化学方程式为
(2)在第Ⅱ步中需要加入氨水,请结合
 +2OH-
+2OH-
 +H2O,用平衡移动原理解释加入氨水的作用为
+H2O,用平衡移动原理解释加入氨水的作用为(3)需在流动空气中加热NH4VO3的原因可能是
(4)将0.250g产品溶于强碱溶液中,加热煮沸,调节pH为8~8.5,向反应后的溶液中加入硫酸酸化的KI溶液(过量),溶液中的还原产物为V3+离子,滴加指示剂,用0.250mol/LNa2S2O3溶液滴定,达到终点时消耗Na2S2O3标准溶液20.00mL,则该产品的纯度为
您最近一年使用:0次
名校
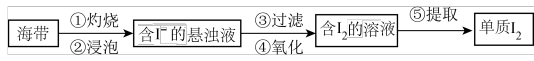
3 . 海带中含有碘元素,从海带中提取碘的实验过程如下图:
(2)步骤④选用的试剂为氯水,则该反应的离子方程式为_____ ;检验该步骤中有I2生成的方法是_____ 。
(3)步骤⑤包含以下四个过程:
_____ (填“能”或“不能”)用乙醇代替。
②过程Ⅱ中 与浓
与浓 溶液反应的离子方程式为
溶液反应的离子方程式为_____ 。
③过程Ⅲ中化合价发生变化的元素为_____ (填元素符号)。
④过程Ⅳ的操作名称为_____ 。
| A.泥三角 | B.漏斗 | C.坩埚 | D.酒精灯 |
(2)步骤④选用的试剂为氯水,则该反应的离子方程式为
(3)步骤⑤包含以下四个过程:


②过程Ⅱ中
 与浓
与浓 溶液反应的离子方程式为
溶液反应的离子方程式为③过程Ⅲ中化合价发生变化的元素为
④过程Ⅳ的操作名称为
您最近一年使用:0次
名校
4 . 下列用洗气的方法,去除气体中杂质的方案不正确的是
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 |
| A | CO2 | SO2 | 饱和NaHSO3溶液 |
| B | NO | NO2 | H2O |
| C | Cl2 | HCl | 饱和NaCl溶液 |
| D | N2 | NH3 | H2SO4 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 工业上用黄铁矿( )为原料制备硫酸的流程如图。下列说法错误的是
)为原料制备硫酸的流程如图。下列说法错误的是
 )为原料制备硫酸的流程如图。下列说法错误的是
)为原料制备硫酸的流程如图。下列说法错误的是
A.步骤①中得到的铁的氧化物可以是 或 或 |
| B.若气体A过量则煅烧黄铁矿可直接得到气体B |
C.气体B经步骤③吸收后,尾气中的 经富集后可返回步骤②循环利用 经富集后可返回步骤②循环利用 |
D.步骤③用 浓硫酸吸收气体B比用水效果好 浓硫酸吸收气体B比用水效果好 |
您最近一年使用:0次
名校
6 . 闽盐集团晾晒海水获得的粗盐中含有可溶性杂质 、
、 、
、 等。粗盐提纯的工艺流程如下,下列说法正确的是
等。粗盐提纯的工艺流程如下,下列说法正确的是
 、
、 、
、 等。粗盐提纯的工艺流程如下,下列说法正确的是
等。粗盐提纯的工艺流程如下,下列说法正确的是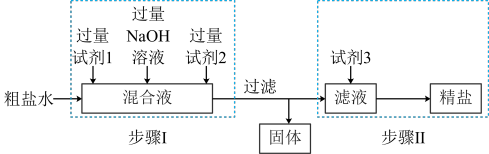
A.“步骤Ⅰ”中试剂1为 溶液,试剂2为 溶液,试剂2为 溶液 溶液 |
| B.“步骤Ⅰ”生成的沉淀也可在加完试剂3之后一次性过滤 |
| C.“步骤Ⅱ”试剂3可以用稀硫酸代替稀盐酸 |
| D.“步骤Ⅱ”从滤液中获得精盐的方法是蒸发结晶 |
您最近一年使用:0次
名校
7 . 一节1号干电池可以让1平方米土地上的庄稼颗粒无收,回收电池既可以防止污染又可以变废为宝。废旧锌锰干电池内部的黑色物质A主要含有 、
、 、
、 、
、 、碳单质、少量有机物(有机物易燃烧生成
、碳单质、少量有机物(有机物易燃烧生成 和
和 ),用黑色物质A制备高纯
),用黑色物质A制备高纯 的流程如图:
的流程如图:________ (填化学式)。
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为 ,另一个是
,另一个是________ 。灼烧时,MnOOH与空气中的氧气反应的化学方程式为________________ 。
(3)第III步中为提高反应速率,可以采取的措施有________ (任写一条)。
(4)已知: 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第IV步中的多步操作可按如图步骤进行:
沉淀。第IV步中的多步操作可按如图步骤进行: 溶液调节溶液pH的过程中有
溶液调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为________________ ;
②操作VI中需要的玻璃仪器有________ ;
③你认为操作VII中检测的方法及现象是________ 时可继续进行操作VIII;
④操作VIII中用无水乙醇洗涤的目的是________ 。
 、
、 、
、 、
、 、碳单质、少量有机物(有机物易燃烧生成
、碳单质、少量有机物(有机物易燃烧生成 和
和 ),用黑色物质A制备高纯
),用黑色物质A制备高纯 的流程如图:
的流程如图:
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为
 ,另一个是
,另一个是(3)第III步中为提高反应速率,可以采取的措施有
(4)已知:
 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第IV步中的多步操作可按如图步骤进行:
沉淀。第IV步中的多步操作可按如图步骤进行: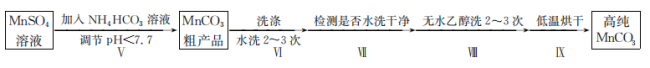
 溶液调节溶液pH的过程中有
溶液调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为②操作VI中需要的玻璃仪器有
③你认为操作VII中检测的方法及现象是
④操作VIII中用无水乙醇洗涤的目的是
您最近一年使用:0次
解题方法
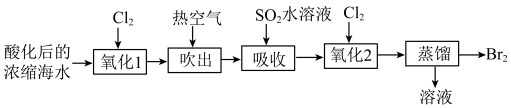
8 . 工业上可利用“吹出法”提溴。“吹出法”提溴的流程如图所示: 等离子。下列说法正确的是
等离子。下列说法正确的是
 等离子。下列说法正确的是
等离子。下列说法正确的是| A.取“吹出”后的溶液滴加到淀粉碘化钾试纸上,若试纸变蓝,则说明溶液中含Cl2 |
| B.“氧化1”中,Cl2过量会增大“吸收”时SO2水溶液的用量 |
C.“吸收”时,溶液中发生反应的离子方程式为Br2+SO2+2H2O=2HBr+2H++SO |
D.蒸馏后溶液中主要存在的离子:Na+、Mg2+、Cl-和SO |
您最近一年使用:0次
解题方法
9 . 铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为_______ ,发生反应的离子方程式为_______ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 在同温同压下的体积之比是
在同温同压下的体积之比是_______ 。
(3)氢氧化亚铁在空气中会逐渐被氧化为氢氧化铁,其化学方程式为_______ 。
(4)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:_______ 。
② 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为_______ 。
③滤液II中溶质的用途之一是_______ 。
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 在同温同压下的体积之比是
在同温同压下的体积之比是(3)氢氧化亚铁在空气中会逐渐被氧化为氢氧化铁,其化学方程式为
(4)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:
②
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为③滤液II中溶质的用途之一是
您最近一年使用:0次
10 . 从某工业废水中(含 、
、 、
、 、
、 、
、 )回收利用Al和
)回收利用Al和 的工艺流程如图所示。下列说法错误的是
的工艺流程如图所示。下列说法错误的是
 、
、 、
、 、
、 、
、 )回收利用Al和
)回收利用Al和 的工艺流程如图所示。下列说法错误的是
的工艺流程如图所示。下列说法错误的是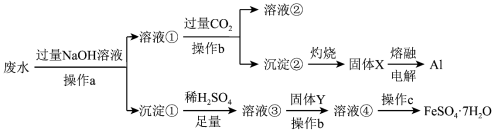
| A.操作a、b均是过滤,c蒸发浓缩、冷却结晶 |
B.溶液①中不止一种物质与 发生反应 发生反应 |
| C.溶液②的溶质主要是NaCl和Na2CO3 |
| D.固体Y可以是铁粉 |
您最近一年使用:0次



