贵州省黔南布依族苗族自治州龙里中学2019-2020学年高一上学期期末考试化学试题
贵州
高一
期末
2020-02-21
667次
整体难度:
容易
考查范围:
认识化学科学、化学实验基础、化学与STSE、常见无机物及其应用、物质结构与性质
一、单选题 添加题型下试题
| A.镁的最外层电子数比铝少 | B.镁带在二氧化碳中能燃烧,而铝不能 |
C.镁的密度比铝小,约为铝的 | D.铝和镁相比较,铝的硬度大、熔点高 |
【知识点】 氧化性、还原性强弱的比较解读
| A.①②③④ | B.①②③④⑦ | C.①②④⑦ | D.①②③④⑤⑥⑦ |
【知识点】 氧化还原反应基本概念
| A.Mg | B.Cu | C.Ag | D.H2 |
| A.由两种或两种以上元素组成的纯净物称为化合物 |
| B.由一种元素组成的纯净物是单质 |
| C.由一种物质组成的是纯净物 |
| D.含氧元素的化合物称为氧化物 |
【知识点】 单质和化合物解读 酸、碱、盐、氧化物的概念及其相互联系解读
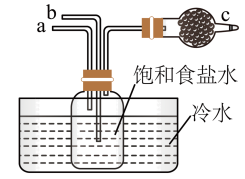
| A.a通入CO2,然后b通入NH3,c中放碱石灰 |
| B.b通入NH3,然后a通入CO2,c中放碱石灰 |
| C.a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉 |
| D.b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉 |
| A.混合气体中含二氧化氮1.12L |
| B.消耗氧气的体积为1.68L |
| C.此反应过程中转移的电子为0.3mol |
| D.参加反应的硝酸是0.4mol |
| A.1:1 | B.1:2 | C.1:3 | D.3:1 |
| A.得电子越多,其氧化性越强 |
| B.分子中一定含有氧元素 |
| C.在反应中易失电子的物质 |
| D.在反应中易结合电子的物质 |
【知识点】 氧化还原反应的几组概念解读
| A.蒸发、蒸馏、萃取 | B.萃取、蒸馏、蒸发 |
| C.蒸发、萃取、蒸馏 | D.蒸馏、萃取、蒸发 |
【知识点】 物质分离、提纯的常见物理方法
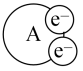 是
是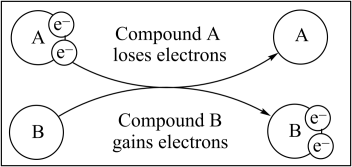
| A.还原剂 | B.氧化剂 | C.氧化产物 | D.还原产物 |
【知识点】 氧化还原反应的几组概念解读
| A.F2 | B.Cl2 | C.HCl | D.CO2 |
【知识点】 阿伏加德罗定律
| A.7、2 | B.5、4 | C.6、3 | D.3、6 |
【知识点】 硅酸盐组成的表示方法解读
| A.硝酸银晶体保存在棕色试剂瓶中 | B.固体烧碱保存在橡胶塞细口试剂瓶中 |
| C.白磷保存在玻璃塞广口瓶中 | D.浓盐酸可存放在敞口容器中 |
| A.酒精和水 | B.食盐和蔗糖 | C.泥沙和食盐 | D.铜粉和铝粉 |
【知识点】 物质分离、提纯的常见物理方法 过滤解读
| A.渗析、蒸馏、萃取 | B.分液、萃取、蒸馏 |
| C.过滤、分液、聚沉 | D.过滤、分液、渗析 |
【知识点】 胶体的性质和应用解读 物质分离、提纯的常见物理方法
①使澄清石灰水变浑浊
②使湿润的蓝色石蕊试纸变红
③使品红溶液褪色
④通入足量NaOH溶液中,再滴加BaCl2溶液,有白色沉淀生成,该沉淀溶于稀盐酸
⑤通入溴水中,能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生
| A.都能证明 | B.都不能证明 |
| C.③④⑤均能证明 | D.只有⑤能证明 |
| A.用托盘天平称取3.23gNaCl固体 | B.用50mL的量筒量取30.12mL的水 |
| C.向小试管中加入100mL稀盐酸 | D.用滴管取约1mL溶液 |
【知识点】 配制一定物质的量浓度的溶液实验的仪器解读
| A.1mol氢气含有的原子数为2NA |
| B.NA个水分子中含有氢原子的物质的量为2 mol |
| C.1 mol 氧气中含有的分子数为2NA |
| D.含有NA个氧原子的硫酸的物质的量是0.25 mol |
| A.Zn+2HCl=ZnCl2+H2↑ |
| B.Ca(ClO)2+2HCl=CaCl2+2HClO |
| C.Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O |
D.3Cl2+6KOH(浓) 5KCl+KClO3+3H2O 5KCl+KClO3+3H2O |
【知识点】 氧化还原反应基本概念
| A.1∶1 | B.1∶2 | C.1∶3 | D.3∶1 |
| A.铁的三种氧化物中铁元素的化合价完全相同 |
| B.都是碱性氧化物,都能与盐酸反应生成氯化铁和水 |
| C.氧化亚铁在空气中加热可生成更稳定的四氧化三铁 |
| D.四氧化三铁中铁元素有+2价和+3价,它是一种混合物 |
【知识点】 铁的氧化物

制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,即可生成黑色的、分散质粒子直径在5.5~36nm之间的磁流体。下列说法中正确的是
| A.所得分散系属于悬浊液 |
| B.该分散系能产生丁达尔效应 |
| C.所得的分散系中分散质为Fe2O3 |
| D.所得的分散系为胶体,且胶粒直径即为氢氧化铁分子直径 |
A.Na+、K+、 、 、 | B. 、 、 、Al3+、 、Al3+、 |
C.Na+、Ca2+、 、 、 | D.K+、 、 、 、 、 |
【知识点】 离子共存 限定条件下的离子共存解读
二、解答题 添加题型下试题
(1)实验①
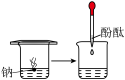 观察到的现象是
观察到的现象是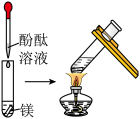 观察到的现象是
观察到的现象是(2)实验③
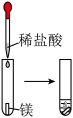 观察到的现象是
观察到的现象是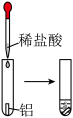 观察到的现象是
观察到的现象是(3)由上述实验,你能得出的结论是
(4)请总结同周期元素金属性的变化规律
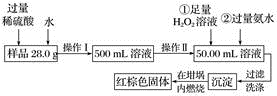
(1)操作Ⅰ中配制溶液时,所用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管以外,还必须有
(2)反应①中加入足量H2O2溶液,反应的离子方程式:
(3)检验沉淀中
 是否洗涤干净的操作是
是否洗涤干净的操作是(4)将沉淀加热,冷却至室温,用天平称量坩埚与加热后固体的总质量为b1g,再次加热并冷却至室温称其质量为b2g,若b1-b2=0.3,还应进行的操作是
(5)坩埚的质量为42.6 g,最终坩埚与加热后的固体的总质量为45.8 g,则样品中铁元素的质量分数为
(6)有同学认为上述方案的实验步骤太繁琐,他认为,只要将样品溶于水充分搅拌,加热、蒸干、灼烧称量即可测得样品中铁元素的质量分数,你认为他的这个方案是否可行?
 ·,B原子L层的电子总数是K层的3倍,0.1 mol C单质能从酸中置换出2.24 L(标准状况)氢气,同时它的电子层结构变成与氖原子相同的电子层结构;D离子的半径比C离子的小,D离子与B离子的电子层结构相同。
·,B原子L层的电子总数是K层的3倍,0.1 mol C单质能从酸中置换出2.24 L(标准状况)氢气,同时它的电子层结构变成与氖原子相同的电子层结构;D离子的半径比C离子的小,D离子与B离子的电子层结构相同。(1)写出A、B、C、D元素的名称:A
(2)D元素在周期表中属于第
(3)用电子式表示A的气态氢化物的形成过程:
(4)A和B的单质充分反应生成的化合物的结构式是
(5)B与C形成的化合物是离子化合物还是共价化合物?如何证明?
三、填空题 添加题型下试题
(1)铝制成铝箔用于食品包装,是利用它的
A.金属光泽 B.延展性C.导电性 D.导热性
(2)铝在空气中会被氧化生成一层致密的氧化膜(氧化物)而对铝起保护作用,但这层氧化膜(氧化物)遇到强酸或强碱都会溶解,请写出其与盐酸反应的离子方程式:
(3)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,相同条件下所得H2的体积之比为
(4)足量的两份铝分别投入到等体积、一定物质的量浓度的HCl、NaOH溶液中,二者恰好完全反应且产生的H2相等,则HCl和NaOH的物质的量浓度之比是
四、解答题 添加题型下试题
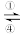 Fe3+
Fe3+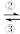 FeO42-(高铁酸根离子)。回答下列有关问题:
FeO42-(高铁酸根离子)。回答下列有关问题:(1)Fe与过量盐酸反应可以制取FeCl2。若用反应所得的酸性溶液,实现上述①、④的转化,要求产物纯净,可选用
a.Cl2 b.Fe c.Cu d.KMnO4
(2)如下化学方程式中:Fe2O3+3NaClO+4KOH=2K2FeO4(高铁酸钾)+3NaCl+2H2O,还原剂是
(3)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是
(4)某同学为了检验家中的一瓶补铁药(成分为FeSO4)是否变质,查阅了有关资料,得知Fe2+能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,并结合已学的知识设计了如下实验:将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,在试管Ⅰ中滴入酸性高锰酸钾溶液,在试管Ⅱ中滴入KSCN溶液。
①请你填出该同学实验中出现以下现象时应得出的结论:
| 实验现象 | 试管Ⅰ | 试管Ⅱ | 结论 |
| a | 褪色 | 不变红 | |
| b | 不褪色 | 变红 | |
| c | 褪色 | 变红 |
(1)把氯气通入紫色石蕊溶液中,可以观察到的现象是
(2)氯气与水反应生成次氯酸(HClO)具有杀菌作用,常用于自来水消毒。请写出氯气与水反应的化学方程式:
(3)某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。其反应原理为(用化学方程式表示):
(4)某同学帮助水质检测站配制480 mL 0.5 mol·L-1NaOH溶液以备使用:
①该同学应称取NaOH固体
②上述实验除了需要托盘天平、药匙、烧杯、玻璃棒、量筒等仪器外,还需要的仪器有
③下列操作使配制的NaOH溶液浓度偏低的有
A.将砝码放在左盘上,NaOH放在右盘上进行称量
B.定容的仰视刻度线
C.定容摇匀后,液面下降,又加水至刻度线
D.整个配制过程中,容量瓶不振荡
(5)取上述配制的NaOH溶液
【知识点】 氯气的化学性质 一定物质的量浓度的溶液的配制
试卷分析
试卷题型(共 32题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 氧化性、还原性强弱的比较 | |
| 2 | 0.65 | 氧化还原反应基本概念 | |
| 3 | 0.85 | 氧化性、还原性强弱的比较 氧化还原反应的应用 氧化还原反应的规律 | |
| 4 | 0.65 | 单质和化合物 酸、碱、盐、氧化物的概念及其相互联系 | |
| 5 | 0.65 | 化学实验基础操作 综合实验设计与评价 纯碱的生产 | |
| 6 | 0.65 | 分类方法的应用 无机物质的分类 | |
| 7 | 0.4 | 基于氧化还原反应守恒规律的计算 铜与强氧化性酸的反应 电子转移计算 | |
| 8 | 0.85 | 钠与水反应原理 | |
| 9 | 0.65 | 物质的量有关计算 化学方程式中物质的量的运用 氮氧化物溶解于水的相关计算 二氧化氮与水反应 | |
| 10 | 0.85 | 氧化还原反应的几组概念 | |
| 11 | 0.94 | 胶体的性质和应用 | |
| 12 | 0.85 | 物质分离、提纯的常见物理方法 | |
| 13 | 0.94 | 氧化还原反应的几组概念 | |
| 14 | 0.85 | 阿伏加德罗定律 | |
| 15 | 0.94 | 硅酸盐组成的表示方法 | |
| 16 | 0.65 | 钠单质的保存与用途 仪器使用与实验安全 | |
| 17 | 0.85 | 物质分离、提纯的常见物理方法 过滤 | |
| 18 | 0.65 | 胶体的性质和应用 物质分离、提纯的常见物理方法 | |
| 19 | 0.65 | 二氧化硫的化学性质 二氧化硫与二氧化碳的性质区别 酸性氧化物的通性 二氧化硫的漂白性 | |
| 20 | 0.85 | 配制一定物质的量浓度的溶液实验的仪器 | |
| 21 | 0.85 | 阿伏加德罗常数的应用 根据n=N/NA进行相关计算 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 22 | 0.65 | 氧化还原反应基本概念 | |
| 23 | 0.65 | 铝与酸溶液反应 铝与强碱溶液反应 氢氧化铝的制备 | |
| 24 | 0.65 | 铁的氧化物 | |
| 25 | 0.85 | 胶体 分散系概念及其分类 胶体的定义及分类 胶体的性质和应用 | |
| 26 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 二、解答题 | |||
| 27 | 0.65 | 钠与水反应原理 同主族元素性质递变规律理解及应用 同主族元素性质递变规律探究实验 元素非金属性强弱的比较方法 | 实验探究题 |
| 28 | 0.65 | 铁的氧化物 亚铁盐 物质含量的测定 综合实验设计与评价 | 实验探究题 |
| 29 | 0.65 | 原子、离子、原子团及其电子式的书写与判断 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 | 无机推断题 |
| 31 | 0.65 | 氧化还原反应的几组概念 铁的其他化合物 铁盐的检验 铁三角转化条件分析及判断 | 实验探究题 |
| 32 | 0.65 | 氯气的化学性质 一定物质的量浓度的溶液的配制 | 实验探究题 |
| 三、填空题 | |||
| 30 | 0.65 | 铝的物理性质及用途 铝与酸溶液反应 铝与强碱溶液反应 金属材料的性质及利用 | |



